
【题目】根据所学知识完成题目:
(1)反应A+3B2C+2D在四种不同情况下的反应速率分别如下:
①.v(B )=3.6molL﹣1min﹣1 ②.v(A )=0.15molL﹣1s﹣1
③.v(C)=0.5molL﹣1s﹣1 ④.v(D)=0.6molL﹣1s﹣1 ,
该反应进行的由快到慢顺序为 (填序号)
(2)已知拆开1mol H﹣H键、1mol N﹣H键、1mol N≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为 .
【答案】
(1)④>③>②>①
(2)N2(g)+3H2(g)?2NH3(g)△H=﹣92kJ?mol﹣1
【解析】解:(1)反应速率与化学计量数的比值越大,反应速率越快,则① ![]() =0.04;②
=0.04;② ![]() =0.15;③
=0.15;③ ![]() =0.25;④
=0.25;④ ![]() =0.3,该反应进行的由快到慢顺序为④>③>②>①,所以答案是:④>③>②>①;(2)在反应N2+3H22NH3中,断裂3molH﹣H键,1mol N三N键共吸收的能量为:3×436kJ+946kJ=2254kJ,生成2mol NH3 , 共形成6mol N﹣H键,放出的能量为:6×391kJ=2346kJ,吸收的能量少,放出的能量多,该反应为放热反应,放出的热量为:2346kJ﹣2254kJ=92kJ,即N2(g)+3H2(g)2NH3(g)△H=﹣92kJmol﹣1 , 所以答案是:N2(g)+3H2(g)2NH3(g)△H=﹣92kJmol﹣1 .
=0.3,该反应进行的由快到慢顺序为④>③>②>①,所以答案是:④>③>②>①;(2)在反应N2+3H22NH3中,断裂3molH﹣H键,1mol N三N键共吸收的能量为:3×436kJ+946kJ=2254kJ,生成2mol NH3 , 共形成6mol N﹣H键,放出的能量为:6×391kJ=2346kJ,吸收的能量少,放出的能量多,该反应为放热反应,放出的热量为:2346kJ﹣2254kJ=92kJ,即N2(g)+3H2(g)2NH3(g)△H=﹣92kJmol﹣1 , 所以答案是:N2(g)+3H2(g)2NH3(g)△H=﹣92kJmol﹣1 .


科目:高中化学 来源: 题型:
【题目】设NA表示阿伏伽德罗常数的值,下列叙述中正确的是( )
A.18gD2O和18gH2O中含有的质子数均为10NA
B.0.5mol/L亚硫酸钠溶液中含有的SO ![]() 的物质的量为0.5mol
的物质的量为0.5mol
C.过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA
D.过量铜片与100mL18mol/L的浓硫酸反应,转移的电子数为1.8NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程中不涉及氧化还原反应的是( )
A.由植物油制备人造黄油
B.用氯化铁溶液腐蚀印刷线路板
C.用牺牲阳极的阴极保护法防止金属被腐蚀
D.在蛋白质溶液中加入饱和硫酸铵溶液,析出白色固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构如右图。下列叙述正确的是( )
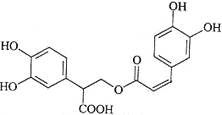
A. 迷迭香酸属于芳香烃
B. 1mol迷迭香酸最多能和9mol氢气发生加成反应
C. 迷迭香酸可以发生水解反应、取代反应和酯化反应
D. 1mol迷迭香酸最多能和含5mol NaOH的水溶液完全反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关Al与NaOH溶液反应的说法中,正确的是( )
A.铝是还原剂,其氧化产物是NaAlO2
B.NaOH是氧化剂,其还原产物是H2
C.Al是还原剂,H2O和NaOH都是氧化剂
D.水是氧化剂,铝被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高分子分离膜可以让某些物质有选择地通过而将物质分离,下列应用不属于高分子分离膜的应用范围的是( )
A.分离工业废水,回收废液中的有用成分
B.将化学能转换成电能,将热能转换成电能
C.食品工业中,浓缩天然果汁、乳制品加工和酿酒
D.海水淡化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有部分短周期元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
T | M层上有6个电子 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
Z | 元素最高正价是+7价 |
W | 其单质既能跟酸反应,又能跟碱反应,都产生H2 |
(1)元素X的一种同位素可测定文物年代,这种同位素的符号是 .
(2)元素Y与氢元素形成一种离子YH4+ , 写出该微粒的化学式:(用元素符号表示).
(3)元素Z与元素T相比,非金属性较强的是(用元素符号表示),下列表述中能证明这一事实的是 . ①常温下Z的单质和T的单质状态不同
②Z的氢化物比T的氢化物稳定
③一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质的性质差异性是学习的重要方法之一.T、X、Y、Z四种元素的最高价氧化物对应的水化物中化学性质明显不同于其他三种的是(填化学式),理由是 . Z的最高价氧化物对应的水化物与W的最高价氧化物对应的水化物反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】各物质之间的转化关系如图,部分生成物省略.C、D是由X、Y、Z中两种元素组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10.D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷线路板.请回答下列问题:
(1)G元素在周期表中的位置 , C的电子式 .
(2)比较Y与Z的原子半径大小>(填写元素符号).
(3)写出E和乙醛反应的化学反应方程式(有机物用结构简式表示);反应类型: .
(4)写出实验室制备G的离子反应方程式 .
(5)气体D与NaOH溶液反应可生成两种盐P和Q,在P中Na的质量分数为43%,其俗名为 .
(6)实验室中检验L溶液中的阳离子常选用溶液,现象是 .
(7)A中包含X、Y、Z元素,A的化学式为
(8)研究表明:气体D在一定条件下可被还原为晶莹透明的晶体N,其结构中原子的排列为正四面体,请写出N及其1种同素异形体的名称、 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值.下列说法正确的是( )
A.14g聚丙烯中含C﹣H键总数目为2NA
B.1molFe与足量的稀硝酸反应转移电子总数目为2NA
C.标准状况下,44.8L乙醛中含乙醛分子总数目为2NA
D.常温常压下,200g质量分数为17%H2O2溶液中含氧原子总数目为2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com