
����Ŀ����ȡm gþ���Ͻ���һ��Ũ�ȵ�ϡ������ǡ����ȫ�ܽ�(����Ļ�ԭ����ֻ��NO)����Ӧ��Ļ����Һ�еμ�b mol/LNaOH��Һ�����μӵ�V mLʱ���õ���������ǡ��Ϊ���ֵn g ���������йظ�˵���в���ȷ���У� ��
A.��״��������N�����Ϊ![]() L
L
B.������OH-������Ϊ17bVg
C.ǡ���ܽ����Һ�е�NO3-�����ʵ���Ϊ![]() mol
mol
D.��Ͻ�Ӧ����������ʵ���Ϊ(![]() +
+![]() )mol
)mol
���𰸡�B
��������
A�����ݵ����غ�ԭ��������NOʱ��![]() ��
��![]() �۵�Nԭ�ӵ�3�����ӣ��������NO�����ʵ���Ӧ����ת�Ƶ��ӵ�����֮һ����
�۵�Nԭ�ӵ�3�����ӣ��������NO�����ʵ���Ӧ����ת�Ƶ��ӵ�����֮һ����![]() ��������ڱ�״����Ϊ
��������ڱ�״����Ϊ![]() ����A��ȷ��
����A��ȷ��
B������Ϊ����������������þ����������������þ�Ͻ�����������������֮�ͣ����Գ�����������������Ϊ![]() g�����ߵ���17bV
g�����ߵ���17bV![]() 10-3g����B����
10-3g����B����
C��ǡ���ܽ����Һ�е�![]() ���ӵ����ʵ������ڳ������������Һ��
���ӵ����ʵ������ڳ������������Һ��![]() ���ӵ����ʵ����������������ʱ����Һ�е�����ֻ��������
���ӵ����ʵ����������������ʱ����Һ�е�����ֻ��������![]() ������������������ӵ����ʵ�����ȣ�
������������������ӵ����ʵ�����ȣ�![]() ����C��ȷ��
����C��ȷ��
D���μӷ�Ӧ���������������ã���������������ã���Ϊ�������![]() ����������
����������![]() �����ʵ������������Ƶ����ʵ���Ϊ
�����ʵ������������Ƶ����ʵ���Ϊ![]() ��������������������ʵ�������NO�����ʵ���Ϊ
��������������������ʵ�������NO�����ʵ���Ϊ![]() ��������Ͻ�Ӧ����������ʵ���Ϊ
��������Ͻ�Ӧ����������ʵ���Ϊ![]() ����D��ȷ��
����D��ȷ��
�𰸣�B��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ƶ�˼ά�����ڻ�ѧѧϰ���о��г����������Ľ��ۣ�������ƵĽ�������Ҫ������ʵ���ļ������ȷ������ȷ������м������ƽ����У���ȷ����
A.��2Cu+O2![]() 2CuO���Ƴ�ͬ�����Ҳ��Cu+S
2CuO���Ƴ�ͬ�����Ҳ��Cu+S![]() CuS
CuS
B.![]() �ɱ�ʾΪ
�ɱ�ʾΪ![]() ����
����![]() �ɱ�ʾΪ
�ɱ�ʾΪ![]()
C.������![]() ��ʯ��ˮ��Ӧ����
��ʯ��ˮ��Ӧ����![]() ������
������![]() ͨ��Ư����Һ�У�������
ͨ��Ư����Һ�У�������![]() ��HClO
��HClO
D.![]() ��������Ʒ�Ӧֻ����
��������Ʒ�Ӧֻ����![]() ��
��![]() ��
��![]() ���������һ������
���������һ������![]() ��
��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�з���ͼ�����

A.2SO3(g) ![]() 2SO2(g)��O2(g) ��H=��Q2kJ��mol��1(Q2>0)
2SO2(g)��O2(g) ��H=��Q2kJ��mol��1(Q2>0)
B.H2(g)��CO(g) ![]() C(s)��H2O(g) ��H=��Q4kJ��mol��1(Q4>0)
C(s)��H2O(g) ��H=��Q4kJ��mol��1(Q4>0)
C.N2(g)��3H2(g) ![]() 2NH3(g) ��H =-Q1kJ��mol-1 ��Q1>0��
2NH3(g) ��H =-Q1kJ��mol-1 ��Q1>0��
D.4NH3(g)��5O2(g) ![]() 4NO(g)��6H2O(g) ��H =-Q3kJ��mol-1 ��Q3>0��
4NO(g)��6H2O(g) ��H =-Q3kJ��mol-1 ��Q3>0��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ֽ���������ĩ15 g�����������ᷴӦʱ���ɱ�״����11.2 L������������������Ľ��������
A.Mg��FeB.Zn��AgC.Zn��FeD.Mg��Al
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2���ǻ��춡������������ˮ����һ��Ӧ�����л��ϳɺ�ҩ������Ļ���ԭ�ϡ�

��1��2���ǻ��춡�������ķ���ʽΪ_________����ͬ��ѧ���������ں˴Ź�������ͼ���в�ͬ�����շ壬��2���ǻ��춡��������_________�����շ壻
��2���٢ڵķ�Ӧ���ͷֱ�Ϊ_________��_________��
��3����֪IΪ�������I��B�Ļ�ѧ����ʽΪ_________��
��4�����۲���F�Ľṹ��ʽΪ_________��
��5�������![]() ��
�� ��˵����ȷ����_________��˫ѡ������ĸ����
��˵����ȷ����_________��˫ѡ������ĸ����
A����������FeCl3��Һ����ɫ����ǰ�߲���
B�����߶�������NaHCO3��Һ��Ӧ�ų�CO2
C�����߶�����������������Һ������Ӧ�����������ʵ������ʱ�������������Ƶ��������
D�����߶����������������ӳɷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Կ����еĵ���Ϊԭ���Ʊ����ᣬ�ϳ���·��ͼ(��Ӧ���������ַ�Ӧ�����������ȥ)��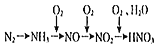 ��֪�����к��������������Ϊ78%������100 L(������ɱ�״����)�����Ʊ����ᣬ�������Ͽ��Ƶ���������ļ���ʽ��ȷ����
��֪�����к��������������Ϊ78%������100 L(������ɱ�״����)�����Ʊ����ᣬ�������Ͽ��Ƶ���������ļ���ʽ��ȷ����
A.![]() B.
B.![]() mol
mol
C.![]() ��63 gD.2��100��78% L
��63 gD.2��100��78% L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ǹ�ҵ����ȡ�����һ�ַ�����

��ش���������(��Ԫ������Ӧ��Ԫ�ط��ű�ʾ)��
��1�����������������У������û���Ӧ����____(�Ӧ����)��
��2��д����Ӧ�۵Ļ�ѧ����ʽ____��
��3��������W����;�ܹ㣬ͨ��������������ҵ����ֽ��ҵ���ϼ�����������������������Ȼˮ������������ʯӢɰ�ʹ��һ��������ϼ�����1 373��1 623 K��Ӧ�����ɻ�����W���仯ѧ����ʽ��____��
��4��A��B��C���������������ܼ���������Ϊ����Ŀ���һ��������___(�ѧʽ)���ֱ�ͨ��W��Һ���ܵõ���ɫ������������___(�ѧʽ)��
��5����ҵ�Ϻϳɰ���ԭ��H2���Ʒ����Ȱѽ�̿��ˮ������Ӧ����ˮú�������ᴿˮú���õ�������H2���ᴿˮú���õ�������H2�Ļ�ѧ����ʽΪ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����84������Һ(��ҵ����Cl2��NaOH��Ӧ�Ƶã�������������Ư�ף�����ʵ������ķ�������ȷ����
ʵ����� |
|
|
|
ʵ������ | ��Ϻ���Һ��pH=9.9,��ʱ����δ��ɫ��һ��ʱ�����ɫ��ȥ�� | ��Ϻ���ҺpH=5.0����ɫѸ����ȥ������������� | ��Ϻ���ҺpH=3.2����ɫѸ����ȥ���������������壬ʹʪ��ĵ��۵⻯����ֽ������ |
A.�Ա�ʵ����������������ɫѸ����ȥ��ԭ���Ƿ����˷�ӦClO+H+�THClO
B.ʵ�����в�����������Cl2����HClO�ֽ�õ���2HClO�TCl2��+H2O
C.�Ա�ʵ������������Һ��pH���ܻ�Ӱ��ClO�������Ի�Cl�Ļ�ԭ��
D.������������84������Һ��Ư��Ч��������Ҫ���غ��ʵ�pH���ܰ�ȫʹ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���� NA Ϊ�����ӵ³�������ֵ������˵����ȷ���ǣ�������
A.18 g H2O ���� 10NA ������
B.1 mol ������ 3NA ��̼̼˫��
C.��״���£�22.4 L ��ˮ���� NA �� NH3 ����
D.�����£�112 g ��ƬͶ������Ũ H2SO4 ������ 3NA �� SO2 ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com