
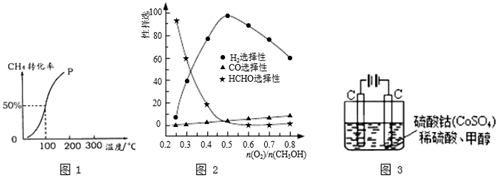
| 1 |
| 2 |
| c(H2) |
| c(CH3OH) |
| n(O2) |
| n(CH3OH) |
| ||
| △t |
| 1 |
| 2 |
| ||
| 5min |
| 0.005×0.0153 |
| 0.005×0.015 |
| 1 |
| 2 |
| c(H2) |
| c(CH3OH) |
| n(O2) |
| n(CH3OH) |


科目:高中化学 来源: 题型:
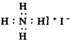
14 6 |
| A、6个 | B、5个 | C、4个 | D、3个 |
查看答案和解析>>
科目:高中化学 来源: 题型:
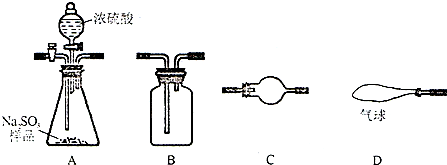
| 实验装置(填字母) | D | ||||||
| 装置中所盛药品(填序号) | ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
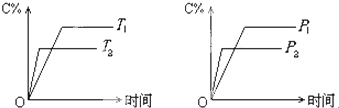
| A、达到平衡后,若使用催化剂,C的体积分数增大 |
| B、达到平衡后,若使温度升高,化学平衡向逆反应方向移动 |
| C、化学方程式中n>c+f |
| D、达到化学平衡后,增加A的量有利于化学平衡向正反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | 实验步骤 | 现象 | 探究目的和结论 |
| ① | 将刚削皮的苹果立刻放入隔绝空气的环境中 | 相当长一段时间内,无明显变化 | |
| ② | 将刚削皮的苹果立刻放入90℃~95℃的水中2min,再放在空气中. 再将另一块刚削皮的苹果立刻放入稀盐酸中浸泡2min后取出洗净,再放在空气中.将盐酸改为酒精、醋酸铅溶液进行相同实验. | 相当长一段时间内,均无明显变化 | |
| ③ | 在刚削皮的苹果上滴加FeCl3溶液. | 苹果由白色变为绿色 | 探究目的:探究苹果中是否含有酚类物质.结论:苹果中含有酚类物质. |
查看答案和解析>>
科目:高中化学 来源: 题型:
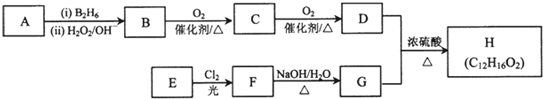
| (i)B2H6 |
| (ii)H2O2/OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 X、Y、Z、W、T是短周期表中的5种主族元素.X基态原子核外L层p电子数等于s电子数.Y的一种核素的质量数为19,中子数比质子数多1.T-离子核外电子数与氩原子的核外电子数相同.X、Y、Z、W的第一电离能与它们的核电荷数的关系如图所示.
X、Y、Z、W、T是短周期表中的5种主族元素.X基态原子核外L层p电子数等于s电子数.Y的一种核素的质量数为19,中子数比质子数多1.T-离子核外电子数与氩原子的核外电子数相同.X、Y、Z、W的第一电离能与它们的核电荷数的关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
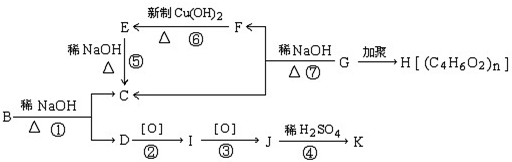
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com