
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是
①加入铝粉只有氢气产生的溶液中:Na+、SO42-、NO3-、Mg2+
②pH=11的溶液中:![]() 、Na+、AlO2-、NO3-、S2-、
、Na+、AlO2-、NO3-、S2-、![]()
③水电离的H+浓度为10-12mol·L-1的溶液中:Cl-、![]() 、NO3-、
、NO3-、![]()
④加入Mg能放出H2的溶液中:Mg2+、NH4+、Cl-、K+、![]()
⑤使甲基橙变黄的溶液中:Fe2+、MnO4-、NO3-、Na+、![]()
⑥中性溶液中:Fe3+、Na+、NO3-、Cl-
A.①③⑤ B.②④ C.①②④ D.②④⑥
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】1920年参与建设亚洲第一座纯碱厂——永利制碱厂,为我国纯碱工业发展做出杰出贡献的化学家是
A. 屠呦呦 B. 侯德榜 C. 张青莲 D. 徐光宪
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)CrO42和Cr2O72在溶液中可相互转化。室温下,初始浓度为1.0mol·L1的Na2CrO4溶液中c(Cr2O72)随c(H+)的变化如下图所示。
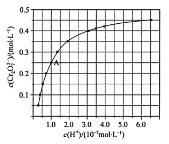
①用离子方程式表示Na2CrO4溶液中的转化反应。
②由图可知,溶液酸性增大,CrO42的平衡转化率__________(填“增大“减小”或“不变”)。
③升高温度,溶液中CrO42的平衡转化率减小,则该反应的ΔH_______0(填“大于”“小于”或“等于”)。
(2)+6价铬的化合物毒性较大,常用NaHSO3将废液中的Cr2O72还原成Cr3+,反应的离子方程式为。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,若锥形瓶内是水,分液漏斗内的液体也是水,向烧杯内滴加水时,发现U形管内液体慢慢右移,恢复到原温度后液面左边与右边基本相平,则烧杯内的物质是
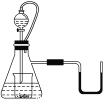
A.过氧化钠 B.氧化钠
C.钠 D.钾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是中学化学常见单质, X、Y、Z、M、N、W、H、K是常见化合物,X是B和C的化合产物,它们之间有如下转化关系(反应物和产物中的H2O已略去):
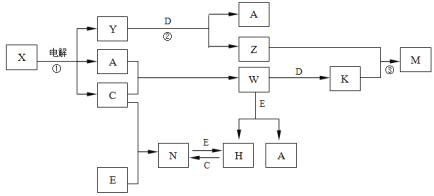
(1)Y的电子式为 ,构成E单质的元素在周期表中位于______________。
(2)反应①的离子方程式为______________
反应③的离子方程式为______________
(3)某工厂用C制漂白粉。
①写出制漂白粉的化学方程式______________
②为测定该工厂制得的漂白粉中有效成分的含量,某小组进行了如下实验:称取漂白粉2.0g,研磨后溶解,配制成250mL溶液,取出25.00mL加入到锥形瓶中,再加入过量的KI溶液和过量的硫酸,此时发生的离子方程式为: ,静置。待完全反应后,用0.1mol·L-1的Na2S2O3溶液做标准溶液滴定反应生成的碘,已知反应式为:2Na2S2O3+I2=Na2S4O6+2NaI,共用去Na2S2O3溶液20.00mL。则该漂白粉中有效成分的质量分数为 (保留到小数点后两位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是:
A.乙烯使溴水或酸性高锰酸钾褪色均属于加成反应
B.用乙醇与浓硫酸加热至170℃制乙烯的反应属于取代反应
C.用重铬酸钾溶液检验司机是否酒驾所发生的反应属于乙醇的氧化反应
D.用“地沟油”生产生物柴油只发生酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取钠-镁合金7.0克进行如下实验:

(1)写出Mg在CO2中燃烧的化学方程式__________。
(2)向溶液1中加过量的NaOH溶液,发生反应的离子方程式为___________。
(3)写出合金的化学组成____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数。下列说法正确的是( )
①在标准状况下,NA个SO3分子所占的体积为22.4L
②S2和S8的混合物共6.4g,其中所含硫原子数一定为0.2NA
③标准状祝下,22.4LNO和11.2LO2混合后气体的分子总数为1.5 NA
④在标准状况下,22.4LCl2与足量的氢氧化钾溶液反应转移的电子数为NA
A.②④ B.①② C.③④ D.①③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com