
����Ŀ��ʵ�����Ա���ȩΪԭ���Ʊ����屽��ȩ�ķ�Ӧ���£�
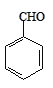 +Br2
+Br2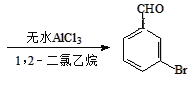 +HBr
+HBr
��֪��(1)���屽��ȩ�¶ȹ���ʱ�ױ�������
(2)�塢����ȩ��1,2-�������顢���屽��ȩ�ķе���±���
���� | �� | ����ȩ | 1,2-�������� | ���屽��ȩ |
�е�/�� | 58.8 | 179 | 83.5 | 229 |
����1����һ����ȵ���ˮAlCl3��1,2-��������ͱ���ȩ��ֻ�Ϻ�װ��������ƿ����ͼ��ʾ���������μӾ�Ũ��������������Һ�壬���·�Ӧһ��ʱ�䣬��ȴ��
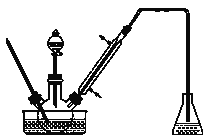
����2������Ӧ����ﻺ������һ������ϡ�����У����衢���á���Һ���л�����10% NaHCO3��Һϴ�ӡ�
����3����ϴ�ӵ��л������������ˮMgSO4���壬����һ��ʱ�����˳�MgSO4nH2O���塣
����4����ѹ�����л��㣬�ռ���Ӧ��֡�
(1)ʵ��װ���������ܵ���Ҫ������_______����ƿ��ӦΪ_______���ѧʽ����Һ��
(2)����1��Ӧ�����У�Ϊ���ԭ�������ʣ����˵��¶ȷ�ΧΪ������ţ�_________��
A ��229�� B 58.8��~179�� C ��58.8��
(3)����2����10% NaHCO3��Һϴ�ӣ���Ϊ�˳�ȥ�����л����________(�ѧʽ)��
(4)����3�м�����ˮMgSO4�����������_______��
(5)����4�в��ü�ѹ������Ϊ�˷�ֹ_______��
(6)��ʵ���м�����5.3 g����ȩ���õ�3.7 g���屽��ȩ������屽��ȩ����Ϊ___��
(7) ![]() ��һ����Ҫ��ҽҩ�м��塣����ƺ���������
��һ����Ҫ��ҽҩ�м��塣����ƺ���������![]() �ϳ������м��塣(����ԭ����ѡ���÷�Ӧ����ͼ��ʾ����ע����Ҫ�ķ�Ӧ����)��_______
�ϳ������м��塣(����ԭ����ѡ���÷�Ӧ����ͼ��ʾ����ע����Ҫ�ķ�Ӧ����)��_______
���磺![]()
![]()
![]()
![]()
![]()
���𰸡��������� NaOH C Br2 ��ȥ�л����ˮ ���屽��ȩ���¶ȹ��߱����� 40% ![]()
![]()
![]()
![]()
![]()
��������
����ȩ�������Ȼ�������������60��ʱ��Ӧ���ɼ��屽��ȩ��ͬʱ�����廯�⣬�����������ɵü��屽��ȩ�����ɵ��廯��������������Һ���գ���ֹ��Ⱦ�������л����к����壬�����Ȼ��⣬����̼�����Ƴ�ȥ���л��������ˮMgSO4���壬��������ˮ�����ã���ѹ���ɽ��ͷе㣬�����¶ȹ��ߣ����¼��屽��ȩ���������Դ˽����⡣
(1)�����ӷ���Ϊʹ���ַ�Ӧ��Ӧ��������������ʵ��װ���������ܵ���Ҫ������������������Ӧ����ȡ����Ӧ�����ɼ��屽��ȩ��ͬʱ���ɣ�Br��������������Һ���գ���ֹ��Ⱦ����������ƿ��ӦΪNaOH��Һ��
(��)���˵��¶ȷ�ΧΪҪȷ����Ӧ�ﲻ�ܳ�����Ӧ��ķе㼴�ɣ�С����ķе㣬��58.8�棬��ѡC��
(3)����Ӧ����ﺬ���壬��������һ������ϡ�����У�����̼�����ƣ������塢�Ȼ��ⷴӦ���ʲ���2����10% NaHCO3��Һϴ�ӣ���Ϊ�˳�ȥ�����л����Br2��
(4)��ϴ�ӵ��л��ຬ��ˮ��������ˮMgSO4���壬����ȡ��ȥ�л����ˮ�����ã�
(5)���屽��ȩ�к���ȩ�����ױ����������Բ��ü�ѹ���ɽ��ͷе㣬�����¶ȹ��ߣ����¼��屽��ȩ��������
(6)����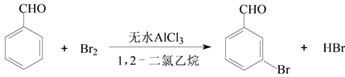 ����5.3g����ȩ��ȫ��Ӧ����xg���屽��ȩ������106:185=5.3:x,���x=9.25g,���Լ��屽��ȩ����3.7g/9.25g
����5.3g����ȩ��ȫ��Ӧ����xg���屽��ȩ������106:185=5.3:x,���x=9.25g,���Լ��屽��ȩ����3.7g/9.25g ![]() 100%=40%;
100%=40%;
(7) ![]() �ڸ��������Һ����������
�ڸ��������Һ����������![]() ��
��![]() ����Ũ���������״�����������Ӧ����
����Ũ���������״�����������Ӧ����![]() ���ϳ�·�����£�
���ϳ�·�����£�
![]()
![]()
![]()
![]()
![]() ��
��


 ��ѧʵ����ϵ�д�
��ѧʵ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ǵڶ����ڲ���Ԫ�ػ�̬ԭ�ӵĵ����Ų�ͼ���ݴ�����˵���������(����)


A. ÿ��ԭ�ӹ�������ֻ������2������
B. ��������ͬһ�ܼ�ʱ���������ȵ���ռ��һ�����
C. ÿ���ܲ������е��ܼ��������ܲ������(n)
D. ��ԭ�ӹ������2�����ӣ���������״̬�෴
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ���У���ѡװ�û�ʵ����ƺ�������
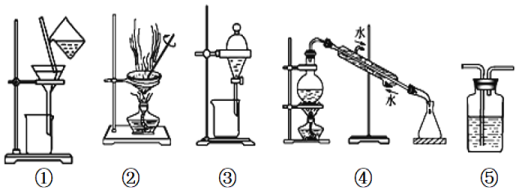
A. ��ͼ�ٺ͢���ʾװ�ÿ��Գ�ȥNa2CO3�е�CaCO3���ʣ������Na2CO3����
B. ���Ҵ���ȡ��ˮ�е���ѡ��ͼ����ʾװ��
C. ��ͼ����ʾװ�ÿ��Է����Ҵ�ˮ��Һ
D. ͼ����ʾװ����ʢ�б���Na2CO3��Һ��ȥCO2�к��е�����HCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(![]() )���������ȶ���������350������Ѹ�ٷֽ⡣ʵ�����Ʊ���Ӧ��
)���������ȶ���������350������Ѹ�ٷֽ⡣ʵ�����Ʊ���Ӧ��![]() ��װ����ͼ��ʾ������˵���������( )
��װ����ͼ��ʾ������˵���������( )
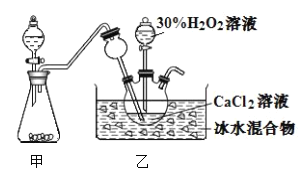
A.����©������������������
B.��װ�ÿ�����Ũ��ˮ�ͼ�ʯ�����Ʊ�����
C.��ˮ��������Ҫ�����Ƿ�ֹ���ɵĹ����������ȷֽ�
D.��Ӧ������![]() �����к�
�����к�![]() �����������ɵ�
�����������ɵ�![]() ���ٽ���Ӧ����
���ٽ���Ӧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У�ǰ�߸պ��Ǻ����������� (����)
A. 2 mol H2O��Ħ��������1 mol H2O��Ħ������
B. 200 mL 1 mol��L-1�Ȼ�����Һ��c(Cl-)��100 mL 2 mol��L-1�Ȼ�����Һ��c(Cl-)
C. 64 g������������ԭ�����ͱ�״����22.4 Lһ����̼����ԭ����
D. 20% NaOH��Һ��NaOH�����ʵ���Ũ�Ⱥ�10% NaOH��Һ��NaOH�����ʵ���Ũ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Һ������ͼ��ʾ������˵���������( )
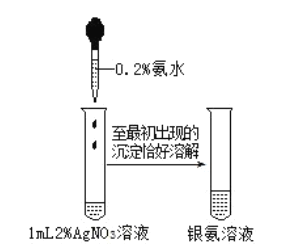
��֪��![]() ��
��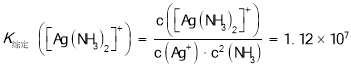
A.�Ƶõ�������Һ�����ڻ�ԭ���ǵļ���
B.![]() ���
���![]() ��
��![]() ��
��
C.������Һ���ܳ��ڴ�ţ���Ҫ��������
D.![]() ��������ڰ�ˮ�õ�������Һ
��������ڰ�ˮ�õ�������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������ơ���װ��ʹ�÷�������ѧ��ѧʵ��Ļ�������ͼΪ����ʵ��װ�á�
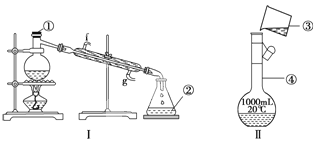
��1��д���������������ƣ���__________����__________��
��2��������װ�����������Ȼ�̼�;ƾ��Ļ�����ȱ�ٵ�������______________��������������������е�ʵ�����������Ϊ____________��
��3����Na2CO3��10H2O���壬����0.2 mol��L��1��Na2CO3��Һ480 mL��
��Ӧ��ȡNa2CO3��10H2O�����������__________��
������������������ƽ���ձ�����������ҩ�ס���Ͳ�⣬����Ҫ__________(����������)��
���������в�����������Һ��Ũ�Ȳ�����Ӱ�죬�������Ҫ��
A��Na2CO3��10H2O����ʧȥ�˲��ֽᾧˮ |
B�����������������ij���������������(ʹ������) |
C������̼���ƾ���ʱ������������ |
D������ƿδ������ʹ�� |
��������������ҺŨ��ƫ�ߵ���___________(����ĸ)
��װ������ijͬѧת����Һ��ʾ��ͼ��ͼ�еĴ�����__________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͭ����Ҫ������Cu�Ļ������ڿ�ѧ�о���ҵ�����о���������;����CuSO4��Һ���������Һ�����Һ�ȡ���ش��������⣺
��1��Ԫ�ؽ�(Au)�������ڱ��еĵ�6���ڣ���Cuͬ�壬��ԭ�����������Ų�ʽΪ_________��һ��ͭ�Ͻ�������������ܶѻ��Ľṹ���ھ�����ͭԭ�Ӵ������ģ���ԭ�Ӵ��ڶ���λ�ã���úϽ���ͭԭ�����ԭ������֮��Ϊ_____���þ����У�ԭ��֮�����������________��
��2������������д���ܣ���ԭ�ӿɽ��뵽��ͭԭ�����ԭ�ӹ��ɵ��������϶�С�����ͭԭ�����ԭ�ӵ�ͬ�������þ��崢���ľ����ṹ��CaF2�Ľṹ���ƣ��þ��崢���Ļ�ѧʽӦΪ_____________��
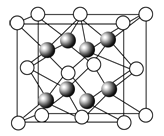
��3��CuSO4����Ĺ�������____��____���������������_______���þ�������____���壻
��4��SO42����S��sp3�ӻ���SO42�������幹����__________________________��
��5��CuSO4��ĩ����������һЩ�л����е���ˮ�֣���ԭ����____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��SO2�ŷ��������л���ɴ�����Ⱦ��ij�о�С���������̿���Ҫ�ɷ�ΪMnO2������������������ͭ�����Ƚ�����������������ͨ�����¼����̣����ѳ�ȼúβ���е�SO2�����Ƶõ�ز���MnO2����Ӧ������ʡ�ԣ���
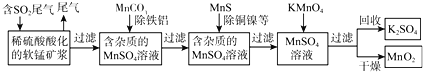
��ش��������⣺
��1����֪��25�桢101kPaʱ��
Mn(s)+O2(g)=MnO2(s) ��H=-520kJ/mol
S(s)+O2(g)=SO2(g) ��H=-297kJ/mol
Mn(s)+S(s)+2O2(g)=MnSO4(s) ��H=-1065kJ/mol
����������Ϣд����MnO2������Ȼ�ѧ����ʽ��______
��2���ڶ�������MnCO3��ԭ����______
��3�������һ������KMnO4ǡ�÷�Ӧ��ȫ�����֤���������õ�MnO2������ϴ�Ӹɾ���______
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com