
| A、SO2+Br2+2H2O═H2SO4+2HBr与2HBr+H2SO4(浓)═Br2+SO2↑+2H2O互为可逆反应 |
| B、既能向正反应方向进行,又能向逆反应方向进行的反应叫可逆反应 |
| C、在同一条件下,同时向正、逆两个方向进行的反应叫可逆反应 |
| D、电解水生成氢气和氧气与氢气和氧气点燃生成水的反应是可逆反应 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、NaClO溶液的消毒原理是使蛋白质变性 |
| B、1molCl2与足量NaOH溶液反应转移1mol电子 |
| C、NaClO溶液的漂白原理与Na2O2、SO2相同 |
| D、“84”消毒液不能与“洁厕灵”(盐酸)共同使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、焰火的五彩缤纷是某些金属元素的性质的展现 |
| B、SiO2可用于制造光导纤维,其性质稳定,不溶于强酸、强碱 |
| C、“光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化合物有关 |
| D、蒙古牧民喜欢用银器盛放鲜牛奶有其科学道理:用银器盛放鲜牛奶,溶入的极微量的银离子,可杀死牛奶中的细菌,防止牛奶变质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
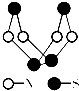 现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.如图是已经合成的最著名的
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.如图是已经合成的最著名的| A、该物质的分子式为SN |
| B、该物质的分子中既有极性键又有非极性键 |
| C、该物质可能是离子化合物 |
| D、该物质的一个分子中含有9个N-S键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 mol H2O和D2O组成的混合物中含有的中子数是NA |
| B、常温常压下,NO2和N2O4的混合物46g中约含有2NA个氧原子 |
| C、1 mol CH3+(碳正离子)中含有电子数为10NA |
| D、在Cu-Zn原电池中,正极产生1.12LH2时,负极产生了0.05 NA 个 Zn2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、观察容量瓶刻度线时仰视 |
| B、小烧杯,玻璃棒没有洗涤 |
| C、所用容量瓶中已有少量水 |
| D、观察容量瓶刻度线时俯视 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硅是一种亲氧元素,在自然界中大多以氧化物和硅酸盐的形式存在 |
| B、硅在地壳中的含量居第一位 |
| C、利用硅的半导体性能,可以制作光电池 |
| D、硅晶体的结构与金刚石类似 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com