
【题目】磷化铝、磷化锌、磷化钙与水反应产生高毒的PH3气体(熔点为-132℃,还原性强、易自燃),可用于粮食熏蒸杀虫。卫生安全标准规定:当粮食中磷化物(以PH3计)的含量低于0.05mg·kg-1时算合格。可用以下方法测定粮食中残留的磷化物含量:
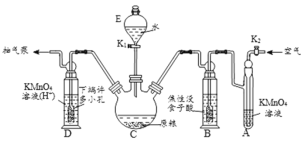
(操作流程)安装吸收装置→PH3的产生与吸收→转移KMnO4吸收溶液→亚硫酸钠标准溶液滴定。
(实验装置)C中盛100g原粮,D中盛有20.00mL1.12×10-4molL-1KMnO4溶液(H2SO4酸化)。
请回答下列问题:
(1)仪器E的名称是___,该仪器可否用于分液操作___?(答“能”或“不能”)
(2)以磷化钙为例,写出磷化钙与水反应除了生成PH3之外,另一产物的电子式是___;检查整套装置气密性的方法是关闭___打开___,抽气泵缓慢抽气,若观察到___(填字母)装置中有气泡产生则气密性良好。
(3)A中盛装KMnO4溶液的作用是___;通入空气的作用是___。焦性没食子酸可以吸收氧化性气体,若没有B装置,则实验中测得PH3含量将___(填“偏低”、“偏高”或“不变”)
(4)D中PH3被氧化成磷酸,所发生反应的离子方程式为___。
(5)把D中吸收液转移至容量瓶中,加水稀释至250mL,取25.00mL于锥形瓶中,用5.0×10-5molL-1的Na2SO3标准溶液滴定剩余的KMnO4溶液,消耗Na2SO3标准溶液11.00mL,则该原粮中磷化物(以PH3计)的含量为___ mgkg-1。
【答案】分液漏斗 不能 ![]() K1 K2 ABD 除去空气中的还原性气体 吹出PH3,使其全部被酸性KMnO4溶液吸收 偏低 5PH3+8MnO
K1 K2 ABD 除去空气中的还原性气体 吹出PH3,使其全部被酸性KMnO4溶液吸收 偏低 5PH3+8MnO![]() +24H+==5H3PO4+8Mn2++12H2O 0.0085
+24H+==5H3PO4+8Mn2++12H2O 0.0085
【解析】
根据题干信息可知,安装吸收装置→PH3的产生与吸收→转移KMnO4吸收溶液→亚硫酸钠标准溶液滴定,已知C中盛有100g原粮,E中盛有20.00mL1.13×10-3molL-1KMnO4溶液(H2SO4酸化),吸收生成的PH3,B中盛装焦性没食子酸的碱性溶液,其作用是吸收空气中的O2,防止氧化装置C中生成的PH3,A中盛装KMnO4溶液的作用除去空气中的还原性气体,据此分析解答。
(1)由E的结构可知,E为球形分液漏斗;梨形分液漏斗下端小,萃取完成以后分液时较容易,球形分液漏斗不能用于分液操作;
(2)磷化钙与水反应生成氢氧化钙和磷化氢,Ca3P2+6H2O=3Ca(OH)2+2PH3↑,另一产物氢氧化钙的电子式为![]() ,检查装置气密性的方法是关闭K1打开K2,抽气泵缓慢抽气,若观察到ABD装置中有气泡产生则说明装置气密性良好;
,检查装置气密性的方法是关闭K1打开K2,抽气泵缓慢抽气,若观察到ABD装置中有气泡产生则说明装置气密性良好;
(3)依据装置图进行分析判断,高锰酸钾溶液是强氧化剂,可以吸收空气中的还原性气体;通入空气,吹出PH3,使其全部被酸性KMnO4溶液吸收,减小实验误差;B中盛装焦性没食子酸的碱性溶液,其作用是吸收空气中的氧气,防止氧化装置C中生成的PH3,若没有B装置,PH3部分被氧气氧化,则实验中测得PH3含量将偏低;
(4)PH3被酸性高锰酸钾氧化成磷酸,高锰酸钾被还原为锰离子,结合电子守恒和电荷守恒、原子守恒配平书写得到离子方程式为:5PH3+8MnO![]() +24H+==5H3PO4+8Mn2++12H2O;
+24H+==5H3PO4+8Mn2++12H2O;
(5)根据2KMnO4+5Na2SO3+3H2SO4=2MnSO4+K2SO4+5Na2SO4+3H2O反应可知,25毫升溶液中剩余KMnO4的量为[5.0×10-5×11×10-3]×![]() =2.2×10-7mol;那么250毫升溶液中剩余KMnO4的量为
=2.2×10-7mol;那么250毫升溶液中剩余KMnO4的量为![]() ×2.2×10-7mol=2.2×10-6mol;与PH3反应的高锰酸钾物质的量=20×1.12×10-4×10-3mol-2.2×10-6mol=4.0×10-8mol,根据5PH3+8MnO
×2.2×10-7mol=2.2×10-6mol;与PH3反应的高锰酸钾物质的量=20×1.12×10-4×10-3mol-2.2×10-6mol=4.0×10-8mol,根据5PH3+8MnO![]() +24H+==5H3PO4+8Mn2++12H2O反应关系可知,消耗PH3的量为[4×10-8]×
+24H+==5H3PO4+8Mn2++12H2O反应关系可知,消耗PH3的量为[4×10-8]×![]() mol;C中盛100g原粮,含有PH3的量[4×10-8]×
mol;C中盛100g原粮,含有PH3的量[4×10-8]×![]() mol,质量为85×10-8g,则该原粮中磷化物(以PH3计)的含量为0.0085mgkg-1。
mol,质量为85×10-8g,则该原粮中磷化物(以PH3计)的含量为0.0085mgkg-1。


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】聚对苯二甲酸丁二醇酯(PBT)是一种性能优异的热塑性高分子材料。PBT的一种合成路线如图所示:
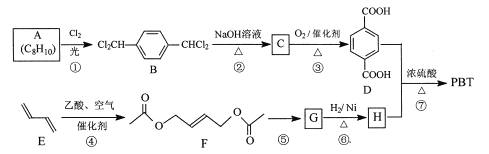
已知:两个羟基同时连在同一碳原子上的结构是不稳定的,它将发生脱水反应: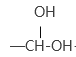 →—CHO
→—CHO
回答下列问题:
(1)A的结构简式为___,C的化学名称为___。
(2)F的分子式为___,⑥的反应类型为___。
(3)⑦的化学方程式是___。
(4)M是H的同分异构体,同时符合下列条件:
a.0.1molM与足量金属钠反应生成氢气2.24L(标准状况)
b.同一个碳原子上不能连接2个羟基
其中核磁共振氢谱显示有3组峰,且峰而积之比为3∶1∶1的结构简式是___。
(5)以2一甲基一1,3一丁二烯为原料(其它试剂任选),设计制备![]() 的合成路线:___。
的合成路线:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中只有T为金属元素。
下列判断错误的是
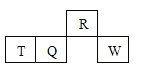
A. 原子半径:T > Q
B. 元素非金属性:Q > R
C. 气态氢化物的热稳定性:R>Q
D. 最高价氧化物对应水化物的酸性: W > Q
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C三种不含结晶水的固体物质的溶解度曲线如图,下列说法中不正确的是

A. t1℃时,A的饱和溶液65 g中含有溶剂50 g
B. 将t1℃ A、B、C三种物质的饱和溶液升温至t2℃ 时,溶液中溶质的质量分数是A=B>C
C. A中含少量C时可用降温结晶法提纯A
D. 25%的A溶液降温至t1℃时会有晶体析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质的叙述一定不正确的是
A. 向FeCl2溶液中滴加NH4SCN溶液,溶液显红色
B. KAl(SO4) 2·12H2O溶于水可形成 Al(OH)3胶体
C. NH4Cl与Ca(OH)2混合加热可生成NH3
D. Cu与FeCl3溶液反应可生成CuCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 2 mol·L1KCl溶液与1 mol·L1 K2SO4溶液等体积混合后,c(K+)为2 mol·L1
B. 120 g NaCl溶液中溶有20 g NaCl,该温度下NaCl的溶解度为20 g
C. 50 mL 1 mol·L1 NaCl溶液与100 mL 0.5 mol·L1 NaCl溶液中所含的Cl物质的量浓度相同
D. 把5 g胆矾(CuSO4·5H2O)溶于45 g水中,所得溶液溶质的质量分数为10%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用王水(浓硝酸和浓盐酸按体积比1:3的混合物)来溶解白金等贵金属进行科学实验。王教授用质量分数为63%的浓硝酸(密度1.40g/ ![]() )和质量分数为36.5%的浓盐酸(密度1.19g/
)和质量分数为36.5%的浓盐酸(密度1.19g/ ![]() )来配制王水600毫升,假设忽略两种酸混合时的体积变化也不考虑混合后的化学变化,下列说法错误的是
)来配制王水600毫升,假设忽略两种酸混合时的体积变化也不考虑混合后的化学变化,下列说法错误的是
A. 该王水中硝酸的物质的量浓度是3.5mol/L
B. 该王水中氧元素的质量是100.8g
C. 该王水的密度约为1.24g/ ![]()
D. 该王水中HCl的质量分数约为26.2%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烷、烯、炔都是常见的碳氢化合物。
(1)写出下列有机物的系统命名法名称:
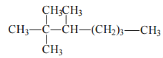 名称是______________________________
名称是______________________________
(2)有下列有机物:①CH3CH3②CH2=CH2③CH3-CH2-C≡CH④CH3-C≡C-CH3⑤C2H6⑥CH3-CH=CH2,其中互为同系物的是__________,互为同分异构体的是_________(填编号)
(3)实验室常用浓硫酸和乙醇混合加热制取乙烯。
①实验室制乙烯的化学方程式为_____________________________________。
②关于该实验的说法中正确的是(________)
a.浓硫酸只有催化剂的作用 b.可用向下排空气法收集乙烯
c.在反应容器中放入几片碎瓷片防止混合液暴沸 d.温度计应插入反应溶液液面下,以便控制温度
③实验后期制得的乙烯气体中常含有杂质气体![]() 和
和![]() ,将此混合气体直接通入溴水中,若观察到溴水褪色,能否证明乙烯发生了加成反应?__________(填“能”或“否”),原因是_________________________________________________________。
,将此混合气体直接通入溴水中,若观察到溴水褪色,能否证明乙烯发生了加成反应?__________(填“能”或“否”),原因是_________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学小组实验探究KI和FeCl3生成KCl、I2和FeCl2的反应存在一定限度。
实验:i.向5mL0.1mol/L KI溶液中滴加5~6滴0.1mol/L FeCl3溶液。充分反应后,将所得溶液分成甲、乙、丙三等份;
ⅱ.向甲中滴加CCl4,充分振荡;
ⅲ.向乙中滴加试剂X。
(1)将KI和FeCl3反应的离子方程式补充完整。_____I-+___Fe3+![]() ______I2+_______Fe2+
______I2+_______Fe2+
(2)步骤ⅲ中,试剂X是_____________。
(3)步骤ⅱ和ⅲ的实验现象中,能说明①中反应存在一定限度的实验现象是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com