
【题目】以氧化铝为原料,通过碳热还原法可合成氮化铝(AlN);通过电解法可制取铝。电解铝时阳极产生的CO2可通过二氧化碳甲烷化再利用。
请回答:
(1)已知:2Al2O3(s)===4Al(g)+3O2(g) ΔH1=3 351 kJ·mol-1
2C(s)+O2(g)===2CO(g) ΔH2=-221 kJ·mol-1
2Al(g)+N2(g)===2AlN(s) ΔH3=-318 kJ·mol-1
碳热还原Al2O3合成AlN的总热化学方程式是________________________,
该反应自发进行的条件________。
(2)在常压、Ru/TiO2催化下,CO2和H2混合气体(体积比1∶4,总物质的量a mol)进行反应,测得CO2转化率、CH4和CO选择性随温度变化情况分别如图1和图2所示(选择性:转化的CO2中生成CH4或CO的百分比)。
反应Ⅰ CO2(g)+4H2(g)![]() CH4(g)+2H2O(g) ΔH4
CH4(g)+2H2O(g) ΔH4
反应Ⅱ CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH5
CO(g)+H2O(g) ΔH5
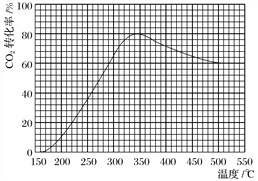
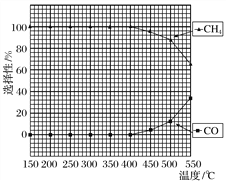
图1 图2
①下列说法不正确的是________。
A.ΔH4小于零
B.温度可影响产物的选择性
C.CO2平衡转化率随温度升高先增大后减少
D.其他条件不变,将CO2和H2的初始体积比改变为1∶3,可提高CO2平衡转化率
②350 ℃时,反应Ⅰ在t1时刻达到平衡,平衡时容器体积为V L,该温度下反应Ⅰ的平衡常数为________(用a、V表示)。
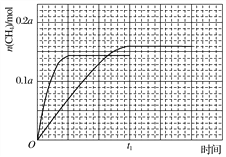
③350 ℃下CH4物质的量随时间的变化曲线如图3所示。画出400 ℃下0~t1时刻CH4物质的量随时间的变化曲线。__________________________
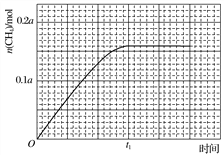
图3
(3)据文献报道,CO2可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是______。
【答案】 Al2O3(s)+3C(s)+N2(g)===2AlN(s)+3CO(g) ΔH=1026 kJ·mol-1 高温 CD ![]()
 CO2+6H2O+8e-===CH4+8OH-
CO2+6H2O+8e-===CH4+8OH-
【解析】(1)①2Al2O3(s)═4Al(g)+3O2(g)△H1=3351KJmol-1,②2C(s)+O2(g)═2CO(g)△H2=-221KJmol-1,③2Al(g)+N2(g)═2AlN(s)△H3=-318KJmol-1,盖斯定律计算,(①+②×3+③×2)×![]() 得到,碳热还原Al2O3合成AlN的总热化学方程式:3C(s)+Al2O3(s)+N2(g)=2AlN(s)+3CO(g)△H=+1026KJ/mol/L,反应△S>0,△H>0,则满足△H-T△S<0,反应自发进行的条件是高温条件下,故答案为:3C(s)+Al2O3(s)+N2(g)=2AlN(s)+3CO(g)△H=+1026KJ/mol/L;高温;
得到,碳热还原Al2O3合成AlN的总热化学方程式:3C(s)+Al2O3(s)+N2(g)=2AlN(s)+3CO(g)△H=+1026KJ/mol/L,反应△S>0,△H>0,则满足△H-T△S<0,反应自发进行的条件是高温条件下,故答案为:3C(s)+Al2O3(s)+N2(g)=2AlN(s)+3CO(g)△H=+1026KJ/mol/L;高温;
(2)①A.图象中,二氧化碳先增大是反应正向进行,到一定温度达到平衡状态,升温平衡逆向进行,二氧化碳转化率随温度升高减小,平衡说明正反应为放热反应,△H4小于零,故A正确;B.图象2分析可知,图象变化趋势随温度升高到400°C以上,CH4和CO选择性受温度影响甲烷减小,一氧化碳增大,温度可影响产物的选择性,故B正确;C.二氧化碳转化率先增大是反应正向进行未达到平衡状态,达到平衡状态,随温度升高二氧化碳转化率减小,故C错误;D.CO2和H2混和气体(体积比1:4,总物质的量a mol)进行反应,将CO2和H2的初始体积比改变为1:3,二氧化碳转化率减小,故D错误;故答案为:CD;
②在常压、Ru/TiO2催化下,CO2和H2混和气体(体积比1:4,总物质的量amol)进行反应,350℃时,反应Ⅰ在t1时刻达到平衡,平衡时容器体积为VL,二氧化碳转化率为80%
CO2(g)+4H2(g) ![]() CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
起始量(mol)0.2a0.8a 0 0
变化量(mol)0.16a0.64a 0.16a0.32a
平衡量(mol)0.04a0.16a 0.16a0.32a
平衡常数K=[![]() ×(
×(![]() )2]÷[
)2]÷[![]() ×(
×(![]() )4]=
)4]=![]() ,故答案为:
,故答案为:![]() ;
;
③反应为放热反应,升温平衡逆向进行,二氧化碳转化率减小,图中分析可知接近72.5%,甲烷物质的量减小小于350°C时甲烷物质的量,达到平衡所需要时间缩短
CO2(g)+4H2(g) ![]() CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
起始量(mol)0.2a0.8a 0 0
变化量(mol)0.145a0.58a0.145a0.29a
平衡量(mol)0.0550.22a0.145a 0.29a
画出图象,达到平衡状态甲烷 0.145amol,升温加快反应速率,达到平衡所需时间缩短,得到图象为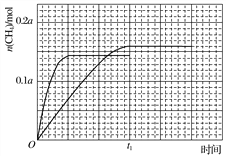 ,故答案为:
,故答案为: ;
;
(3)CO2可以在碱性水溶液中电解生成甲烷,结合电荷守恒和原子守恒,用氢氧根离子浓度配平电荷守恒得到电极反应为:CO2+6H2O+8e-═CH4+8OH-,故答案为:CO2+6H2O+8e-═CH4+8OH-。


 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】PH3是一种无色剧毒气体,其分子结构和NH3相似,但P—H键键能比N—H键键能低。下列判断错误的是
A. PH3沸点低于NH3沸点,因为P—H键键能低
B. PH3分子是极性分子
C. 一个PH3分子中,P原子核外有一个孤电子对
D. PH3分子稳定性低于NH3分子,因为N—H键键能高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是教师在课堂中演示的两个实验装置(铁架台等辅助仪器略去)

请回答下列问题
(1)实验一的实验目的是 _____________________________________ , 实验过程中可以观察到烧杯中的现象是_______________________________________________________ ,加热后试管中发生反应的化学方程式是: ____________________________
(2)实验二用来验证Na2O2与CO2的反应,观察到的实验现象是:包有Na2O2的棉花燃烧。Na2O2与CO2的反应的化学方程式________________________________________ ,该实验可以得出许多结论,请你写出由该实验得出的两个结论。
结论1:__________________________________
结论2:__________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
苯酚是一种重要的化工原料,以苯酚为主要起始原料,经下列反应可制得香料M 和高分子化合物N(部分产物及反应条件已略去):
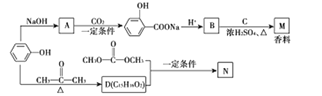
已知化合物N为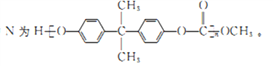
回答下列问题:
(1)B的结构简式为________________,B中能与NaHCO3反应的官能团名称是_______________。
(2)已知C的分子式为C5H12O,C能与金属Na反应,C的核磁共抓氢谱有3组峰,峰面积比值是9: 2:1,则M的结构简式为_________________。
(3)由苯酚生成D的化学方程式为______________________。
(4)化合物D与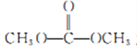 发生反应,除生成化合物N 外,还生成_____________(写结构简式)。 (5)F是相对分子质量比B大14的同系物,F有多种同分异构体,符合下列条件的F的同分异构体有_____种。①属于芳香族化合物 ②遇FeCl3 溶液显紫色,且能发生水解反应
发生反应,除生成化合物N 外,还生成_____________(写结构简式)。 (5)F是相对分子质量比B大14的同系物,F有多种同分异构体,符合下列条件的F的同分异构体有_____种。①属于芳香族化合物 ②遇FeCl3 溶液显紫色,且能发生水解反应
③苯环上有两个取代基
(6)已知: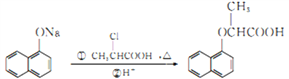 ,写出用苯酚、乙醇和ClCH2COOH为原料制备化合物
,写出用苯酚、乙醇和ClCH2COOH为原料制备化合物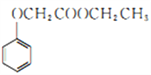 的合成路线_________________(其他试剂任选)。
的合成路线_________________(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水得到的粗食盐水中常含Ca2+、Mg2+、SO42-,需要分离提纯。现有含少量CaCl2、MgSO4的粗食盐水,在除去悬浮物和泥沙之后,要用4种试剂:①盐酸、②Na2CO3、③NaOH、④BaCl2来除去食盐水中的Ca2+、Mg2+、SO42-。提纯时的操作步骤和加入试剂的情况如图。

图中a、b、c、d分别表示上述4种试剂中的一种,请回答:
(1)沉淀A的名称是________。
(2)试剂d是________;判断试剂d已经足量的方法是__________________________。
(3)加入b、c后溶液中发生的化学反应的化学方程式有______________________(任写两个)。
(4)现有下列仪器,过滤出沉淀A、B、C时必须用到的是____(填序号),仪器③的名称是_______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用98%的浓硫酸(密度为1.84g/cm3)配制l00mL 1mol/L的稀硫酸,现绐出下列仪器(配制过程中可能用到):①100mL量筒②10mL量筒③50mL烧杯 ④托盘天平⑤100mL容量瓶⑥胶头滴管⑦玻璃棒,配制中使用仪器的先后順序排列正确的是
A. ④③⑦⑤⑥ B. ②⑤⑦⑥ C. ①③⑤⑥⑦ D. ②⑥③⑦⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列金属的冶炼方法正确的是( )
A.电解氯化钠溶液冶炼金属钠
B.电解熔融的氯化铝冶炼金属铝
C.将铁粉与氧化镁混合加热冶炼镁
D.用一氧化碳还原氧化铁冶炼铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列方程式(注明反应条件),每个方程式2分,共10分
(1)乙醇催化氧化反应:_____________________________________________;
(2)实验室制乙炔的化学反应方程式: _____________________________________________;
(3)苯酚钠溶液通入少量的二氧化碳气体的化学反应方程式: __________________________;
(4)溴乙烷与氢氧化钠水溶液的化学反应方程式: ______________________________;
(5)苯甲醛水溶液与新制的氢氧化铜悬浊液化学反应的方程式:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硒(Se)是人体健康必需的一种微量元素。已知Se的原子结构示意图为: 下列说法不正确的是
下列说法不正确的是
A. 该原子的质量数为34 B. 该元素处于第四周期第ⅥA族
C. SeO2既有氧化性又有还原性 D. 酸性:HBrO4 > H2SeO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com