
【题目】现有六种元素,其中A、B、C、D、E为短周期主要族元素,F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
A元素形成的物质种类繁多,其形成的一种固体单质工业上常用作切割工具 |
B元素原子的核外p电子数比s电子数少1 |
C元素基态原子p轨道有两个未成对电子 |
D原子的第一至第四电离能分别是: Ⅰ1=738kJ·mol-1;Ⅰ2=1451kJ·mol-1;Ⅰ3=7733kJ·mol-1;Ⅰ4=10540kJ·mol-1; |
E原子核外所有p轨道全满或半满 |
F在周期表的第8纵列 |
(1)某同学根据上述信息,推断A基态原子的核外最子排布为了![]() ,该同学所画的电子排布图违背了___________。
,该同学所画的电子排布图违背了___________。
(2)B元素的电负性_____(填“大于”、“小于”或“等于”)C元素的电负性。
(3)C与D形成的化合物所含有的化学键类型为_____________。
(4)E基态原子中能量最高的电子,其电子云在空间有__________个方向。
(5)下列关于F原子的价层电子排布图正确的是___________。
a.![]() b.
b.![]()
c.![]() d.
d.![]()
(6)基态F3+离子核外电子排布式为_____________。过量单质F与B的最高价氧化物的水化物的稀溶液完全反应,生成BC气体,该反应的离子方程式为____________。
(7)元素铜与镍的第二电离能分别为:ICu=1959kJ·mol-1,INi=1753kJ·mol-1,ICu>INi原因是__________________。
【答案】 洪特规则 小于 离子键 3 c [Ar]3d5或 1s22s22p63s23p63d5 3Fe+8H++2NO3-=3Fe2++2NO↑ +4H2O Cu+核外价电子排布为3d10,3d全充满,比Ni+的3d84s1稳定,难以失去电子
【解析】(1) A基态原子的核外最子排布为了![]() ,该同学所画的电子排布图违背了洪特规则。
,该同学所画的电子排布图违背了洪特规则。
(2)B元素元素原子的核外p电子数比s电子数少1知B为N, C元素基态原子p轨道有两个未成对电子知C为O, N的电负性小于O,所以B元素的电负性小于C元素的电负性,答案:小于。
(3)根据电离能知D为镁,C与D形成的化合物所为离子化合物,其化学键类型为离子键。答案:离子键。
(4)E原子核外所有p轨道全满或半满知P 为磷。E基态原子中能量最高的电子,其电子云在空间有3个方向。
(5)F为第四周期元素且在周期表的第8纵列知F为铁元素,F原子的价层电子排布图.![]() ,答案:c。
,答案:c。
(6)基态F3+离子即为Fe3+核外电子排布式为: 1s22s22p63s23p63d5.答案:1s22s22p63s23p63d5。
过量单质为铁与B的最高价氧化物的水化物为硝酸的稀溶液完全反应,生成BC气体,该反应的离子方程式为:3Fe+8H++2NO3-=3Fe2++2NO↑ +4H2O。
(7)元素铜与镍的第二电离能分别为:ICu=1959kJ·mol-1,INi=1753kJ·mol-1,ICu>INi原因是
. Cu+核外价电子排布为3d10,3d全充满,比Ni+的3d84s1稳定,难以失去电子。


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:高中化学 来源: 题型:
【题目】25℃时,0.01 mol·L-1两种弱酸溶液的pH如表,下列说法正确的是

A.相同pH的两种酸溶液中,CH3COOH溶液中水电离的c(H+)较大
B.物质的量浓度相同的CH3COONa与NaCN 溶液中,CH3COONa溶液pH较大
C.等体积pH相同的两种酸溶液,分别滴加NaOH溶液至恰好中和,消耗等量的NaOH
D.HCN的电离平衡常数(Ka)与CN—的水解平衡常数(K)存在如下关系:KaK=Kw
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.氧化还原反应的本质是元素化合价的升降
B.氯化钠溶液在电流的作用下电离产生Na+、Cl-
C.发生氧化反应的物质也可能同时发生还原反应
D.氧化反应一定先于还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氧化二镍是一种重要的电子元件材料、蓄电池材料。工业上利用含镍废料(以镍、铁、钙、镁合金为主)制取草酸镍(NiC2O4·2H2O),再高温煅烧草酸镍制取三氧化二镍。已知草酸的钙、镁、镍盐均难溶于水。根据下列工艺流程示意图回答问题。
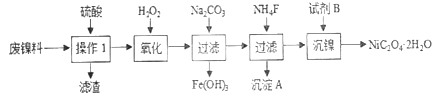
(1)操作1的名称为__________。
(2)保持其他条件相同,在不同温度下对废镍料进行“酸浸”,镍浸出率随时间变化如图。“酸浸”的适宜温度与时间分别为_______(填字母)。
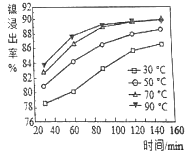
a.30℃、30min b.70℃、120min
c.90℃、150min d.90℃、120min
(3)沉淀A为CaF2和_________(填化学式)。
(4)试剂B的化学式为_________________。
(5)NiC2O4·2H2O样品经某稀酸酸化处理后,用稀KMnO4标准溶液滴定[在本实验条件下,Ni(Ⅱ)不能被氧化,其他物质不参与反应],通过测定草酸的量可测定NiC2O4·2H2O样品的纯度,滴定反应为:2MnO4-+6H++5H2C2O4=2Mn2++10CO2↑+8H2O。实验中称取0.183g样品,滴定时消耗了0.0400mol.L-1的KMnO4溶液8.00mL,则该样品中NiC2O4·2H2O的质量分数为_________。
(6)高温煅烧草酸镍制取三氧化二镍时会产生CO、CO2、水蒸气等混合气体。某同学设计如下实验流程进行检验。
混合气体![]() 现象
现象![]() 现象
现象![]()
![]() 现象
现象![]() 现象
现象
①试剂1的名称为____________。
②证明混合气体有CO的现象是_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验过程中产生的现象与图形相符合的是( )
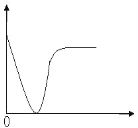
A. 稀硫酸滴加到 B a ( O H ) 2 溶液中(横坐标是稀硫酸的体积,纵坐标为溶液的导电能力)
B. 铁粉加到一定量 CuSO4 溶液中(横坐标是铁粉的质量,纵坐标为沉淀质量)
C. CO2 通入一定量 NaOH 溶液中(横坐标是 CO2 的体积,纵坐标为溶液的导电能力)
D. 稀盐酸滴加到一定量 NaOH 溶液中(横坐标是稀盐酸的体积,纵坐标为钠离子物质的量)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列四种有机物的有关说法正确的是
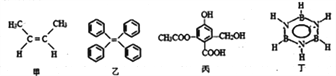
A. 甲的名称为反-2-丁烯
B. 乙中所有碳原子一定处于同一平面
C. 1mol丙分别与足量Na、NaOH、NaHCO3反应,消耗这三种物质分别是3mol、4mol、1mol
D. 丁的二氯代物有3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.棉花、油脂、ABS树脂都是由高分子化合物组成的物质
B.开发核能、太阳能等新能源,推广甲醇汽油,使用无磷洗涤剂都可直接降低碳排放
C.体型高分子是由高分子链间形成的化学键交联而成的空间网状结构
D.酚醛树脂与涤纶都是热固性高分子材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向等物质的量浓度的NaC1、MgCl2、AlC13三种溶液中,加入足量的AgNO3溶液,产生的沉淀的质量比为3:2:1,则NaC1、MgCl2、AlC13三种溶液体积比为( )
A.9:3:1B.6:3:2C.3:2:1D.1:1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25 ℃、101 kPa条件下,将15 L O2通入10 L CO和H2的混合气体中,使其完全燃烧,干燥后,恢复至原来的温度和压强。
(1)若剩余气体的体积是15 L,则原CO和H2的混合气体中V(CO)=________ L,V(H2)=________ L。
(2)若剩余气体的体积为a L,则原CO和H2的混合气体中V(CO)∶V(H2)=________。
(3)若剩余气体的体积为a L,则a的取值范围是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com