
【题目】硼镁泥是一种工业废料,主要成分是MgO(MgO占40%,还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质),以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4·7H2O的流程如下:
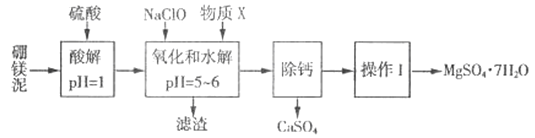
根据题意回答下列问题:
(1)实验中需用1mol/L的硫酸800 mL,若用18.4 mol/L的浓硫酸来配制,则量取浓硫酸时,需使用的量筒规格为_______。(填字母)
A.10 mL B.25 mL C.50 mL D.100 mL
(2)加入的NaClO 可与酸解液中Mn2+ 反应:Mn2+ + ClO-+H2O= MnO2 ↓+ 2H+ + Cl-,溶液中还有一种离子也会被NaClO氧化,该反应的离子方程式为___________。该步骤中,物质X是________(填化学式)。
(3)“滤渣”中除MnO2、CaSO4 外还有_______。(填化学式)
(4)已知MgSO4、CaSO4的溶解度如下表:
温度/℃ | 40 | 50 | 60 | 70 | |
溶解度/g | MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 | |
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明操作步骤:____________。
(5)“操作I”是将滤液经过一系列操作后真空干燥,采用“真空干燥”的原因是________。
(6)实验中提供的硼镁泥共100g,得到的MgSO4·7H2O 为147.6 g,则MgSO4·7H2O的产率为________%。
【答案】 D 2Fe2++ClO-+2H+=2Fe3++Cl-+H2O MgO[或MgCO3或Mg(OH)2或其他合理答案] Fe(OH)3、Al(OH)3、SiO2 蒸发浓缩、趁热过滤 减小压强,降低水的沸点,避免干燥溫度过高而使晶体失去结晶水 60(答60%不给分)
【解析】(1)稀释前后溶质的物质的量不变,1mol/L×800ml=18.4mol/L×V(浓硫酸),V(浓硫酸)=43.5ml,故选择的量筒的规格应为100ml,答案选D。
(2)FeO溶于酸中生成有还原性的Fe2+,能与ClO-发生氧化还原反应,离子方程式为:2Fe2++ClO-+2H+=2Fe3++Cl-+H2O;氧化和水解步骤中加入X的目的是将Fe3+和Al3+转化为沉淀,故可加入. MgO[或MgCO3或Mg(OH)2等不溶物,中和酸性,促进Fe3+ 和Al3+的水解正向进行生成沉淀而除去,故X为MgO[或MgCO3或Mg(OH)2或其他合理答案]。
(3)CaSO4微溶于水,Mn2+转化为MnO2,SiO2不溶于水,Fe3+和Al3+完全水解得到Fe(OH)3和Al(OH)3沉淀,故滤渣中除MnO2、CaSO4外还有:SiO2、Fe(OH)3、Al(OH)3。
(4) MgSO4的溶解度随温度的升高而增大,CaSO4的溶解度随温度的升高而降低,将MgSO4和CaSO4混合溶液加热蒸发浓缩,CaSO4近乎沉淀完,然后在较高温度下过滤而除去CaSO4,在较高温度下过滤可以防止温度降低时CaSO4溶解度增大,故答案为:蒸发浓缩,趁热过滤。
(5)压强低液体的沸点就低,降低压强,可以降低水的沸点,从而可以在较低的温度下干燥晶体,避免温度高而使晶体失去部分结晶水。
(6)Mg2+的物质的量为100g×40%÷40g·mol-1=1mol,所以理论上MgSO4·7H2O的质量为1mol×246g/mol=246g,故MgSO4·7H2O的产率为147.6g÷246g×100%=60%。


 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案科目:高中化学 来源: 题型:
【题目】某化学兴趣小组要完成中和热的测定.回答下列问题:
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5molL﹣1盐酸、0.55molL﹣1NaOH溶液,实验尚缺少的玻璃用品是 .
(2)已知:反应后溶液的比热容c为4.18J℃﹣1g﹣1 , 0.5molL﹣1盐酸和0.55molL﹣1NaOH溶液的密度均为1gcm﹣3 . 实验时记录的实验数据如表:
实验 | 反应物及用量 | 溶 液 温 度 | ||
t1 | t2 | |||
1 | 50mL0.55molL﹣1NaOH溶液 | 50mL.0.5molL﹣1HCl溶液 | 20℃ | 23.3℃ |
2 | 50mL0.55molL﹣1NaOH溶液 | 50mL.0.5molL﹣1HCl溶液 | 20℃ | 23.5℃ |
①盐酸和氢氧化钠反应的中和热△H1=(保留两位小数)
②已知:CH3COOH(aq)CH3COO﹣(aq)+H+(aq)△H2>0,
CH3COOH(aq)+OH﹣(aq)=CH3COO﹣(aq)+H20(l)△H3 则△H3△H1(填“>”、“<”、“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有通电条件下,用如图所示装置由乙二醛(OHC-CHO)制备乙二酸(HOOC-COOH),其反应为:OHC-CHO+2Cl2+2H2O![]() HOOC-COOH+4HCl。下列说法正确的是
HOOC-COOH+4HCl。下列说法正确的是
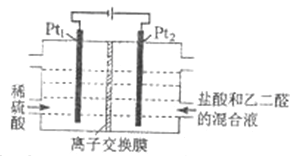
A. Pt1的电极反应为:2H2O+ 2e-=2OH-+H2↑
B. 盐酸起提供Cl- 和增强导电性的作用
C. 每消耗0.1mol乙二醛,在Pt1极放出2.24 L 气体(标准状况)
D. 每得到1mol乙二酸将有2 mol H+从右室迁移到左室
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】莽草酸可用于合成药物达菲,其结构简式如下图。下列关于莽草酸的说法正确的是
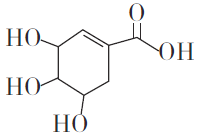
A. 分子式为C7H6O5
B. 可发生加成和取代反应
C. 分子中含有两种官能团
D. 1mol莽草酸与足量的Na反应,生成标准状况下33.6L的H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】辣椒素是辣椒的活性成分,可在口腔中产生灼烧感,能够起到降血压和胆固醇的功效,进而在很大程
度上预防心脏病,也能缀解肌肉关节疼痛。辣椒素酯类化合物的结构可以表示为:
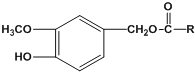
其中一种辣椒素脂类化合物J的合成路线如下:
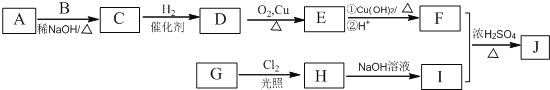
已知:①A、B和E为同系物,其中B的相对分子质量为44,A和B核磁共振氢谱显示都有两组峰
②J的分子式为C15H22O4
③![]()
回答下列问题:
(1)G所含官能团的名称为_______________________。
(2)由A和B生成C的化学方程式为___________________。
(3)由C生成D的反应类型为____________,D的化学名称为________________。
(4)由H生成I的化学方程式为_______________________。
(5)在G的同分异构体中,苯环上的一氯代物只有种的共有_____种(不含立体异构),其中核磁共振氢谱显示两组峰的是__________(写结构简式)。
(6)参照上述路线,设计一条以乙醛为原料(无机试剂任选)合成乙酸正丁酯的路线:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随原子序数的递增,七种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。

根据判断出的元素回答:
(1)x在元索周期表的位置是________________________。
(2)y的最高价氧化物对应的水化物与其氢化物反应,产物中含有化学键的类型为________________。
(3)d的单质在空气中充分燃烧,所得产物的电子式为________;7.8g该产物与足量的水完全反应,转移电子的数目为____________________。
(4)z、e、f的简单离子半径由大到小的顺序为_______________(用离子符号表示)。
(5)能说明g的非金属性比f强的实验事实是________________(列举一条)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镓(Ga)被誉为第三代半导体的明屋元素,广泛应用于电子工业。Ga位于周期表的第四周期,与A1同主族,主要存在Ga3+、GaO2-两种离子形态。
(1)请画出Ga的原子结构示意图___________。
(2)请写出Ga2O3溶解在NaOH溶液中的离子方程式_________________。
(3)氮化镓(GaN)可用于制作蓝色LED光源。GaN的传统工艺是用GaCl3与NH3反应来制备,新工艺则采用金属Ga与NH3在一定条件下来合成。已知:
①GaCl3(s)+NH3(g)=GaN(s)+3HCl(g) H1=+180kJ/mol
②2Ga(s)+6HCl(g)=2GaCl3(s)+3H2(g)H2=-492kJ/mol
③Ga(s)+NH3(g)=GaN(s)+3/2H2(g) H3
由上述反应可知H3=_____________。
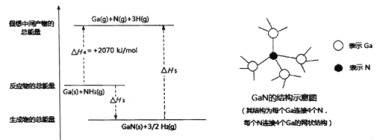
已知H-H的键能为436kJ/mol,结合上图分析,1molGaN含有_____molGa-N键,拆开lmolGa-N键所需能量为______kJ。
(4)工业上多用电解精炼法提纯镓。具体原理如下图所示:
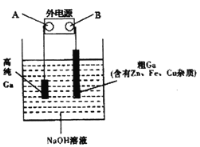
已知:金属的活动性Zn>Ga>Fe>Cu
①A为电源的_____极,电解精炼镓时产生阳极泥的主要成分是___________。
②电解过程中阳极产生的离子迁移到达阴极并在阴极放电析出高纯镓。请写出电解过程的阴极的电极反应_______________。
③电解过程中需控制合适的电压,若电压太高时阴极会产生H2导致电解效率下降。若外电路通过0.4mole-时,阴极得到7.0g的镓。则该电解装置的电解效率η=___________。(η=生成目标产物消耗的电子数÷转移的电子总数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com