
【题目】一种合成囧烷(E)的路线如下:
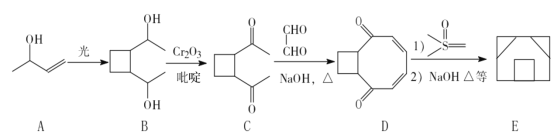
⑴ A中所含官能团的名称是_______________;E的分子式为_________。
⑵ A→B、B→C的反应类型分别是___________、___________。
⑶ 在一定条件下,B与足量乙酸可发生酯化反应,其化学方程式为______________。
⑷ F是一种芳香族化合物,能同时满足下列条件的F的同分异构体有_____种。
① 1个F分子比1个C分子少两个氢原子
② 苯环上有3个取代基
③ 1molF能与2molNaOH反应
写出其中核磁共振氢谱图有5组峰,且面积比为3∶2∶2∶2∶1的一种物质的结构简式:__________。
⑸ 1,2-环己二醇( 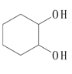 )是一种重要的有机合成原料,请参照题中的合成路线,以
)是一种重要的有机合成原料,请参照题中的合成路线,以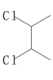 和
和![]() 为主要原料,设计合成1,2-环己二醇的合成路线。______________
为主要原料,设计合成1,2-环己二醇的合成路线。______________
【答案】羟基、碳碳双键 C12H18 加成反应 氧化反应  +2CH3COOH
+2CH3COOH![]()
 +2H2O 6
+2H2O 6  或
或
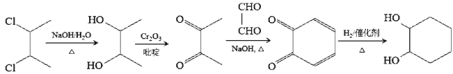
【解析】
⑴ 根据A(![]() )的结构结合常见官能团的结构判断;根据E(
)的结构结合常见官能团的结构判断;根据E(![]() )确定其分子式;
)确定其分子式;
(2)对比A、B结构,2个A分子中碳碳双键中一个键断裂,碳原子相互连接成环得到B;B中羟基转化为C中羰基,据此判断反应类型;
⑶ B中含有羟基,在一定条件下,能够与乙酸发生酯化反应,结合酯化反应的机理书写与乙酸反应的方程式;
⑷ C为 ,分子式为C8H12O2,1个F分子比1个C分子少两个氢原子,则F的分子式为C8H10O2,其不饱和度=4,F是一种芳香族化合物,说明除了苯环外,不存在不饱和结构,1molF能与2molNaOH反应,并且苯环上有3个取代基,说明苯环上含有2个羟基和1个乙基,据此书写满足条件的同分异构体;
,分子式为C8H12O2,1个F分子比1个C分子少两个氢原子,则F的分子式为C8H10O2,其不饱和度=4,F是一种芳香族化合物,说明除了苯环外,不存在不饱和结构,1molF能与2molNaOH反应,并且苯环上有3个取代基,说明苯环上含有2个羟基和1个乙基,据此书写满足条件的同分异构体;
⑸以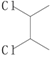 和
和![]() 为主要原料合成1,2-环己二醇(
为主要原料合成1,2-环己二醇( ![]() ),根据题干流程图C→D的提示,需要合成
),根据题干流程图C→D的提示,需要合成![]() ,再由
,再由![]() 与乙二醛反应生成
与乙二醛反应生成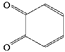 ,最后将
,最后将 转化为
转化为![]() 即可。
即可。
⑴ A(![]() )中所含官能团有羟基和碳碳双键;E(
)中所含官能团有羟基和碳碳双键;E(![]() )的分子式为C12H18,故答案为:羟基、碳碳双键;C12H18;
)的分子式为C12H18,故答案为:羟基、碳碳双键;C12H18;
(2)对比A、B结构,2个A分子中碳碳双键中一个键断裂,碳原子相互连接成环得到B,属于加成反应;B中羟基转化为C中羰基,发生氧化反应,故答案为:加成反应;氧化反应;
⑶ B中含有羟基,在一定条件下,能够与乙酸发生酯化反应,反应的化学方程式为 +2CH3COOH
+2CH3COOH![]()
 +2H2O,故答案为:
+2H2O,故答案为: +2CH3COOH
+2CH3COOH![]()
 +2H2O;
+2H2O;
⑷ C为 ,分子式为C8H12O2,1个F分子比1个C分子少两个氢原子,则F的分子式为C8H10O2,不饱和度=
,分子式为C8H12O2,1个F分子比1个C分子少两个氢原子,则F的分子式为C8H10O2,不饱和度=![]() =4,F是一种芳香族化合物,说明除了苯环外,不存在不饱和结构,1molF能与2molNaOH反应,并且苯环上有3个取代基,说明苯环上含有2个羟基和1个乙基,满足条件的同分异构体有6种(羟基位于邻位的2种,羟基位于间位的3种,羟基位于对位的1种);其中核磁共振氢谱图有5组峰,且面积比为3∶2∶2∶2∶1的结构简式为
=4,F是一种芳香族化合物,说明除了苯环外,不存在不饱和结构,1molF能与2molNaOH反应,并且苯环上有3个取代基,说明苯环上含有2个羟基和1个乙基,满足条件的同分异构体有6种(羟基位于邻位的2种,羟基位于间位的3种,羟基位于对位的1种);其中核磁共振氢谱图有5组峰,且面积比为3∶2∶2∶2∶1的结构简式为 或
或 ,故答案为:6;
,故答案为:6; 或
或 ;
;
⑸以 和
和![]() 为主要原料合成1,2-环己二醇(
为主要原料合成1,2-环己二醇( ![]() ),根据题干流程图C→D的提示,可以首先由
),根据题干流程图C→D的提示,可以首先由 合成
合成![]() ,再由
,再由![]() 与乙二醛反应生成
与乙二醛反应生成 ,最后将
,最后将 转化为
转化为![]() 即可;其中由
即可;其中由 合成
合成![]() 可以将氯原子水解后氧化得到;将
可以将氯原子水解后氧化得到;将 转化为
转化为![]() 只需要与氢气加成得到,因此合成路线为
只需要与氢气加成得到,因此合成路线为 ,故答案为:
,故答案为: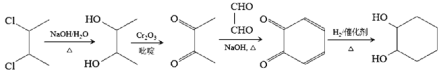 。
。


科目:高中化学 来源: 题型:
【题目】锑(Sb)广泛用于生产各种阻燃剂、陶瓷、半导体元件和医药及化工等领域。
Ⅰ.(1)锑在元素周期表中的位置_____。
(2)锑(Ⅲ)的氧化物被称为锑白,可以由SbCl3水解制得,已知SbCl3水解的最终产物为锑白。为了得到较多、较纯的锑白,操作时将SbCl3徐徐加入大量水中,反应后期还要加入少量氨水。试用必要的化学用语和平衡移动原理解释这两项操作的作用_______。工业上,还可用火法制取锑白,是将辉锑矿(主要成分为Sb2S3)装入氧化炉的坩埚中,高温使其融化后通入空气,充分反应后,经冷却生成锑白。写出火法制取锑白的化学方程式______。
Ⅱ.以辉锑矿为原料制备金属锑,其中一种工艺流程如下:
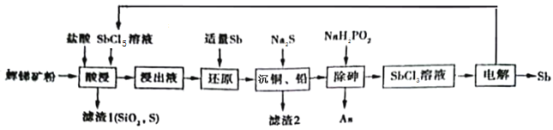
已知部分信息如下:
①辉锑矿(除Sb2S3外,还含有砷、铅、铜的化合物和SiO2等);
②浸出液主要含盐酸和SbCl3,还含SbCl5、CuCl2、AsCl3和PbCl2等杂质;
③常温下,Ksp(CuS)=1.0×10-36,Ksp(PbS)=9.0×10-29。
回答下列问题:
(3)“酸浸”过程中Sb2S3发生反应的化学方程式为_____。
(4)已知:浸出液中c(Cu2+)=0.0001mol/L,c( Pb2+)=0.1mol/L。在沉淀铜、铅过程中,缓慢滴加极稀的硫化钠溶液,先产生沉淀的是_____(填化学式);当CuS、PbS共沉沉时,![]() =______(保留小数点后一位)。
=______(保留小数点后一位)。
(5)在“除砷”过程中,氧化产物为H3PO4。该反应氧化产物与还原产物的物质的量之比为__________。
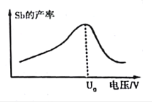
(6)在“电解”过程中,锑的产率与电压大小关系如图所示。当电压超过U0 V时,锑的产率降低的原因可能是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在研究金矿床物质组分的过程中,通过分析发现了Cu—Ni—Zn—Sn—Fe多金属互化物。
(1)某种金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该金属互化物属于________(填“晶体”或“非晶体”)
(2)基态Ni2+的核外电子排布式为________;Ni2+和Fe2+的半径分别为69 pm和78 pm,则熔点NiO______FeO(填“<”或“>”),其原因是_________________________________________。
(3)铜能与类卤素(SCN)2反应生成Cu(SCN)2,1 mol (SCN)2分子中含有σ键的数目为________;写出一种与SCN-互为等电子体的分子________(用化学式表示)。
(4)氨基乙酸铜的分子结构如图,碳原子的杂化方式为________。

(5)立方NiO(氧化镍)晶体的结构如图所示,其晶胞边长为a pm,列式表示NiO晶体的密度为________g·cm-3(不必计算出结果,阿伏加德罗常数的值为NA)。人工制备的NiO晶体中常存在缺陷(如图):一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代,其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化。已知某氧化镍样品组成Ni0.96O,该晶体中Ni3+与Ni2+的离子个数之比为________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如下能量关系示意图,下列说法正确的是
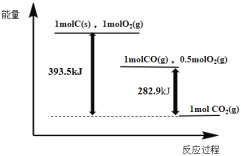
A.1 mol C(s)与1 mol O2(g)的能量之和为393.5 kJ
B.由C→CO的热化学方程式为:2C(s)+O2(g) = 2CO(g) ΔH= 221.2 kJmol1
C.反应2CO(g)+O2(g) =2CO2(g)中,生成物的总能量大于反应物的总能量
D.将1 mol C(s)磨成粉末后,反应更加剧烈,说明粉碎可以改变ΔH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚苯胺是一种在充放电过程中具有更优异可逆性的电极材料。Zn一聚苯胺二次电池的结构示意图如图所示,设NA为阿伏加德罗常数的值。下列说法错误的是( )
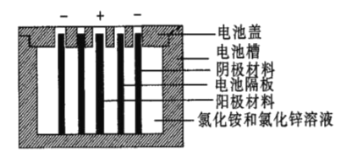
A.放电时,外电路每通过0.1NA个电子时,锌片的质量减少3.25g
B.充电时,聚苯胺电极的电势低于锌片的电势
C.放电时,混合液中的Cl-向负极移动
D.充电时,聚苯胺电极接电源的正极,发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以炼锌厂的烟道灰(主要成分为ZnO,另含少量Fe2O3、CuO、SiO2、MnO等)为原料可生产草酸锌晶体(ZnC2O42H2O)
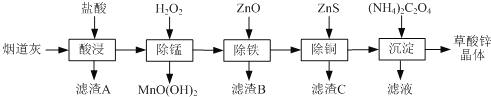
已知:常温下Ksp[Fe(OH)3]=2.6×10-39, Ksp[Cu(OH)2]=2.2×10-20。
请问答下列问题:
(1)为了提高“酸浸”时锌元素的浸出率,可以采取的措施有:_________、________(填写2条)。
(2)“除锰”反应后,溶液的pH__________(填“增大”“减小”或“不变”)。
(3)常温下“除铁”反应中,加入ZnCO3可调节溶液的pH,使得Fe3+和部分Cu2+被除去,当两种沉淀共存且溶液的pH=8时,c(Cu2+)/ c( Fe3+)=________________ 。
(4)“除铜”反应的离子方程式为________。
(5)若“沉淀”过程中采用Na2C2O4代替(NH4)2C2O4生产草酸锌晶体,应该在搅拌下,将Na2C2O4溶液缓慢加入ZnCl2溶液中,如果顺序颠倒,会产生的不良后果是__________。
(6)将草酸锌晶体加热分解可得到一种纳米材料。加热过程中固体残留率(剩余固体的质量/原始固体的质量×100%)随温度的变化如图所示,则A、B点固体的化学式分别为____、___________。
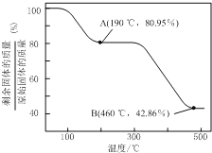
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为确定Na2CO3和NaHCO3混合物样品的组成,称取四份该样品溶于水后分别逐滴加入相同浓度盐酸30.0 mL,充分反应,产生CO2的体积(已折算成标准状况下的体积,不考虑CO2在水中的溶解)如下表:
实验序号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
盐酸体积(mL) | 30.0 | 30.0 | 30.0 | 30.0 |
样品质量(g) | 2.96 | 3.70 | 5.18 | 6.66 |
CO2体积(mL) | 672 | 840 | 896 | 672 |
(1)样品中的物质的量之比n(Na2CO3)∶n(NaHCO3)=________。
(2)盐酸的物质的量浓度c(HCl)=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取一支硬质大试管,通过排饱和食盐水的方法先后收集半试管甲烷和半试管氯气,并置于光亮处(如图),下列对于试管内发生的反应及现象的说法正确的是( )
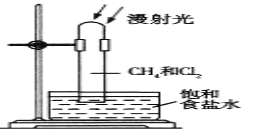
A. 反应过程中试管内黄绿色逐渐变浅,试管壁上有油珠产生
B. 将该装置放在黑暗处,![]() 与
与![]() 也能反应
也能反应
C. 该反应仅得到一种有机产物
D. ![]() 和
和![]() 完全反应后液面上升,液体充满试管
完全反应后液面上升,液体充满试管
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.石油裂解气可以使溴水褪色,也可以使高锰酸钾溶液褪色
B.可以用溴水检验乙烷中是否含有乙烯
C.1 mol 甲烷在光照条件下最多能与 2 mol Cl2发生取代反应
D.CH2=CHCH3+Cl2![]() CH2=CHCH2Cl+HCl属于取代反应
CH2=CHCH2Cl+HCl属于取代反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com