
【题目】通常检测SO2含量是否达到排放标准的反应原理是SO2 +H2O2 + BaCl2 ===BaSO4↓+ 2HCl。NA表示阿伏伽德罗常数,下列说法正确的是( )
A. 0.1 mol BaCl2晶体中所含微粒总数为0.1NA
B. 25 ℃时,pH =1的HCl溶液中含有H+的数目为0.1NA
C. 17 g H2O2中含有非极性键数目为0.5NA
D. 生成2.33 g BaSO4沉淀时,转移电子数目为0.01NA
 作业辅导系列答案
作业辅导系列答案科目:高中化学 来源: 题型:
【题目】已知 25℃时部分弱电解质的电离平衡常数数据如表:
化学式 | HSCN | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.3×10﹣1 | 1.8×10﹣5 | Ka1=4.3×10﹣1Ka2=5.6×10﹣1 | 3.0×10﹣8 |
回答下列问题:
(1)写出碳酸的主要的电离方程式 . 若将碳酸饱和溶液稀释 10 倍,则稀释后的溶液中 c(H+)原来的十分之一(填“大于”、“小于”或“等于”).
(2)物质的量浓度均为 0.1mol/L 的五种溶液:pH 由小到大的顺序为(用编号填写).
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3 e.NaSCN
(3)25℃时,将 20mL0.1molL﹣1CH COOH 溶液和 20mL0.1molL﹣1HSCN 溶液分别与 20mL0.1molL﹣1NaHCO 溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图.
反应初始阶段两种溶液产生 CO2气体的速率存在明显差异的原因是反应结束后,假设 NaHCO3完全反应且气体全部逸出,则所得两溶液中,c(CH3COO)c(SCN)(填“>”、“<”或“=”)
(4)25℃时,CH3COONa 与 CH3COOH 的混合溶液,若测得 pH=8,则溶液中c(Na+)﹣c(CH3COO﹣)=mol/L(填代入数据后的计算式,不必算出具体数值).
(5)向 NaClO 溶液中通入少量的 CO2 , 发生反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,A、D同主族,C与E同主族,D、E、F同周期,A、B的最外层电子数之和与C的最外层电子数相等, A能分别与B、C形成电子总数相等的分子,且A与C形成的化合物常温下为液态,A能分别与E、F形成电子总数相等的气体分子。请回答下列问题:
(1)F的元素符号为_________,E、F的简单离子中半径较大的是______(填离子符号)。
(2)A、C、D三种元素组成的一种常见化合物,是氯碱工业的重要产品,该化合物电子式为__________。
(3)B、C简单氢化物中稳定性较强的是__________(填分子式)。
(4)B与F两种元素形成的一种化合物分子,各原子均达8电子稳定结构,则该化合物的化学式为___________;B的简单氢化物与F的单质常温下可发生置换反应,请写出该反应的化学方程式:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】抗过敏药物H 可通过如下合成路线制备。

已知: ![]()
(1)A物质的名称为_______________,B中含氧官能团的名称为__________________。
(2)由B生成C的反应类型为________________,由E 生成F 的反应类型为_______________。
(3)下列试剂可用于鉴别![]() 和
和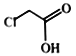 的有________(填标号)。
的有________(填标号)。
a.NaOH 溶液 b.小苏打溶液 c.AgNO3溶液 d.溴的CCl4溶液
(4)由D生成E的化学方程式为____________________________________。
(5)己知联苯由两个苯环通过单键连接而成(![]() ),分子中苯环间的单键可以自由旋转。则B的同分异构体中含联苯基团且能发生银镜反应的至少有____种。
),分子中苯环间的单键可以自由旋转。则B的同分异构体中含联苯基团且能发生银镜反应的至少有____种。
(6)M(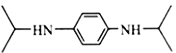 )是制备合成染料、颜料的重要中间产物。参照上面合成路线,请以丙酮(
)是制备合成染料、颜料的重要中间产物。参照上面合成路线,请以丙酮(![]() )和对苯二胺(
)和对苯二胺(![]() )为主要有机原料设计M的合成路线________________(其它试剂任选)。
)为主要有机原料设计M的合成路线________________(其它试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图装置,电流计指针会偏转,正极变粗,负极变细,符合这种情况的是

A. 正极:Cu 负极:Zn S:稀H2SO4
B. 正极:Zn 负极:Cu S:CuSO4溶液
C. 正极:Ag 负极:Zn S:AgNO3溶液
D. 正极:Fe 负极:Cu S:AgNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关。下列说法中正确的是

A. ①②中Mg作负极、③④中Fe作负极
B. ②中A1作负极,电极反应式为2A1-6e-=2Al3+
C. ③中Fe作负极,电极反应式为Fe-2e-=Fe2+
D. ④中Cu作正极,电极反应式为O2+4e-+2H2O=4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L密闭容器内,800℃时反应2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.006 | 0.006 | 0.006 |
(1)上述反应在第5s时NO的转化率是___________。用O2表示从0~2s内该反应的平均速率V(O2)=__________。
(2)下图中表示NO2的变化的曲线是__________。

(3)能使该反应的反应速率增大的是__________。
A.及时分离出NO2气体 B.适当升高温度 C.增大O2的浓度 D.选择高效催化剂
(4)能说明该反应已达到平衡状态的是___________。
A.v(NO2)=2v(O2) B.容器内压强保持不变
C.v逆(NO)=2v正(O2) D.容器内质量保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述不正确的是( ) 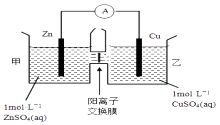
A.铜电极上发生还原反应
B.电池工作一段时间后,甲池的c(SO42﹣)不变
C.电池工作一段时间后,乙池溶液的总质量增加
D.阴阳离子离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com