
【题目】用菱锰矿(主要含MnCO3、FeCO3、Al2O3、SiO2)制备MnSO4·H2O的工艺流程如下:
Ⅰ.向菱锰矿中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量MnO2,过滤;
Ⅲ.调节滤液pH=a,过滤;
Ⅳ.浓缩、结晶、分离、干燥得到产品;
Ⅴ.检验产品纯度。
(1)步骤Ⅰ中,滤渣的主要成分是 。
(2)将MnO2氧化Fe2+的离子方程式补充完整:
![]() MnO2 +
MnO2 +![]() Fe2++
Fe2++![]() =
=![]() Mn2+ +
Mn2+ + ![]() Fe3+ +
Fe3+ +![]()
(3)与选用Cl2作为氧化剂相比,MnO2的优势主要在于:原料来源广、成本低、可避免环境污染、 。
(4)已知:生成氢氧化物沉淀的pH
Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Mn(OH)2 | |
开始沉淀时 | 3.4 | 6.3 | 1.5 | 7.6 |
完全沉淀时 | 4.7 | 8.3 | 2.8 | 10.2 |
注:金属离子的起始浓度为0.1mol/L
步骤Ⅲ中a的取值范围是 。
(5)步骤Ⅴ,通过测定产品中锰元素的质量分数来判断产品纯度。
已知一定条件下,MnO4-与Mn2+反应生成MnO2 。取x g产品配成溶液,用0.1mol/L KMnO4溶液滴定,消耗KMnO4溶液y mL,产品中锰元素的质量分数为 。
【答案】(1)SiO2
(2)1 2 4H+ 1 2 2H2O
(3)不会引入Cl-,使制得的MnSO4H2O产品更纯净
(4)4.7≤a<7.6
(5)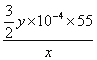
【解析】
试题分析: 菱锰矿(主要含MnCO3、FeCO3、Al2O3、SiO2),加入过量稀H2SO4,生成硫酸锰、硫酸亚铁、硫酸铝溶液,二氧化硅不溶解,;向滤液中加入过量MnO2,将亚铁离子氧化为铁离子,本身被还原为二价锰离子,调节滤液pH,使三价铁离子和铝离子沉淀,过滤除去氢氧化铁和氢氧化铝固体,对硫酸锰溶液进行浓缩、冷切结晶、过滤、洗涤干燥得到产品。(1)菱锰矿(主要含MnCO3、FeCO3、Al2O3、SiO2),加入过量稀H2SO4,生成硫酸锰、硫酸亚铁、硫酸铝溶液,二氧化硅不溶解,滤渣的主要成分是二氧化硅,故答案为:二氧化硅;(2)锰元素化合价由+4价降低到+2价,铁元素由+2价升高到+3价,根据化合价升降守恒、电荷守恒、原子守恒,配平反应为MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O,故答案为:MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;(3)选用Cl2作为氧化剂会最后的溶液中引入氯离子,使制得的产品不纯,而MnO2不会引入Cl-,使制得的MnSO4H2O产品更纯净,故答案为:不会引入Cl-,使制得的MnSO4H2O产品更纯净;(4)调节滤液pH,使三价铁离子和铝离子沉淀,根据表格可知二价锰离子开始沉淀的pH=7.6,铝离子开始沉淀的pH=4.7,故4.7≤a<7.6,故答案为:4.7≤a<7.6;(5)设含有硫酸锰的物质的量为z,根据方程式
3Mn2++2MnO4-+2H2O=5MnO2+4H+
3mol 2mol
z 0.1y×10-3mol
z=0.15y×10-3mol,
锰元素的质量分数=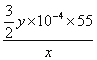


 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案科目:高中化学 来源: 题型:
【题目】(1)已知20℃时的溶解度:Na2CO3:S=21.2g; NaHCO3:S=9.6g。则20oC恒温条件下向121.2g饱和碳酸钠溶液中通入足量的CO2气体,理论上可以析出NaHCO3__________g(小数点后保留1位)
(2)向500mL KOH溶液中缓慢通入一定量的![]() 气体,充分反应后,在减压低温下蒸发溶液,得到白色固体。若通入
气体,充分反应后,在减压低温下蒸发溶液,得到白色固体。若通入![]() 气体为2.24L(标准状况下),得到11.9g的白色固体。则所用的KOH溶液的物质的量浓度为______mol/L。
气体为2.24L(标准状况下),得到11.9g的白色固体。则所用的KOH溶液的物质的量浓度为______mol/L。
(3)将一定质量的钠加入到89g水中,完全反应后的溶液为100g,则该溶液的质量分数为________
(4)现有甲、乙两瓶无色溶液,已知它们可能是AlCl3溶液和NaOH溶液.现做如下实验:
① 取440mL甲与120mL乙反应,产生1.56g沉淀;
② 取440mL乙与120mL甲反应,也产生1.56g沉淀;
③ 取120mL甲溶液与400mL乙溶液反应,则产生3.12g沉淀;
通过必要的计算和推理判定:
甲溶液为 溶液,其物质的量浓度为 mol·L-1;
乙溶液为 溶液,其物质的量浓度是 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组为了检验浓硫酸与木炭在加热条件下反应产生的SO2和CO2气体,设计了如图所示实验装置,a、b、c为止水夹,B是用于储气的气囊,D中放有用I2和淀粉的蓝色溶液浸湿的脱脂棉。
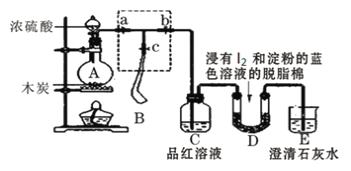
(1)装置A中盛放浓硫酸的仪器名称______________。
(2)装置A中发生反应的化学方程式为___________________________________。
(3)实验时,装置C中的现象为_______________________________________。
(4)此实验成败的关键在于控制反应产生气体的速率不能过快,因此设计了虚框部分的装置,则正确的操作顺序是_________________(用操作编号填写)。
①向A装置中加入浓硫酸,加热,使A中产生的气体进入气囊B,当气囊中充入一定量气体时,停止加热;
②待装置A冷却,且气囊B的体积不再变化后,关闭止水夹a,打开止水夹b,慢慢挤压气囊,使气囊B中气体慢慢进入装置C中,待达到实验目的后,关闭止水夹b;
③打开止水夹a和c,关闭止水夹b;
(5)当D中产生_________________现象时,可以说明使E中澄清石灰水变浑浊的是CO2,而不是SO2;写出D中发生反应的化学方程式_______________________________________,当D中反应发生0.3mol电子转移时,发生反应的气体的体积(标准状况)是_____________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】牛奶放置时间长了会变酸,这是因为牛奶中含有的乳糖,在微生物的作用下分解变成了乳酸。乳酸最初就是从酸牛奶中得到并由此而得名的。乳酸的结构简式为CH3CH(OH)COOH。完成下列问题:
(1)写出乳酸分子中官能团的名称:______________________________________________。
(2)写出乳酸与足量金属钠反应的化学方程式:___________________________________________。
(3)写出乳酸与少量碳酸钠溶液反应的化学方程式:_____________________________________________。
(4)乳酸在浓硫酸作用下,两分子相互反应生成六元环状结构的物质,写出此生成物的结构简式:
____________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硅和硅的化合物性质的叙述,正确的是( )
A.二氧化硅溶于水可制得硅酸
B.二氧化硅是酸性氧化物,不跟任何酸起反应
C.硅酸的酸性比碳酸弱
D.硅在常温下能跟氢气起反应生成SiH4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组拟用右图装置制备氢氧化亚铁并观察其颜色。提供化学药品:铁屑、稀硫酸、氢氧化钠溶液。
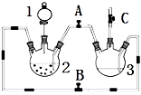
(1)稀硫酸应放在 中(填写仪器名称).
(2)本实验通过控制A、B、C三个开关,将仪器中的空气排尽后,再关闭开关B,打开开关A,就可观察到氢氧化亚铁的颜色。试分析实验开始时排尽装置中空气的理由
(3)实验时为防止仪器2中铁粉通过导管进入仪器3中,可采取的措施是 。
(4)在FeSO4溶液中加入(NH4)2SO4固体可制备摩尔盐晶体[(NH4)2SO4·FeSO4·6H2O] (相对分子质量392),该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇。
①为洗涤(NH4)2SO4·FeSO4·6H2O粗产品,下列方法中最合适的是
A.用冷水洗 B.先用冷水洗,后用无水乙醇洗
C.用30%的乙醇溶液洗 D.用90%的乙醇溶液洗
②为了测定产品的纯度,称取a g产品溶于水,配制成500mL溶液,用浓度为c mol·L-1的酸性KMnO4溶液滴定。每次所取待测液体积均为25.00mL,实验结果记录如下:
实验次数 | 第一次 | 第二次 | 第三次 |
消耗高锰酸钾溶液体积/mL | 25.52 | 25.02 | 24.98 |
i滴定过程中发生反应的离子方程式为
ii滴定终点的现象是
iii通过实验数据计算的该产品纯度为 (用字母a,c表示).上表中第一次实验中记录数据明显大于后两次,其原因可能是
A.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
D.该酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com