
【题目】有X、Y、Z三种短周期元素,分别位于不同的周期。已知X和Y原子最外层电子数相同,Z原子次外层只有2个电子,X和Z可以形成离子化合物X2Y,Y和Z可以形成共价化合物Y2Z
(1)写出X、Y、Z三种元素的元素符号:X是____,Y是_____,Z是_____ ;
(2)X2Z的电子式_________, Y2Z的电子式________;
(3)X2Z和 Y2Z反应的化学方程式_________________________。
【答案】Na H O ![]()
![]() Na2O+H2O==2NaOH
Na2O+H2O==2NaOH
【解析】
Z原子次外层只有2个电子,所以Z是第二周期元素,X、Y、Z三种短周期元素,分别位于不同的周期,则X和Y位于第一、第三周期,X和Y原子最外层电子数相同,所以X和Y位于同一主族,X和Z可以形成离子化合物X2Z,Y和Z可以形成共价化合物Y2Z,则Y为氢元素,X为钠元素,Z为氧元素,据此答题。
由分析可知X为Na元素,Y为H元素,Z为O元素。
(1)根据上面的分析可知,X、Y、Z三种元素分别为Na、H、O,故答案为:Na;H;O。
(2)X2Z为氧化钠,它的电子式为![]() ,Y2Z为水,它的电子式为
,Y2Z为水,它的电子式为![]() ,故答案为:
,故答案为:![]() ;
; ![]() 。
。
(3)Na2O和H2O反应的化学方程式为Na2O+H2O=2NaOH,故答案为:Na2O+H2O=2NaOH。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是四种短周期元素,X原子M层上的电子数是原子核外电子层数的2倍;Y原子最外层电子数是次外层电子数的2倍;Z元素的单质为双原子分子,Z的氢化物水溶液呈碱性;W元素最高正价是+7价。回答下列问题:
(1)元素X原子结构示意图为________。
(2)元素Y的最高价氧化物的分子式为__________,其中一种同位素可测定文物年代,这种同位素的符号是________。
(3)元素Z能与氢元素形成18电子分子,分子式为_________。
(4)元素W的单质与元素X的低价氧化物在水溶液中反应的离子方程式为___________。
(5)ZW3常温下呈液态,可与水反应生成一种具有漂白性的酸和一种碱性气体,反应的化学方程式为_______。
(6)探寻物质的性质差异性是学习的重要方法之一。X、Y、Z、W四种元素的最高价氧化物的水化物中酸性明显不同于其他三种酸的是_______(用酸的分子式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO3,还含有少量MgO、SiO2等杂质)来制备,工艺流程如下:

回答下列问题:
(1)“酸浸”后,钛主要以TiOCl42-形式存在,写出相应反应的离子方程式_______。
(2)Li2Ti5O15中过氧键的数目为4,其中Ti的化合价为______。
(3)若“滤液②”中c(Mg2+)=0.02mol/L,加入双氧水和磷酸(设溶液体积增加1倍),使Fe2+恰好沉淀完全即溶液中c(Fe3+)=1×10-5mol/L,此时_____(填“有”或“无”)Mg3(PO4)2沉淀生成。FePO4、Mg3(PO4)2的Ksp分别为1.3×10-2、1.0×10-2。
(4)写出“高温煅烧②”中由FePO4制备LiFePO4的化学方程式_________。
(5)TiO2·xH2O加热制得的粗TiO2是电解法生产金属钛的一种较先进的方法,电解液为某种可传导02-离子的熔融盐,原理如图所示,则其阴极电极反应为:_______,电解过程中阳极电极上会有气体生成,该气体可能含有____________。
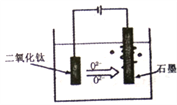
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA代表阿伏加德罗常数的值,下列说法正确的是
A. 32.5g锌粒与足量盐酸反应产生11.2 L H2
B. 标准状况下,11.2 L CCl4所含分子数为0.5NA
C. 1mol NaHSO4中含有的阴阳离子的总数目为 3NA
D. 常温常压下,40g O2和O3的混合气体中,含有氧原子的数目为2.5 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】50mL 18mol/L的硫酸中加入足量的铜片并加热,被还原的硫酸的物质的量
A. 小于0.45mo1B. 等于0.45molC. 在0.45mol和0.9mol之间D. 大于0.9mo1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:
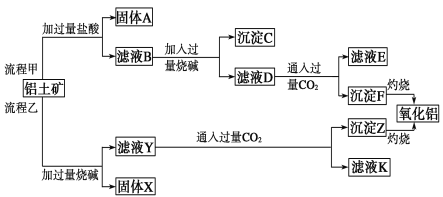
请回答下列问题:
(1)流程甲加入盐酸后生成Al3+的离子方程式为_______________________。
(2)流程乙加入烧碱后生成AlO2-的离子方程式为____________________。
(3)滤液E、K中溶质的主要成分是__________(填化学式)。
(4)已知298 K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,取适量的滤液B,加入一定量的烧碱达到沉淀溶解平衡,测得pH=13.00,则此温度下残留在溶液中的c(Mg2+)=__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中草药秦皮中含有的七叶树内酯(每个折点表示一个碳原子,氢原子未画出),具有抗菌作用。若1 mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
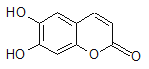
A、2 mol Br2 2 mol NaOH
B、2 mol Br2 3 mol NaOH
C、3 mol Br2 4 mol NaOH
D、4 mol Br2 4 mol NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,水作还原剂的是
A. 2H2O+2F2=4HF+O2 B. 2Na2O2+2H2O=4NaOH+O2↑
C. 2Na+2H2O=2NaOH+H2↑ D. 2H2O2 ![]() 2H2O+O2↑
2H2O+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的固定对人类的生存发展具有重要意义,科学家一直致力于“人工固氮”的新方法研究。
(1)豆科植物的根瘤菌含有一种固氮酶,能在常温下将空气中的氮气转化为自身生长所需的含氮化合物,下列说法错误的是________(填标号)。
a.固氮酶是一种蛋白质
b.固氮酶能降低固氮反应发生所需的能量
c.固氮酶能使固氮反应的平衡正向移动
d.固氮酶能加快固氮反应的速率
(2)合成氨是目前最重要的固氮方法。下图为合成氨反应N2(g)+3H2(g)![]() 2NH3(g)在不同温度和压强、使用相同催化剂条件下,初始时氮气、氢气的体积之比为1∶3时,平衡混合物中氨的体积分数的变化曲线如下图。
2NH3(g)在不同温度和压强、使用相同催化剂条件下,初始时氮气、氢气的体积之比为1∶3时,平衡混合物中氨的体积分数的变化曲线如下图。
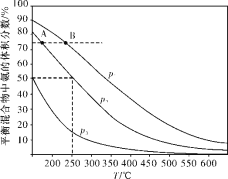
①A、B两平衡状态相比较,前者较大的是___________(填标号)。
a.平衡常数 b.平衡混合物的平均摩尔质量
c.氢气的转化率 d.从反应开始至达到平衡状态所需要的时间
②图中p1、p2、p3由大到小的顺序为_____________________。
③在250 ℃、p2下,H2的转化率为_____________%(结果保留小数点后一位)。
(3)据报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3和一种单质。已知:①H2(g)+![]() O2(g)===H2O(l) ΔH1=-285.6 kJ/mol,②N2(g)+3H2(g)
O2(g)===H2O(l) ΔH1=-285.6 kJ/mol,②N2(g)+3H2(g)![]() 2NH3(g) ΔH2=-92.2 kJ/mol,写出此条件下氮气和水反应的热化学方程式:________________。
2NH3(g) ΔH2=-92.2 kJ/mol,写出此条件下氮气和水反应的热化学方程式:________________。
(4)下图为一种常温常压下水溶液中电化学合成氨的实验装置示意图。请据此写出其正极反应的电极反应式:_________________________________。
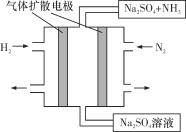
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com