
【题目】碳酸钠是造纸、玻璃、纺织、制革等行业的重要原料。工业碳酸钠(纯度约98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO42-等杂质,提纯工艺流程如下:
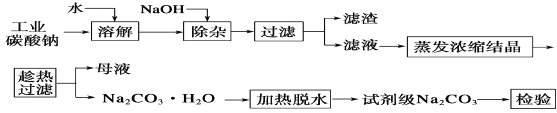
已知碳酸钠的溶解度(S)随温度变化的曲线如下图所示:
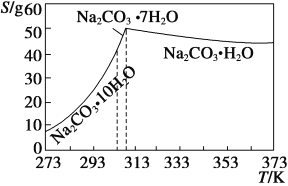
回答下列问题:
(1)滤渣的主要成分为_______________________________。
(2)“趁热过滤”的原因是___________________________。
(3)若在实验室进行“趁热过滤”,可采取的措施是_____(写出一种)。
(4)已知:Na2CO3·10H2O (s)===Na2CO3(s)+10H2O(g) ΔH1= +532.36 kJ·mol-1
Na2CO3·10H2O(s)===Na2CO3·H2O(s)+9H2O(g) ΔH2= +473.63 kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式____________。
【答案】
(1)Mg(OH)2 Fe(OH)3 CaCO3
(2)使析出的晶体为NaCO3·H2O,防止因温度过低析出NaCO3·10H2O,令后续加热脱水时间长。
(3)用已预热的布氏漏斗趁热过滤
(4)NaCO3·H2O(s)= NaCO3(s)+ H2O(g) △H=+58.73kJ·mol-1
【解析】
试题分析:(1)工业碳酸钠(钝度约98%)中含有Mg2+,Fe3+,Ca2+,所以“除杂”中加入过量的NaOH溶液,可生成Mg(OH)2、Fe(OH)3沉淀,滤渣的主要成分为Mg(OH)2、Fe(OH)3,故答案为:Mg(OH)2、Fe(OH)3;
(2)根据所给的坐标图可以发现:温度减少至313K时发生突变,溶解度迅速减少,若不趁热过滤将析出晶体,所以“趁热过滤”的原因是使析出的晶体为Na2CO3H2O,防止因温度过低而析出Na2CO310H20晶体或Na2CO37H20晶体,使后续的加热脱水耗时长,故答案为:使析出的晶体为Na2CO3H2O,防止因温度过低而析出Na2CO310H20晶体或Na2CO37H20晶体,使后续的加热脱水耗时长;
(3)在实验室进行“趁热过滤”时,要注意减少过滤的时间和保持过滤时的温度,可采取的措施是用预热过滤装置(或已预热的布氏漏斗趁热抽滤,或用常压热过滤漏斗进行过滤),故答案为:用预热过滤装置(或已预热的布氏漏斗趁热抽滤,或用常压热过滤漏斗进行过滤);
(4)通过观察两个热化学方程式,利用盖斯定律,可将两式相减得到Na2CO3H2O(S) ═ Na2CO3(s) + H2O(g),即Na2CO3H2O(S) ═ Na2CO3(s) + H2O(g)△H = +58.73 kJ/mol


 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:高中化学 来源: 题型:
【题目】有50 mL NaOH溶液,向其中逐渐通入一定量的CO2,随后取此溶液10 mL将其稀释至100 mL,并向此稀释后的溶液中逐滴加入0.1 mol·L-1的HCl溶液,产生CO2气体的体积(标准状况)与所加入盐酸的体积之间的关系如下图所示:
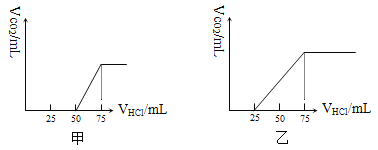
(1)甲溶液中的溶质是_____________,其物质的量之比为__________________。
(2)乙溶液中的溶质是_____________,在标准状况下吸收CO2气体的体积为________。
(3)原NaOH溶液的物质的量浓度为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关燃料的说法错误的是( )
A.含硫化石燃料的大量燃烧是形成酸雨的主要原因
B.绿色化学的核心就是利用化学原理对工业生产上造成的环境污染进行彻底治理
C.以压缩天然气、液化石油气代替燃油可减少大气污染
D.燃料不完全燃烧排放的CO是大气污染物之一
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学—物质结构与性质】M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素。M基态原子L层中p轨道电子数是s电子的2倍,R是同周期元素中最活泼的金属元素,X和M形成的一种化合物是引起酸雨的主要大气污染物,Z的基态原子4s和3d轨道半充满。请回答下列问题:
(1)R基态原子的电子排布式是 ,X和Y中电负性较大的是 (填元素符号)。
(2)X的氢化物的沸点低于与其组成相似的M的氢化物,其原因是________________。
(3)X与M形成的XM3分子的空间构型是__________。
(4)M和R所形成的一种离子化合物R2M晶体的晶胞如右图所示,则图中大球代表的离子是_________(填离子符号)。

(5)在稀硫酸中,Z的最高价含氧酸的钾盐(橙色)氧化M的一种氢化物,Z被还原为+3价,该反应的化学方程式是_________。
(6)若晶胞的棱长为a cm ,则R2M晶体的密度为=___________g·cm–3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生物界与非生物界具有统一性,是因为
A. 构成细胞的化合物在非生物界都存在
B. 构成细胞的无机物在非生物界都存在
C. 构成细胞的化学元素在非生物界都存在
D. 生物与非生物都具有新陈代谢的功能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列小实验不能成功的是( )
A. 用活性炭将硬水软化 B. 用紫卷心菜自制酸碱指示剂
C. 用食醋制无壳鸡蛋 D. 用灼烧闻气味的方法区分棉纤维和羊毛纤维
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据估计,地球上的绿色植物通过光合作用每年能结合来自CO2中的碳1500亿吨和来自水中的氢250亿吨,并释放4000亿吨氧气。光合作用的过程一般可用下式表示:

CO2+H2O+微量元素(P、N等)![]() (蛋白质、碳水化合物、脂肪等)+O2
(蛋白质、碳水化合物、脂肪等)+O2
下列说法不正确的是
A. 某些无机物通过光合作用可转化为有机物
B. 碳水化合物就是碳和水组成的化合物
C. 叶绿素是光合作用的催化剂
D. 增加植被,保护环境是人类生存的需要
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用SiO2与C在高温下发生反应制造粗硅,粗硅中含有SiC,其中Si和SiC的物质的量之比为1∶1。下列说法正确的是( )
A.硅元素在地壳中含量居第二位,主要以单质硅和硅酸盐的形式存在
B.纯净的SiO2只能用于制造光导纤维
C.SiC因有很高的化学稳定性和热稳定性,故可用作高温结构陶瓷材料。
D.制造粗硅时的上述反应方程式为:2SiO2+5C![]() Si+SiC+4CO↑
Si+SiC+4CO↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6 mol·L-1的H2SO4溶液中,乙同学将电极放入6 mol·L-1的NaOH溶液中,如图所示。
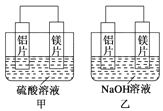
(1)写出甲中正极的电极反应式___________________。
(2)乙中总反应的离子方程式:________________________。
(3)如果甲与乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出 活动性更强,而乙会判断出_____________活动性更强。(填写元素符号)
(4)由此实验得出的下列结论中,正确的有______________。
A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动性顺序表已过时,没有实用价值了
D.该实验说明化学研究对象复杂、反应受条件影响较大,应具体问题具体分析
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com