
| A、水的电离程度始终增大 | ||||
| B、当加入氨水的体积为1 mL时,c(NH4+)=c(CH3COO-) | ||||
C、
| ||||
| D、c(CH3COOH)与c(CH3COO-)之和始终保持不变 |
| c(H+)?c(NH3?H2O) |
| c(NH4+) |
| c(NH4+) |
| c(NH3?H2O) |
| c(OH-)?c(NH4+) |
| c(NH3?H2O) |
| c(NH4+) |
| c(NH3?H2O) |
| c(NH4+) |
| c(NH3?H2O) |


 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:
| A、SiO2是酸性氧化物,不与任何酸反应 |
| B、物质的量浓度相同的Na2SiO3和Na2CO3溶液,其pH值前者大于后者 |
| C、可以用加热的方法除去NaCl中的NH4Cl |
| D、用pH试纸测得新制氯水的pH为2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 装置用于Cu和浓H2SO4制取少量的SO2气体 |
B、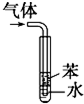 用于吸收HCl气体能防倒吸 |
C、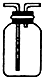 可用于收集气体H2、CO2、Cl2、NH3 |
D、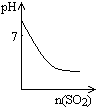 表示将SO2气体通入溴水中,所得溶液的pH变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2:3 | B、3:8 |
| C、1:4 | D、1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、曲线A是向NaAlO2溶液中滴入盐酸至过量 |
| B、曲线B是向澄清石灰水中通入CO2至过量 |
| C、曲线C是向含有盐酸的AlCl3溶液中滴入NaOH溶液至过量 |
| D、曲线D是向含有等物质的量的Ca(OH)2、KOH的混合溶液中通入CO2至沉淀消失 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ① | ② | ③ | ④ |
| 0.1mol/L NaOH溶液 | pH=11 NaOH溶液 | 0.1mol/L CH3COOH溶液 | pH=3 CH3COOH溶液 |
| A、由水电离出的c(H+):③<① |
| B、③稀释到原来的100倍后,pH与④相同 |
| C、①与③混合,若溶液pH=7,则V(NaOH)>V(CH3COOH) |
| D、②与④混合,若溶液显酸性,则所得溶液中离子浓度可能为:c(CH3COOˉ)>c(H+)>c(Na+)>c(OHˉ) |
查看答案和解析>>
科目:高中化学 来源: 题型:
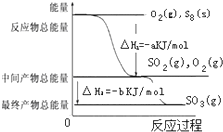 在一定条件下,S8(s)和O2(g)发生反应依次转化为SO2(g)和SO3(g).反应过程和能量关系可用如图简单表示(图中的△H表示生成1 mol含硫产物的数据).由图得出的结论正确的是( )
在一定条件下,S8(s)和O2(g)发生反应依次转化为SO2(g)和SO3(g).反应过程和能量关系可用如图简单表示(图中的△H表示生成1 mol含硫产物的数据).由图得出的结论正确的是( )| A、S8(s)的燃烧热△H=-8akJ?mol-1 |
| B、2SO3(g)?2SO2(g)+O2(g);△H=-2b kJ?mol-1 |
| C、S8(s)+8O2(g)=8SO2(g);△H=-a kJ?mol-1 |
| D、由1molS8(s)生成SO3(g)的反应热△H=-(a+b)kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v (NH3)=0.008 mol/(L?s) |
| B、v (NO)=0.04 mol/(L?s) |
| C、v (O2)=0.006 mol/(L?s) |
| D、v (H2O)=0.06 mol/(L.min) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com