
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
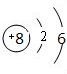 ,故答案为:O;
,故答案为:O;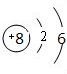 ;
;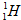 、
、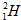 、
、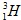 ,故答案为:
,故答案为: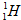 ;
;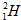 ;
;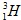 ;
;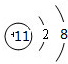 ,故答案为:
,故答案为: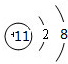 .
.


 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:
| A、水的电离程度始终增大 | ||||
| B、当加入氨水的体积为1 mL时,c(NH4+)=c(CH3COO-) | ||||
C、
| ||||
| D、c(CH3COOH)与c(CH3COO-)之和始终保持不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HClO+NaOH=NaClO+H2O 非氧化还原反应 复分解反应 |
| B、MnO2+4HCl(浓)=MnCl2+Cl2↑+2H2O氧化还原反应 分解反应 |
| C、3Fe+2O2=Fe3O4 非氧化还原反应 化合反应 |
| D、Fe2O3+3CO=2Fe+3CO2 氧化还原反应 置换反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4Cl═NH3↑+HCl↑ |
| B、NH3+CO2+H2O═NH4HCO3 |
| C、2NaOH+Cl2═NaCl+NaClO+H2O |
| D、2Na2O2+2 CO2═2Na2 CO3+O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、HCl是氧化剂 |
| B、Cl元素被还原 |
| C、MnO2在反应中失去电子 |
| D、生成1 mol Cl2时有2 mol电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同周期相邻主族的两元素原子序数均相差1 |
| B、原子最外层有2个电子的元素一定是金属元素 |
| C、第ⅦA族元素从上到下,其氢化物的酸性逐渐增强 |
| D、同主族元素从上到下,单质的熔点逐渐降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
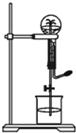 喷泉是一种常见的自然现象,其产生原因是存在压强差.图中为化学教学中所用的喷泉实验装置实验装置.已知3NO2+H2O=2HNO3+NO (NO为气体,难溶于水)在烧瓶中充满干燥NO2气体,胶头滴管及烧杯中分别盛有水进行喷泉实验.假设实验在标准状况下进行,经充分反应后,计算瓶内HNO3溶液的物质的量浓度为多少?
喷泉是一种常见的自然现象,其产生原因是存在压强差.图中为化学教学中所用的喷泉实验装置实验装置.已知3NO2+H2O=2HNO3+NO (NO为气体,难溶于水)在烧瓶中充满干燥NO2气体,胶头滴管及烧杯中分别盛有水进行喷泉实验.假设实验在标准状况下进行,经充分反应后,计算瓶内HNO3溶液的物质的量浓度为多少?查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.03mol/L |
| B、0.3mol/L |
| C、0.05mol/L |
| D、0.04mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com