
【题目】一定温度下,在三个容积均为 1.0L 的恒容密闭容器中发生反应: CH3OH(g)+CO(g) CH3COOH(g) △H<0。下列说法正确的是
容器编号 | 温度/K | 物质的起始浓度/mol/L | 乙酸的平衡浓度/ mol/L | 平衡常数 | ||
c(CH3OH) | c(CH3OH) | c(CH3COOH) | c(CH3COOH) | |||
I | 530 | 0.50 | 0.5 | 0 | 0..40 | K1 |
II | 530 | 0.20 | 0.2 | 0.4 | K2 | |
III | 510 | 0 | 0 | 0.5 | K3 | |
A.三个容器中的平衡常数 K1<K2< K3
B.达平衡时,容器I与容器II中的总压强之比为3 : 4
C.达平衡时,容器I中CH3OH转化率与容器 III 中CH3COOH转化率之和小于l
D.达平衡时,容器III中的正反应速率比容器I中的大
【答案】C
【解析】
A.平衡常数只于温度有关,温度不变平衡常数不变,则 K1=K2,反应体系△H<0,降低温度,平衡正向移动,平衡常数增大,则K1=K2< K3,故A错误;
B.根据理想气体状态方程pV=nRT,容器为恒容装置,V不变,则有p=cRT,容器Ⅰ与容器Ⅱ温度相同,则体系压强与体系中反应物总浓度成正比,温度不变,化学平衡常数不变,容器Ⅰ中平衡时c(CH3OH)=0.5mol/L0.4mol/L=0.1mol/L,c(CO)=0.5mol/L0.4mol/L=0.1mol/L,c(CH3COOH)=0.4mol/L,K=![]() =
=![]() =40,设容器Ⅱ反应到达平衡时CH3OH转化cmol/L,所以达平衡时,容器I与容器II中的总压强之比为=
=40,设容器Ⅱ反应到达平衡时CH3OH转化cmol/L,所以达平衡时,容器I与容器II中的总压强之比为=![]() =
=![]() =
=![]() ,容器ⅡQc=
,容器ⅡQc=![]() =10<K=40,可知容器Ⅱ中反应向右进行,则c为正值,所以达平衡时,容器I与容器II中的总压强之比大于3:4,故B错误;
=10<K=40,可知容器Ⅱ中反应向右进行,则c为正值,所以达平衡时,容器I与容器II中的总压强之比大于3:4,故B错误;
C.容器Ⅲ与容器Ⅰ刚好为互为逆反应过程,对于容器I,容器I中CH3OH转化率容器Ⅰ中CH3COOH转化率之和刚好为1,容器Ⅲ温度低于容器I,正反应为放热反应,温度降低对正反应有利,所以容器Ⅲ中CH3COOH转化率低于容器Ⅰ以等量CH3COOH起始时的CH3COOH转化率,所以达平衡时,容器I中CH3OH转化率与容器III中CH3COOH转化率之和小于1,故C正确;
D.容器Ⅲ与容器Ⅰ刚好互为逆反应过程,但容器Ⅰ温度高于容器Ⅲ,温度越高,化学反应速率越大,所以达到化学平衡时容器III中的正反应速率比容器I中的小,故D错误;
答案选C。


科目:高中化学 来源: 题型:
【题目】研究发现,NOx和SO2是雾霾的主要成分。
I.NOx主要来源于汽车尾气,可以利用化学方法将二者转化为无毒无害的物质。
已知:N2(g)+O2(g)![]() 2NO(g) △H=+180 kJ·mol-1
2NO(g) △H=+180 kJ·mol-1
2CO(g)+O2(g)![]() 2CO2(g) △H=-564 kJ·mol-1
2CO2(g) △H=-564 kJ·mol-1
(1)2NO(g)+2CO(g)![]() 2CO2(g)+N2(g) △H=___________。
2CO2(g)+N2(g) △H=___________。
(2)T℃时,将等物质的量的NO和CO充入容积为2L的密闭容器中,保持温度和体积不变,反应过程(0~15min)中NO的物质的量随时间变化如图所示。

①已知:平衡时气体的分压=气体的体积分数×体系的总压强,T℃时达到平衡,此时体系的总压强为p=2MPa,则T℃时该反应的压力平衡常数Kp=___________;平衡后,若保持温度不变,再向容器中充入NO和CO2各0.15 mol,平衡将___________ (填“向左”、“向右”或“不”)移动。
②15min时,若改变外界反应条件,导致n(NO)发生如上图所示的变化,则改变的条件可能是___________(填序号)
A.增大CO浓度 B.升温 C.减小容器体积 D.加入催化剂
II.SO2主要来源于煤的燃烧。燃烧烟气的脱硫减排是减少大气中含硫化合物污染的关键。
(3)如图所示的电解装置,可将雾霾中的NO、SO2转化为硫酸铵,从而实现废气的回收再利用。通入NO的电极反应式为___________;若通入的NO体积为4.48L(标况下),则另外一个电极通入的SO2质量至少为___________g。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯乙稀(![]() )是重要的有机化工原料。工业上以乙苯(
)是重要的有机化工原料。工业上以乙苯(![]() )为原料,采用催化脱氢的方法制取苯乙稀的化学方程式为:
)为原料,采用催化脱氢的方法制取苯乙稀的化学方程式为:![]() △H=124kJ·mol-1
△H=124kJ·mol-1
(1)25℃、101 kPa 时,1 mol 可燃物完全燃烧生成稳定的化合物时所放出的热量,叫做该物质的燃烧热。 已知:H2 和苯乙烯的燃烧热 △H 分别为-290 kJ·mol -1 和-4400 kJ·mol-1,则乙苯的燃烧热△H=_____kJ·mol-1。
(2)在体积不变的恒温密闭容器中,发生乙苯催化脱氢的反应,反应过程中各物质浓度随时间变化的关系如图所示。 在 t1 时刻加入 H2,t2 时刻再次达到平衡。
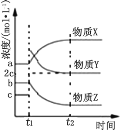
①物质 X 为_____,判断理由是_____;
②乙苯催化脱氢反应的化学平衡常数为_____(用含 a、b、c 的式子表示)。
(3)在体积为 2 L 的恒温密闭容器中通入 2 mol 乙苯蒸气,2 min 后达到平衡,测得氢气的浓度是 0.5 mol·L-1,则乙苯蒸气的反应速率为_____;维持温度和容器体积不变,向上述平衡中再通入 1.5 mol 氢气和 1.5 mol 乙苯蒸气,则 v 正______v 逆(填“大于”、“小于”或“等于”)。
(4)实际生产时反应在常压下进行,且向乙苯蒸气中掺入水蒸气,利用热力学数据计算得到温度和投料比(M)对乙苯的平衡转化率的影响如图所示。[M=![]() ]
]
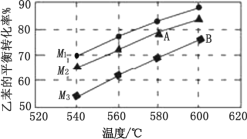
①比较图中 A、B 两点对应的平衡常数大小:KA_____KB(填“>”、“<”或“=”);
②图中投料比 M1、M2、M3 的大小顺序为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用废旧锌铁皮制备磁性Fe3O4胶体粒子及副产物ZnO。制备流程图如下:

已知:Zn及化合物的性质与Al及化合物的性质相似。请回答下列问题:
(1)用NaOH溶液处理废旧锌铁皮的作用有_________________________________________。
A.去除油污 | B.溶解镀锌层 | C.去除铁锈 | D.钝化 |
(2)调节溶液A的pH可产生Zn(OH)2沉淀,为制得ZnO,后续操作步骤是______________。
(3)由溶液B制得Fe3O4胶体粒子的过程中,须持续通入N2,原因是___________________。
(4)Fe3O4胶体粒子能否用减压过滤发实现固液分离?____________(填“能”或“不能”),理由是_________________________________________________。
(5)用重铬酸钾法(一种氧化还原滴定法)可测定产物Fe3O4中的二价铁含量。若需配制浓度为0.01000 mol·L-1的K2Cr2O7标准溶液250 mL,应准确称取_______g K2Cr2O7(保留4位有效数字,已知M(K2Cr2O7)=294.0 g·mol-1)。
配制该标准溶液时,下列仪器中不必要用到的有_____________。(用编号表示)。
①电子天平 ②烧杯 ③量筒 ④玻璃棒 ⑤容量瓶 ⑥胶头滴管 ⑦移液管
(6)滴定操作中,如果滴定前装有K2Cr2O7标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失,则测定结果将__________(填“偏大”、“偏小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲~庚等元素在周期表中的相对位置如表,己的最高价氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数,下列判断正确的是( )
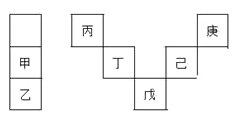
A.丙与戊的原子序数相差28
B.气态氢化物的稳定性:庚<己<戊
C.常温下,甲和乙的单质均能与水剧烈反应
D.丁的最高价氧化物为分子晶体,可用于制造光导纤维
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组利用麦芽酚 A 制备某药物中间体 X, 其合成路线如下
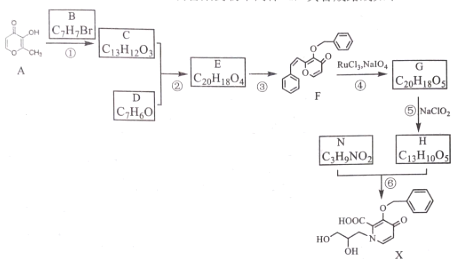
已知:

请回答 :
(l)化合物F的含氧官能团名称为__________,化合物E 的结构简式为____________。
(2)写出反应① 的化学方程式:_________________ 。
(3)下列说法不正确的是__________ ( 填字母序号)。
A.化合物 E 可发生取代、加成、消去、氧化、还原等反应
B.化合物 N 的同分异构体可能是某氨基酸
C.反应③属于消去反应
D.化合物X在一定条件下反应生成的物质中可能含有3个六元环
(4) 写出化合物H同时符合下列条件的同分异构体的结构简式______________。
a.IR 谱检测表明:分子中含有2个独立的苯 环,不含其他的环 ;
b.1H - NMR 谱表明:分子中共有3种化学环境不同的氢原子;
(5)由乙烯和苯为原料合成 D, 利用已知信息,设计合成路线(用流程图表示,无机试剂任选)__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化物(NOx)是有毒的大气污染物,研究发现,可以采用如图装置有效去除氮的氧化物,下列说法正确的是( )
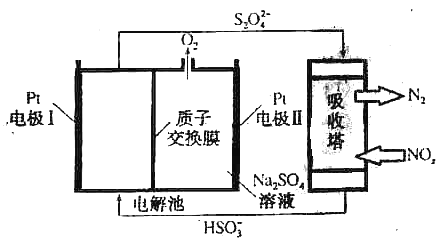
A.电解过程中,Pt电极I上发生氧化反应
B.电解过程中,Pt电极II上发生反应:4OH--4e-=2H2O+O2↑
C.电解过程中,左极室pH会逐渐减小,
D.若NOx为NO,转移1mol电子时吸收塔中消耗0.5molS2O42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在密闭容器中,能表示反应X(g)+2Y(g)![]() 2Z(g)一定达到化学平衡状态的是( )
2Z(g)一定达到化学平衡状态的是( )
①X、Y、Z的物质的量之比为1∶2∶2
②X、Y、Z的浓度不再发生变化
③容器中的压强不再发生变化
④单位时间内生成n mol Z,同时生成2n mol Y
A.①②B.①④C.②③D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A.用石墨电极电解MgCl2溶液:Mg2++2Cl-+2H2O![]() Mg(OH)2↓+Cl2↑+H2↑
Mg(OH)2↓+Cl2↑+H2↑
B.泡沫灭火器工作时化学反应:2Al3++3CO32-+6H2O=Al(OH)3↓+3CO2↑
C.向Ca(HCO3)2溶液中滴加少量NaOH溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O
D.硫化钠的水解反应;S2-+H3O+=HS-+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com