
【题目】海冰是海水冻结而成的咸水冰。海水冻结时,部分来不及流走的盐分以卤汁的形式被包围在冰晶之间,形成“盐泡”![]() 假设盐分以一个NaCl计
假设盐分以一个NaCl计![]() ,其大致结构如下图所示,若海冰的冰龄达到1年以上,融化后的水为淡水。下列叙述正确的是( )
,其大致结构如下图所示,若海冰的冰龄达到1年以上,融化后的水为淡水。下列叙述正确的是( )

A.海冰内层“盐泡”越多,密度越小
B.海冰冰龄越长,内层的“盐泡”越多
C.海冰内层“盐泡”内的盐分主要以NaCl分子的形式存在
D.海冰内层NaCl的浓度约为![]() 设冰的密度为
设冰的密度为![]()
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:
【题目】某密闭容器中发生如下反应:X(g)+3Y(g)![]() 2Z(g),△H<0。如图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量,下列说法中正确的是( )
2Z(g),△H<0。如图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量,下列说法中正确的是( )
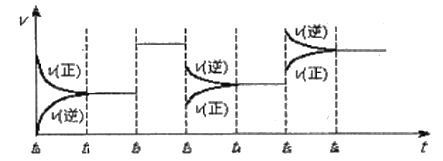
A.t3时降低了温度
B.t2-t3时间段相对于t1-t2时间段来说平衡并没有移动
C.t5时增大了压强
D.t4-t5时间内反应物的转化率最低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A是一种常见金属,F是一种红褐色沉淀。根据图中转化关系,回答下列问题。

(1)写出F、G的化学式:F.________;G._______。
(2)检验D中阳离子的方法为_____________________________________________________
(3)保存C溶液时要加固体A的原因是_____________________________________________
(4)写出下列转化的离子方程式:
①B→C:______________________________________________________________________
②C→D:______________________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(g)+5B(g)4C(g)+6D(g)在四种不同情况下的反应速率分别为:
①v(A)=0.4 mol·L-1·min-1②v(B)=0.5 mol·L-1·s-1③v(C)=0.4 mol·L-1·s-1④v(D)=0.5 mol·L-1·s-1
下列有关反应速率的比较中,正确的是
A.③=②>④>①B.②=④>③=①C.①>②>③>④D.④>③>②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是( )
A.NaCl(aq)![]() NaHCO3(s)
NaHCO3(s)![]() Na2CO3
Na2CO3
B.Al(s)![]() Al2O3(s)
Al2O3(s)![]() Al(OH)3
Al(OH)3
C.AgNO3(aq)![]() [Ag(NH3)2]+(aq)
[Ag(NH3)2]+(aq)![]() Ag(s)
Ag(s)
D.MgCO3(s)![]() MgCl2(aq)
MgCl2(aq)![]() Mg(s)
Mg(s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中装置通过控制开关连接K1或K2,可利用太阳能电池电解水制高纯氢。下列说法错误的是( )
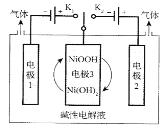
A.制H2时,连接K1
B.制O2时,电极3的反应式:NiOOH+H2O+e-=Ni(OH)2+OH-
C.交替连接K1和K2,可使电极3得以循环使用
D.上述过程,若用酸性电解质一样可以实现上述过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组研究温度对化学反应H2(g)+I2(g)![]() 2HI(g)的影响,在其他条件相同时,将1molH2(g)、1molI2(g)充入体积为2L的恒容容器中,测得HI(g)的物质的量分数随时间(min)变化的实验数据如下:
2HI(g)的影响,在其他条件相同时,将1molH2(g)、1molI2(g)充入体积为2L的恒容容器中,测得HI(g)的物质的量分数随时间(min)变化的实验数据如下:
时间 | 0 | 20 | 40 | 60 | 80 | 100 | |
HI(g)的物质 的量分数 | T1 | 0 | 0.50 | 0.68 | 0.76 | 0.80 | 0.80 |
T2 | 0 | 0.60 | 0.72 | 0.75 | 0.75 | 0.75 | |
下列说法正确的是( )
A.T1温度下,0~20min之间,H2的平均反应速率为0.025mol·L-1·min-1
B.在T1温度下,该反应有可能在70min时已达到平衡状态
C.T2温度下,20min时的正反应速率大于40min时的逆反应速率
D.由表中数据可知,温度越高,H2(g)与I2(g)的反应限度越大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学在日常生活中用途广泛,甲是原电池装置,电池总反应为Mg+C1O-+H2O=C1-+Mg(OH)2,乙是电解池装置用于含Cr2O72-的工业废水的处理。下列说法错误的是

A.甲中负极发生的电极反应为Mg一2e-=Mg2+
B.乙中惰性电极作阴极
C.乙中Cr2O72-向惰性电极移动
D.当消耗3.6g镁时,理论上也消耗8.4g铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.标准状况下,22.4L甲酸中含有的氧原子数为2.0NA
B.1mol乙醇在O2中完全燃烧,电子转移数目为6NA
C.室温下,26.0g乙炔和苯乙烯的混合物中含有的碳、氢原子数目的和为2NA
D.常温下a g某烷烃(CnH2n+2)中含有共用电子对数目为![]() NA
NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com