
【题目】根据反应:2Fe+3Cl2 ![]() 2FeCl3 , 当28gFe在71gCl2中点燃时( )
2FeCl3 , 当28gFe在71gCl2中点燃时( )
A.Fe和Cl2恰好完全反应
B.生成99gFeCl3
C.会有9.33gFe过量
D.会有17.75gCl2过量
科目:高中化学 来源: 题型:
【题目】化合物X是一种有机合成中间体,Z是常见的高分子化合物,某研究小组采用如下路线合成X和Z: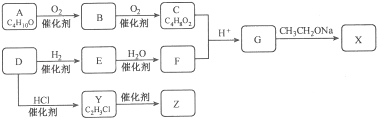
已知:①化合物A的结构中有2个甲基
②RCOOR′+R″CH2COOR′ ![]()
![]()
请回答:
(1)写出化合物E的结构简式 , F中官能团的名称是;
(2)Y→Z的化学方程式是;
(3)G→X的化学方程式是 , 反应类型是;
(4)若C中混有B,请用化学方法检验B的存在(要求写出操作、现象和结论) .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是现代光学及光纤制品的基本原料,它能被NaOH溶液或氢氟酸腐蚀.A与NaOH溶液反应生成B和水,B的焰色反应呈黄色,若向B的水溶液中滴加稀盐酸能生成一种胶体D.请回答下列问题:
(1)A的化学式是 .
(2)B的水溶液俗称 .
(3)A与氢氟酸反应的化学方程式是 .
(4)B与稀盐酸反应的离子方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为元素周期表的一部分,X,Y,W,Z均为短周期元素,其中只有X为金属元素.下列说法错误的是( ) ![]()
A.原子半径:Z<W<Y<X
B.元素Y的氧化物能与NaOH溶液反应
C.最简单气态氢化物的热稳定性:Y<X
D.W,Z的氧化物都能与碱反应生成盐和水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铜矿(CuFeS2)是炼钢和炼铜的主要原料,在高温下灼烧生成三氧化二铁和氧化亚铜.三氧化二铁和氧化亚铜都是红色粉末,常用作颜料.某学校化学兴趣小组通过实验来探究﹣红色粉末是Fe2O3、Cu2O或两者的混合物,探究过程如下:[查阅资料]Cu2O溶于稀硫酸生成Cu和CuSO4 , 在空气中加热生成CuO.
[提出假设]假设1:红色粉末是Fe2O3 .
假设2:红色粉末是Cu2O.
假设3:红色粉末是Fe2O3和Cu2O的混合物.
[提出探究实验]取少量粉末放入足量稀硫酸中,在所得溶液中再滴加KSCN试剂.
(1)若假设1成立,则实验现象是 .
(2)滴加KSCN试剂后溶液不变红色,某同学认为原固体粉末中一定不含三氧化二铁,你认为这种说法合理吗? . 简述你的理由(不需要写出反应的化学方程式) .
(3)若固体粉末完全溶液无固体存在,滴加KSCN试剂时溶液不变红色,则证明原固体粉末是 , 写出发生的氧化还原反应的离子方程式: .
(4)[探究延伸]经试验分析,确定红色粉末为Fe2O3和Cu2O的混合物.实验小组称取3.04g该红色粉末,设计如下实验方案进行实验.经查资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:
物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
开始沉淀时的pH | 6.0 | 7.5 | 1.4 |
沉淀完全时的pH | 13 | 14 | 3.7 |
步骤Ⅰ:将3.04g红色粉末溶于足量稀硫酸中,再加入足量H2O2溶液,振荡,得澄清透明溶液X.
步骤Ⅱ:在溶液X中加入适量Cu(OH)2粉末,调节溶液pH=4.0,过滤,得红褐色沉淀Y和滤液Z.
步骤Ⅲ:将沉淀Y充分灼烧,得1.6g红色固体M.
步骤Ⅳ:将滤液Z蒸发浓缩,冷却结晶,过滤,得6.0gCuSO45H2O晶体.
①沉淀Y的化学式为 .
②步骤Ⅳ中不需要用到的实验仪器 .
a.烧杯b.玻璃棒c.分液漏斗d.酒精灯e.铁架台(带铁圈)f.托盘天平g.量筒h.蒸发皿i.容量瓶.
③红色粉末样品中Cu2O的质量分数为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨的合成是一项重要的化工生产.已知合成氨有关能量变化的图象如图1.
(1)反应N2(g)+3H2(g) ![]() 2NH3(g)△H=KJ/mol;
2NH3(g)△H=KJ/mol;
(2)已知键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.
化学键 | H﹣H | N﹣H | N≡N |
键能/kJmol﹣1 | 436 | X | 946 |
则表中X的值是 .
(3)在一定条件下按图2实线I进行,改变某条件按图2虚线II进行,则该条件可能是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下,0.1molL﹣1的HA溶液中 ![]() =1×10﹣8 , 下列叙述中正确的是( )
=1×10﹣8 , 下列叙述中正确的是( )
A.0.01 molL﹣1HA的溶液中 c(H+)=l×l0﹣4molL﹣1
B.pH=3的HA溶液与pH=ll的NaOH溶液等体积混合后所得溶液中:c(Na+)=c(A﹣)>c(OH﹣)=c(H+)
C.浓度均为0.1 molL﹣1的HA溶液和NaA溶液等体积混合后所得溶液显酸性,则c(H+)﹣c(OH﹣)>c(A﹣)﹣c(HA)
D.pH=3的HA溶液与pH=11的NaOH溶液混合后所得溶液显碱性,则 c(Na+)>c(A﹣)>c(OH﹣)><c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学用语表述正确的是( )
A.质量数为16的氧原子: ![]() O
O
B.漂白粉的有效成分:NaClO
C.Mg2+结构示意图: ![]()
D.钠在氧气中燃烧的化学方程式:4Na+O2 ![]() 2Na2O
2Na2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列材料说法不正确是( )
序号 | 材料 | 类别 | 性能 | 用途 |
A | 钛合金 | 金属材料 | 密度小,强度高 | 制飞机机翼 |
B | 普通玻璃 | 硅酸盐材料 | 熔点高,透明 | 制试管、烧杯 |
C | 压电陶瓷 | 半导体材料 | 具有压电效应 | 声纳、地震仪 |
D | 氮化硅陶瓷 | 新型无机非金属材料 | 硬度高,耐磨 | 制发动机 |
A. AB. BC. CD. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com