
【题目】结合下图,分析下列叙述中,正确的是( )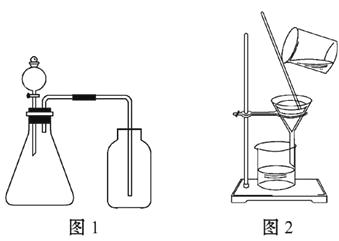
A.图1所示装置可用于分别制取少量NO和H2
B.图1所示装置可用于验证氧化性:KMnO4>Cl2
C.洗涤沉淀时(见图2),向漏斗中加适量水,搅拌并滤干
D.利用图2所示的方法可以提纯精制氢氧化铁胶体
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】化学与生活、社会密切相关,下列说法不正确的是
A.医院常用75%的酒精作消毒剂
B.通信光缆的主要成分是晶体硅,太阳能电池的材料主要是SiO2
C.氯气、臭氧、高铁酸钾都是常用的自来水消毒剂
D.活性铁粉可用作抗氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知钙的活动性介于钠和钾之间(钙的密度为1.54克/厘米3),下列叙述正确的是
A.少量的钙储存在煤油B.氧化性:K+>Ca2+>Na+
C.钙可以从K2SO4溶液中置换出钾D.钙与水反应生成氢氧化钙和氧气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与环境保护、社会可持续发展密切相关,下列说法或做法合理的是( )
A. 将地沟油回收加工为生物柴油,提高资源的利用率
B. 进口国外电子垃圾,回收其中的贵重金属
C. 洗衣粉中添加三聚磷酸钠,增强去污效果
D. 大量生产超薄塑料袋,方便人们的日常生活
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,浓度均为1.0molL﹣1的NH3H2O和NH4Cl混合溶液10mL,测得其pH为9.3.下列有关叙述正确的是( )
A.加入适量的NaCl,可使c(NH4+)=c(Cl﹣)
B.滴加几滴浓氨水,c(NH4+)减小
C.滴加几滴浓盐酸, ![]() 的值减小
的值减小
D.1.0 molL﹣1的NH4Cl溶液中c(NH4+)比该混合溶液大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】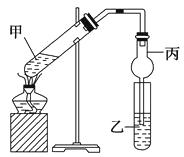
如图在试管甲中先加入2 mL95%的乙醇,并在振荡下缓慢加入2 mL浓硫酸,充分摇匀,冷却后再加入2 g无水乙酸钠(CH3COONa)。将试管甲固定在铁架台上,在试管乙中加入5 mL饱和碳酸钠溶液,按图连接好装置进行实验,当试管乙中有明显现象时停止实验。
试回答:
(1)实验时,应对试管甲缓慢加热,其目的是。
(2)写出试管甲中发生反应的化学方程式:。
(3)加入浓硫酸的作用是、、。
(4)该实验中球形管丙的作用是。
(5)某同学做此实验时,观察到反应混合液变黑,并闻到刺激性气味,试分析其原因:。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.常温下,在0.1molL﹣1的HNO3溶液中,由水电离出的c(H+)< ![]()
B.浓度为0.1molL﹣1的NaHCO3溶液:c(H2CO3)>c(CO32﹣)
C.25℃时,AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶度积相同
D.冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据《天工开物》记载我国古代以炉甘石(主要成分是ZnCO3)来升炼倭铅(即锌),其原理如图2。已知锌的熔点420℃、沸点906℃。则下列说法不正确的是
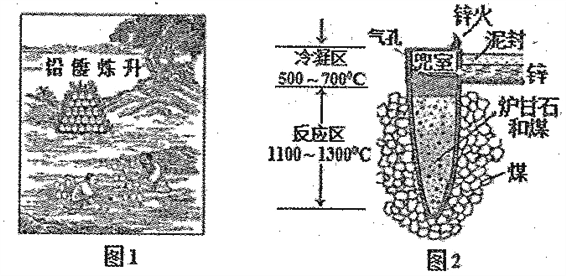
A. 升炼佞铅过程包含氧化还原反应
B. “锌火”是锌蒸气和-氧化碳在空气的燃烧
C. “泥封”的目的是为了防止得到的锌被氧化
D. 冶炼时锌变为蒸气在兜室冷凝为固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组准备在实验室配制95mL1.0mol/L的硝酸溶液,然后再研究金属铜与硝酸的反应情况。
(1)配制95mL1.0mol/L的硝酸溶液,需要的仪器除烧杯、玻璃棒、量筒、胶头滴管外,还需要的玻璃仪器是_____________。
(2)若用10mol/L的浓硝酸来配制上述溶液,需要量取浓硝酸的体积是_________mL。
(3)配制过程中,下列操作会引起浓度偏小的是________。
A,.定容摇勾后发现液面低于刻度线,再加水至刻度线
B.定容时俯视容量瓶的刻度线
C.将溶液转入容量瓶后,没有洗涤烧杯和玻璃棒,就进行定容操作
D.容量瓶用蒸馏水洗涤后未烘干
E.量取浓硝酸后,用少量蒸馏水洗涤量筒并将洗涤液也放入烧杯
(4)课外小组同学将制得的硝酸与铜片在下列装置中反应,反应初期观察到大试管中的液体a逐渐变为蓝色,试管上方有浅红棕色气体出现。
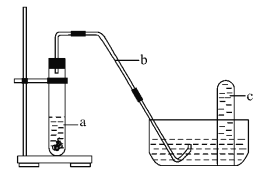
①反应初期液体a逐渐变为蓝色是由于反应生成了_________(填化学式)。
②请解释反应初期试管上方有浅红棕色气体出现的理由_________ (结合化学方程式说明)。
③导致红棕色气体在试管c中颜色消失的反应方程式为_________。
【答案】 100mL容量瓶 10.0 AC Cu(NO3)2 装置中有空气,将NO气体氧化为红棕色的NO2 气体,2NO+O2 = 2NO2 3NO2+H2O = 2HNO3+NO
【解析】(1)实验室没有95mL规格的容量瓶,必须配制100mL,配制100mL1.0molL-1的硝酸溶液步骤为:计算、称量、溶解冷却、移液、洗涤、定容、摇匀、装瓶,用到的玻璃仪器有:烧杯、玻璃棒、100ml容量瓶、胶头滴管,所以需要的玻璃仪器是:100mL容量瓶;(2)配制100mL1.0molL-1的硝酸溶液,设需要10molL-1的浓硝酸体积为V,则依据溶液稀释过程中溶质的物质的量不变得:100mL×1.0molL-1=10molL-1×V,解得V=10mL;(3)A.定容摇匀后发现液面低于刻度线,再加水至刻度线,导致溶液体积偏大,溶液浓度偏低,选项A选;B.定容时俯视容量瓶的刻度线,导致溶液体积偏小,溶液浓度偏低,选项B不选;
C.将溶液转入容量瓶后,没有洗涤烧杯和玻璃棒,就进行定容操作,导致部分溶质损耗,溶质的物质的量偏小,溶液浓度偏低,选项C选;D.容量瓶用蒸馏水洗涤后未烘干,对溶质的物质的量和溶液体积都不产生影响,溶液浓度不变,选项D不选;E.量取浓硝酸后,用少量蒸馏水洗涤量筒并将洗涤液也放入烧杯,则相当于所量硝酸偏多,导致所配溶液浓度偏大,选项E不选。答案选AC;(4)①铜与硝酸反应生成硝酸铜,化学式为Cu(NO3)2;②装置中有空气,将NO气体氧化为红棕色的NO2 气体,2NO+O2 = 2NO2,即使开始没有NO2而只有NO气体也可能变成红棕色,反应初期试管上方有浅红棕色气体出现;
③二氧化氮能够与水反应生成硝酸和一氧化氮,反应方程式:3NO2+H2O = 2HNO3+NO,所以红棕色气体在试管c中颜色消失。
点睛:本题考查了一定物质的量浓度溶液的配制及硝酸性质探究,明确配制原理及操作步骤,熟悉硝酸的性质是解题关键,易错点为(4)①铜与硝酸反应生成硝酸铜,硝酸铜为蓝色溶液;②依据一氧化氮能够与空气中氧气反应生成二氧化氮解答;③依据二氧化氮能够与水反应生成硝酸和一氧化氮解答。
【题型】综合题
【结束】
29
【题目】某废水中含有CN-和Cr2O72-等离子,需经污水处理达标后小能排放,污水处理拟采用下列流程进行处理:
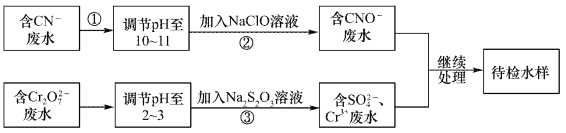
回答下列问题:
(1)步骤②中,CN-被ClO-氧化为CNO-的离子方程式为____________。
(2)步骤③的反应的离了方程式为S2O32-+Cr2O72-+H+→SO42-+Cr3++H2O(未配平),每消耗0.4mol Cr2O72-时,反应中S2O32-失去_________mol电子。
(3)含Cr3+废水可以加入熟石灰进一步处理,目的是___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com