
،¾جâؤ؟،؟دضسذ73gآب»¯ا⣨HCl£©ئّجه£¬شٍ£؛
£¨1£©¸أئّجهµؤؤ¦¶ûضتء؟خھ_____________،£
£¨2£©¸أئّجهµؤخïضتµؤء؟خھ________ £¬ثù؛¬·ض×س×ـتخھ___________________¸ِ،£
£¨3£©¸أئّجهشع±ê×¼×´؟ِدآµؤجه»خھ_____________L،£
£¨4£©½«73gآب»¯ا⣨HCl£©ئّجهبـسعث®إن³ة2Lبـز؛£¬ثùµأرخثلµؤخïضتµؤء؟إ¨¶بخھ__________،£
£¨5£©شع±ê×¼×´؟ِدآ£¬²âµأ1.92gؤ³ئّجهµؤجه»خھ672ml£¬¼ئثم´ثئّجهµؤدà¶ش·ض×سضتء؟__________،£
£¨6£©N2،¢CO2،¢SO2بضضئّجهµؤضتء؟±بخھ7£؛11£؛16ت±£¬ثüأاµؤ·ض×س¸ِت±بخھ_______£¬ح¬خآح¬ر¹دآجه»±بخھ___________،£
،¾´ً°¸،؟36.5g/mol2 mol2NA(1.204![]() 1024)44.81mol/L641£؛1£؛11£؛1:1
1024)44.81mol/L641£؛1£؛11£؛1:1
،¾½âخِ،؟
£¨1£©HClئّجهµؤدà¶ش·ض×سضتء؟تا36.5£¬شٍ¸أئّجهµؤؤ¦¶ûضتء؟خھ36.5g£¯mol£»
£¨2£©¸ù¾فn£½![]() ؟ةضھ¸أئّجهµؤخïضتµؤء؟خھ
؟ةضھ¸أئّجهµؤخïضتµؤء؟خھ![]() £½2mol£¬ثù؛¬·ض×س×ـتخھ2NA¸ِ£»
£½2mol£¬ثù؛¬·ض×س×ـتخھ2NA¸ِ£»
(3£©×¼×´؟ِدآئّجهµؤؤ¦¶ûجه»تا22£®4L/mol£¬ثùزش¸أئّجهشع±ê×¼×´›rدآµؤجه»خھ2mol،ء22.4L/mol£½44.8L£»
£¨4£©½«73gآب»¯ا⣨HCl£©ئّجهµؤخïضتµؤء؟خھ2mol£¬بـسعث®إن³ة2Lبـز؛£¬ثùµأرخثلµؤخïضتµؤء؟إ¨¶بخھ![]() £»
£»
£¨5£©شع±ê×¼×´›rدآ£¬²âµأ1.92gؤ³ئّجهµؤجه»خھ672mL£¬خïضتµؤء؟تا![]() £½0.03mol£¬ثùزش´ثئّجهµؤدà¶ش·ض×سضتء؟خھ
£½0.03mol£¬ثùزش´ثئّجهµؤدà¶ش·ض×سضتء؟خھ![]() £½64£»
£½64£»
£¨6£©N2،¢CO2،¢SO2بضضئّجهµؤضتء؟±بخھ7£؛11£؛16ت±£¬ثüأاµؤ·ض×س¸ِت±بخھ£؛![]() £½1£؛1£؛1£¬شٍخïضتµؤء؟ض®±بخھ1£؛1£؛1£¬ح¬خآح¬ر¹دآجه»±بخھ1£؛1£؛1،£
£½1£؛1£؛1£¬شٍخïضتµؤء؟ض®±بخھ1£؛1£؛1£¬ح¬خآح¬ر¹دآجه»±بخھ1£؛1£؛1،£



| ؤ꼶 | ¸كضذ؟خ³ج | ؤ꼶 | ³ُضذ؟خ³ج |
| ¸كز» | ¸كز»أâ·ر؟خ³جحئ¼ِ£، | ³ُز» | ³ُز»أâ·ر؟خ³جحئ¼ِ£، |
| ¸ك¶ | ¸ك¶أâ·ر؟خ³جحئ¼ِ£، | ³ُ¶ | ³ُ¶أâ·ر؟خ³جحئ¼ِ£، |
| ¸كب | ¸كبأâ·ر؟خ³جحئ¼ِ£، | ³ُب | ³ُبأâ·ر؟خ³جحئ¼ِ£، |
؟ئؤ؟£؛¸كضذ»¯ر§ ہ´ش´£؛ جâذح£؛
،¾جâؤ؟،؟NA´ْ±ي°¢·ü¼سµآآق³£ت£¬دآءذثµ·¨صب·µؤتا
A. 9gD2Oضذ؛¬سذµؤµç×ستخھ5NA
B. اâرُ»¯جْ½؛جه´ّصµç؛ة،£سأ؛¬0.1molµؤFeCl3بـز؛ضئ³ةµؤاâرُ»¯جْ½؛جهضذ£¬½؛ء£تذ،سع0.1NA
C. ³£خآدآ£¬7.8gNa2O2سë100mL0.05mol/LµؤHClبـز؛·´س¦£¬²ْةْµؤئّجهجه»´َسع1120mL
D. 0.1mol/LNa2CO3بـز؛ضذ:H2CO3،¢CO32-،¢HCO3-خïضتµؤء؟ض®؛حخھ0.1NA
²é؟´´ً°¸؛ح½âخِ>>
؟ئؤ؟£؛¸كضذ»¯ر§ ہ´ش´£؛ جâذح£؛
،¾جâؤ؟،؟شعخز¹ْµؤ×تش´´¢±¸ضذ£¬¸ُتاضطزھµؤص½آش½ًتô×تش´،£زشدآتازشؤ³¸ُشü£¨ض÷زھ³ة·ضخھCr2O3£¬شسضتض÷زھتاFeO،¢SiO2µب£©خھشءدةْ²ْCr2O3µؤ¹¤زصء÷³ج£؛
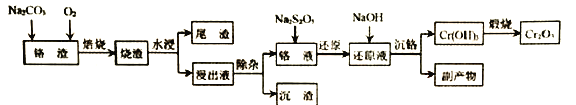
زرضھ£؛Ksp[Mg(OH)2]£½1.2،ء10£11£¬Ksp [Cr(OH)3]£½6.4،ء10£31
£¨1£©بôزشرُ»¯خïذخت½±يت¾؟َخïµؤ×é³ة£¬Fe2SiO4؟ة±يت¾خھ______،£
£¨2£©±؛ةصت±ح¨بëرُئّµؤ×÷سأتا ______،£
£¨3£©،°³شس،±ت±¼سبëMgSO4-(NH4)2SO4»ى؛دخïسëبـز؛ضذةظء؟µؤPO43£ ،¢AsO43£ ،¢SiO32£·´س¦£¬·ض±ً×ھ»¯خھNH4MgPO4،¢NH4MgAsO4،¢MgSiO3³ءµي³ب¥،£
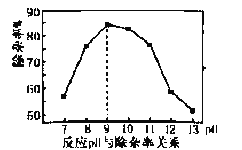
¢ظ·´س¦¹³ج؟طضئبـز؛pHخھ9£¬بôpH£¾9³شسآت½µµحµؤشزٍتا ______،£
¢ع·´س¦µؤخآ¶ب؟طضئشع80،و×َسز£¬خآ¶ب²»زثج«¸كµؤض÷زھشزٍتا_______،£
£¨4£©،°»¹ش،±ت±دبµ÷½عبـز؛pH£¬شظ¼سبë½¹راءٍثلؤئ£¨Na2S2O5£©
¢ظحê³ة،°»¹ش،±·´س¦µؤہë×س·½³جت½£؛_____________
![]()
¢عزرضھ¸ُز؛ضذc(Cr2O72£ )£½0.32 mol/L £¬خھءث²»ت¹»¹ش¹³ج²ْةْCr(OH)3³ءµي£¬س¦ ؟طضئ·´س¦¹³جpH²»´َسع _____،£
£¨5£©،°³ء¸ُ،±ض÷زھ¸±²ْخïخھ______،£
²é؟´´ً°¸؛ح½âخِ>>
؟ئؤ؟£؛¸كضذ»¯ر§ ہ´ش´£؛ جâذح£؛
،¾جâؤ؟،؟ؤ³¹ججه»ى؛دخïX؟ةؤـتاسةNa2SiO3،¢Fe،¢Na2CO3،¢ BaCl2ضذµؤء½ضض»ٍء½ضضزشةدµؤخïضت×é³ة،£ؤ³ذثب¤ذ،×éخھج½¾؟¸أ¹ججه»ى؛دخïµؤ×é³ة£¬ةè¼ئتµرé·½°¸بçدآح¼ثùت¾£¨ثù¼ستش¼ء¾ù¹ء؟£©،£

دآءذثµ·¨²»صب·µؤتا£؛
A. ئّجهAز»¶¨تا»ى؛دئّجه
B. ³ءµيAز»¶¨تاH2SiO3
C. °×ة«³ءµيBشع؟صئّضذضً½¥±ن»زآجة«£¬×î؛َ±ن؛ى؛ضة«
D. ¸أ¹ججه»ى؛دخïز»¶¨؛¬سذFe،¢Na2CO3،¢BaCl2
²é؟´´ً°¸؛ح½âخِ>>
؟ئؤ؟£؛¸كضذ»¯ر§ ہ´ش´£؛ جâذح£؛
،¾جâؤ؟،؟دآءذبـز؛ضذ¸÷خ¢ء£µؤإ¨¶ب¹طدµصب·µؤتا£¨ £©
A. 0.1mol،¤L-1Na2Sبـز؛ضذ£؛2[Na+]=[S2-]+[HS-]+[H2S]
B. 0.1mol،¤L-1NaHSO4بـز؛ضذ£؛[Na+]>[SO42-]>[H+]>[OH-]
C. Na2C2O4بـز؛£؛c(OH-)=c(H+)+c(HC2O4)+2c(H2C2O4)
D. CH3COONa؛حCaCl2»ى؛دبـز؛£؛c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-)
²é؟´´ً°¸؛ح½âخِ>>
؟ئؤ؟£؛¸كضذ»¯ر§ ہ´ش´£؛ جâذح£؛
،¾جâؤ؟،؟ؤـسأH++OH©پ=H2Oہ´±يت¾µؤ»¯ر§·´س¦تا£¨ £©
A.اâرُ»¯أ¾؛حد،رخثل·´س¦
B.Ba£¨OH£©2بـز؛µخبëد،ءٍثلضذ
C.³خاهت¯»زث®؛حد،دُثل·´س¦
D.¶رُ»¯ج¼ح¨بë³خاهت¯»زث®ضذ
²é؟´´ً°¸؛ح½âخِ>>
؟ئؤ؟£؛¸كضذ»¯ر§ ہ´ش´£؛ جâذح£؛
،¾جâؤ؟،؟ؤ³خآ¶بدآشع؛مبفأـ±صبفئ÷ضذ·¢ةْبçدآ·´س¦£؛2M(g)+N(g)![]() 2E(g),بô؟ھت¼ت±ض»³نبë2molE(g)£¬´ïئ½؛âت±£¬»ى؛دئّجهµؤر¹ا؟±بئًت¼ت±شِ´َءث20%£»بô؟ھت¼ت±ض»³نبë2molM؛ح1molNµؤ»ى؛دئّجه£¬´ïئ½؛âت±Mµؤ×ھ»¯آتخھ
2E(g),بô؟ھت¼ت±ض»³نبë2molE(g)£¬´ïئ½؛âت±£¬»ى؛دئّجهµؤر¹ا؟±بئًت¼ت±شِ´َءث20%£»بô؟ھت¼ت±ض»³نبë2molM؛ح1molNµؤ»ى؛دئّجه£¬´ïئ½؛âت±Mµؤ×ھ»¯آتخھ
A. 20% B. 40% C. 60% D. 80%
²é؟´´ً°¸؛ح½âخِ>>
؟ئؤ؟£؛¸كضذ»¯ر§ ہ´ش´£؛ جâذح£؛
،¾جâؤ؟،؟°±»ù»اثلؤّ[Ni(H2NSO3)2]تا¹¤زµµç¶ئؤّثù±طذèµؤ»¯¹¤شءد£¬ؤ³؟ئرذذ،×éدبسأؤٍثط،¢SO3؛د³ةضذ¼نجه°±»ù»اثل(H2NSO3H)£¬شظسأ°±»ù»اثل،¢½ًتôؤّ؛حث«رُث®·´س¦ہ´؛د³ة°±»ù»اثلؤّ،£زرضھ»ا»¯ضئ°±»ù»اثل·´س¦شہي؛حصû¸ِ¹³جµؤء÷³جح¼بçدآ£؛
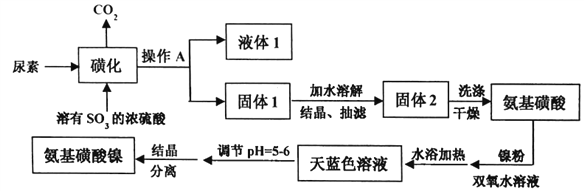
¢ظCO(NH2)2(s)+SO3(g)،ْH2NCONHSO3H(s) ،÷H<0
¢عH2NCONHSO3H (s)+ H2SO4،ْ2H2NSO3H (s)+ CO2،ü
زرضھخïضتµؤ²؟·ضذشضتبçدآ£؛
خïضت | بـ½âذش | خب¶¨ذش | ثل¼îذش |
°±»ù»اثل | بـسعث®،¢²»بـسعزز´¼ | pH½دµحت±·¢ةْث®½âةْ³ةNH4HSO4 | ا؟ثلذش |
°±»ù»اثلؤّ | بـسعث®،¢زز´¼ | ¸كسع110،وت±·ض½â | ثلذش |
اë»ط´ً
(1)²ظ×÷Aµؤأû³ئتا_________ز؛جه1µؤض÷زھ³ة·ضتا_______£¨جر§ت½£©،£
(2)،°»ا»¯،±¹³جµؤخآ¶بسë²ْآتµؤ¹طدµبçدآح¼،£خآ¶ب¸كسع80،وت±°±»ù»اثلµؤ²ْآت»ل½µµح£¬شزٍز»تاة¸كخآ¶بئ½؛âؤودٍزئ¶¯£¬شزٍ¶تا__________،£
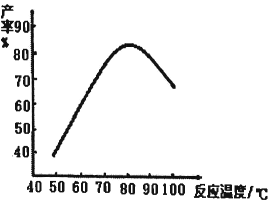
(3)ذ´³ِضئ±¸°±»ù»اثلؤّµؤ»¯ر§·½³جت½____________________،£
(4)ذ´³ِ¹ججه2د´µسµؤ²ظ×÷¹³ج___________________،£
(5)ء÷³جح¼ضذ،°جىہ¶ة«بـز؛،±ذèزھµ÷½عpH=5~6µؤشزٍتا___________،£
²é؟´´ً°¸؛ح½âخِ>>
؟ئؤ؟£؛¸كضذ»¯ر§ ہ´ش´£؛ جâذح£؛
،¾جâؤ؟،؟µç½âشہيشع»¯ر§¹¤زµضذسذ¹م·؛س¦سأ،£سزح¼±يت¾ز»¸ِµç½â³ط£¬×°سذµç½âز؛a£»X،¢Yتاء½؟éµç¼«°ه£¬ح¨¹µ¼دكسëض±ء÷µçش´دàء¬،£اë»ط´ًزشدآختجâ£؛

£¨1£©بôX،¢Y¶¼تا¶èذشµç¼«£¬aتا±¥؛حNaClبـز؛£¬تµرé؟ھت¼ت±£¬ح¬ت±شعء½±ك¸÷µخب뼸µخ·سجھتشز؛£¬شٍ
¢ظµç½â³طضذX¼«ةدµؤµç¼«·´س¦تا______________،£شعX¼«¸½½ü¹غ²ىµ½µؤدضدَتا______________________________،£
¢عYµç¼«ةدµؤµç¼«·´س¦ت½تا______________،£¼ىرé¸أµç¼«·´س¦²ْخïµؤ·½·¨تا______________،£
£¨2£©بçزھسأµç½â·½·¨¾«ء¶´ضح£¬µç½âز؛aر،سأCuSO4بـز؛£¬شٍ
¢ظXµç¼«µؤ²ؤءدتا___________________£¬µç¼«·´س¦ت½تا______________،£
¢عYµç¼«µؤ²ؤءدتا___________________£¬µç¼«·´س¦ت½تا______________،£
£¨ثµأ÷£؛شسضت·¢ةْµؤµç¼«·´س¦²»±طذ´³ِ£©
¢غ¼ظبôµçآ·ضذسذ0.04ؤ¦¶ûµç×سح¨¹ت±£¬زُ¼«شِضط________؟ث،£
²é؟´´ً°¸؛ح½âخِ>>
¹ْ¼تر§ذ£سإر، - ء·د°²لءذ±ي - تشجâءذ±ي
؛±±ت،»¥ءھحّخ¥·¨؛ح²»ء¼ذإد¢¾ظ±¨ئ½ج¨ | حّةدسذ؛¦ذإد¢¾ظ±¨×¨اّ | µçذإص©ئ¾ظ±¨×¨اّ | ةوہْت·ذéخقض÷زهسذ؛¦ذإد¢¾ظ±¨×¨اّ | ةوئَاضب¨¾ظ±¨×¨اّ
خ¥·¨؛ح²»ء¼ذإد¢¾ظ±¨µç»°£؛027-86699610 ¾ظ±¨ستدن£؛58377363@163.com