
【题目】某固体混合物X可能是由Na2SiO3、Fe、Na2CO3、 BaCl2中的两种或两种以上的物质组成。某兴趣小组为探究该固体混合物的组成,设计实验方案如下图所示(所加试剂均过量)。

下列说法不正确的是:
A. 气体A一定是混合气体
B. 沉淀A一定是H2SiO3
C. 白色沉淀B在空气中逐渐变灰绿色,最后变红褐色
D. 该固体混合物一定含有Fe、Na2CO3、BaCl2
【答案】D
【解析】固体混合物可能由Na2SiO3、Fe、Na2CO3、BaCl2中的两种或两种以上的物质组成,由实验可知,气体A与与澄清的石灰水反应,溶液变浑浊,则A中一定含CO2;混合物与足量稀盐酸反应后的沉淀A为H2SiO3。溶液A与NaOH反应后生成白色沉淀B,则B为Fe(OH)2,溶液B与硝酸、硝酸银反应生成沉淀C为AgCl,则原混合物中一定含有Fe、Na2CO3、Na2SiO3,可能含有BaCl2。根据以上分析可以解答下列问题。A. 稀盐酸与Na2CO3反应生成CO2气体,与Fe反应生成H2,气体A是CO2与H2的混合气体,A正确;B. 沉淀A为H2SiO3沉淀,B正确;C. B为Fe(OH)2 ,在空气中被氧气氧化,逐渐变灰绿色,最后变红褐色,C正确;D. 该固体混合物中可能含有BaCl2,D错误。答案选D.


 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源: 题型:
【题目】有机物F(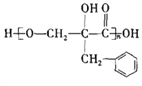 )为一种高分子树脂,其合成路线如下:
)为一种高分子树脂,其合成路线如下:
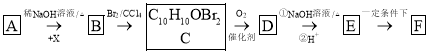
已知:①A为苯甲醛的同系物,分子中无甲基,其相对分子质量为134;
②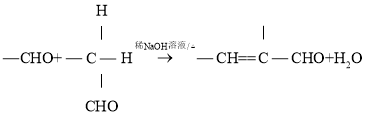
请回答下列问题:
(1)X的化学名称是__________。
(2)B生成C的反应类型为__________。
(3)E的结构简式为__________。
(4)由C生成D的化学方程式为____________________________________________________。
(5)芳香族化合物Y是D的同系物,Y的同分异构体能与饱和![]() 溶液反应放出气体,分子中只有1个侧链,核磁共振氢谱显示有5种不同化学环境的氢,峰面积比为6:2:2:1:1.写出两种符合要求的Y的结构简式:__________、__________。
溶液反应放出气体,分子中只有1个侧链,核磁共振氢谱显示有5种不同化学环境的氢,峰面积比为6:2:2:1:1.写出两种符合要求的Y的结构简式:__________、__________。
(6)写出以乙醛和乙二醇为主要原料合成高分子化合物(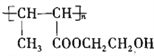 )的合成路线(无机试剂自选):__________________________________________________。
)的合成路线(无机试剂自选):__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以有机化合物A为初始原料,合成有机化合物C和F的路线如图所示:
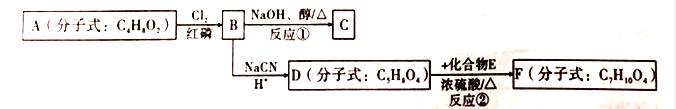
已知以下信息:
①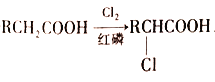 ,R-Cl
,R-Cl![]() R—COOH,其中R表示烃基;
R—COOH,其中R表示烃基;
②D的核磁共振氢谱有两种不同化学环境的氢;
③F为七元环状化合物。
回答下列问题:
(1)A中含有的官能团名称为________;1molA完全燃烧消耗O2________mol.
(2)判断反应类型:反应①为_________;反应②为_________。
(3)E的结构简式为_________;F的结构简式为_________。
(4)由B生成C的化学方程式为_________。
(5)请写出满足下列条件的D的2种链状同分异构体的结构简式: _________。
①可发生水解反应;②核磁共振氢谱显示有两组峰,且峰面积之比为1:3。
(6)利用该合成路线中的有关信息,写出以乙醇为初始原料,其他无机试剂任选,制备有机化合物CH2=CHCOOH的合成路线流程图:(流程图示例:CH3CH2OH![]() H2C=CH2
H2C=CH2![]() BrH2C—CH2Br)________________
BrH2C—CH2Br)________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓度为0.50mol/L的某金属阳离子Mn+的溶液10.00mL,与0.80mol/L的NaOH溶液12.50mL完全反应,生成沉淀,则n等于( )
A.1
B.2
C.3
D.4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学帮助水质检测站配制480mL 0.5mol·L-1 NaOH溶液以备使用。
(1).该同学应选择__________mL的容量瓶。
(1).其操作步骤如乙图所示,则甲图操作应在乙图中的__________(填选项字母)之间。
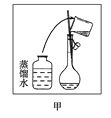
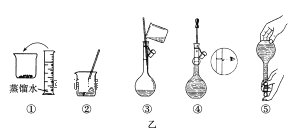
A.②与③B.①与②C.③与④
(1). 该同学应称取NaOH固体__________g,用质量为23.1g的烧杯放在托盘天平上称取所需NaOH固体时,请在附表中选取所需的砝码大小__________(填字母),并在如图中选出能正确表示游码位置的选项__________(填字母)。
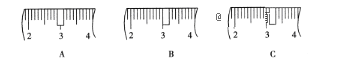
a | b | c | d | e | |
砝码大小/g | 100 | 50 | 20 | 10 | 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有73g氯化氢(HCl)气体,则:
(1)该气体的摩尔质量为_____________。
(2)该气体的物质的量为________ ,所含分子总数为___________________个。
(3)该气体在标准状况下的体积为_____________L。
(4)将73g氯化氢(HCl)气体溶于水配成2L溶液,所得盐酸的物质的量浓度为__________。
(5)在标准状况下,测得1.92g某气体的体积为672ml,计算此气体的相对分子质量__________。
(6)N2、CO2、SO2三种气体的质量比为7:11:16时,它们的分子个数比为_______,同温同压下体积比为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】侯氏制碱法制得的NaHCO3固体中含有部分Na2CO3·nH2O(n<10)。取该固体8.50g充分加热,产生的气体依次通过浓硫酸(增重1.44 g)和碱石灰(增重1.76 g)。
请计算:
(1)固体中NaHCO3的质量为_________g。
(2)固体中Na2CO3·nH2O的n值为 ___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com