
【题目】在25mL 0.1mol/L NaOH溶液中逐滴加入0.2mol/L CH3COOH溶液,曲线如图所示,下列有关离子浓度关系的比较,正确的是

A.在A、B间任一点,溶液中一定都有c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B.在B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
C.在C点:c(CH3COO-)>c(Na+)> c(OH—)>c(H+)
D.在D点:c(CH3COO-)+ c(CH3COOH)=2 c(Na+)
【答案】D
【解析】
A.在B点由于溶液的pH=7,所以c(OH-)=c(H+),结合电荷守恒可知:c(Na+)=c(CH3COO-)在A、B间任一点,由于溶液显碱性所以c(OH-)>c(H+)。根据电荷守恒可知:c(Na+)>c(CH3COO-),但是c(CH3COO-)和c(OH-)的浓度不容易比较大小,因此溶液中不一定都有c(Na+)>c(CH3COO-)> c(OH-) >c(H+),错误;
B.盐电离产生的离子浓度远大于水电离产生的离子的浓度,因此在B点,a>12.5,且有c(Na+)=c(CH3COO-) > c(OH-)=c(H+),错误。
C.在C点溶液显酸性,微粒间的关系是:c(CH3COO-) >c(Na+)>c(H+)> c(OH—),错误;
D.在D点n(CH3COOH)=2n(NaOH)。根据物料守恒可得:c(CH3COO-)+ c(CH3COOH)=2 c(Na+) ,正确。


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.1mol/L的![]() 溶液中含
溶液中含![]() 的数目为2NA
的数目为2NA
B.标准状况下,4.48L ![]() 中所含原子数目为0.2NA
中所含原子数目为0.2NA
C.常温常压下,28g ![]() 中所含分子数目为NA
中所含分子数目为NA
D.1mol Al与足量盐酸完全反应,转移电子数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温、恒容的密闭容器中进行反应 A(g)═B(g)+C(g),若反应物的浓度由2molL-1 降到 0.8molL-1 需要 20s,那么反应物浓度再由 0.8molL-1 降到 0.2molL-1 所需要的时间为
A.10sB.大于 10sC.小于 10sD.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化钠![]() 化合物中钠元素是
化合物中钠元素是![]() 价,NaH跟水反应放出
价,NaH跟水反应放出![]() ,下列叙述正确的是( )
,下列叙述正确的是( )
A.在NaH中的氢离子半径比锂离子半径大
B.在NaH中的氢离子的电子层排布与![]() 不相同
不相同
C.NaH跟水反应后溶液呈酸性
D.NaH中的氢离子被还原成氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸钠(Na2FeO4)的装置如右图所示。下列说法正确的是

A.铁是阳极,电极反应为Fe-2e-+2OH-![]() Fe(OH)2
Fe(OH)2
B.电解一段时间后,镍电极附近溶液的pH减小
C.若离子交换膜为阴离子交换膜,则电解结束后左侧溶液中含有FeO42-
D.每制得1mol Na2FeO4,理论上可以产生67.2L气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将KCl和CuSO4两种溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如图所示,则下列说法正确的是
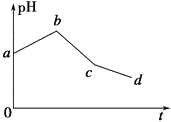
A.整个过程中两电极反应2Cl--2e-=Cl2↑、2H++2e-=H2↑不可能同时发生
B.电解至c点时,往电解液中加入适量CuCl2固体,即可使电解液恢复至原来的浓度
C.ab段表示电解过程中H+被还原,pH上升
D.原混合溶液中KCl和CuSO4的浓度之比恰好为2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果酸是一种常见的有机酸,结构简式为![]() 苹果酸可能发生的反应是( )
苹果酸可能发生的反应是( )
①与NaOH溶液反应 ②与石蕊试液作用变红
③等量的苹果酸与足量的Na、NaHCO3在相同条件下生成的气体一样多
④一定条件下与乙酸酯化 ⑤一定条件下与乙醇酯化
A.①②③B.①②④⑤
C.①②③⑤D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】830 K时,在密闭容器中发生下列可逆反应: CO(g)+H2O(g) ![]() CO2(g)+H2(g) ΔH<0 。请回答下列问题:
CO2(g)+H2(g) ΔH<0 。请回答下列问题:
(1)若起始时c(CO) =2 mol·L-1,c(H2O) =3 mol·L-1,4 s后达到平衡,此时CO的转化率为60%,则在该温度下,该反应的平衡常数K=____;用H2O表示的化学反应速率为_____。
(2)在相同温度下,若起始时c(CO) =1 mol·L-1,c(H2O) =2 mol·L-1,反应进行一段时间后,测得H2的浓度为0.5 mol·L-1,此时v(正)______ v(逆) (填“大于”“小于”或“等于”)。
(3)若降低温度,该反应的K值可能为______。
a.1 b.2 c.0.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化碘(ICl3)在药物合成中用途非常广泛,其熔点为33℃,沸点为73℃,氯气与单质碘需在温度稍低于70℃下反应制备ICl3。实验室可用如图装置制取ICl3。下列说法正确的是( )

A.装置A可选用的药品为二氧化锰与浓盐酸
B.装置B的作用是除杂,也作安全瓶,能监测实验进行时装置C中是否发生堵塞
C.装置C中的硅胶可用碱石灰代替
D.装置D最恰当的加热方式为酒精灯直接加热
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com