
【题目】下列金属冶炼的反应原理错误的是
A. 2NaCl(熔融)=== 2Na+Cl2↑B. Al2O3+ 3H2 ===2Al + 3H2O
C. Fe2O3 + 3CO === 2Fe + 3CO2D. ZnO + CO === Zn + CO2
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A.向硫酸酸化的FeSO4溶液中加入过量的H2O2溶液:2Fe2++H2O2+2H+═2Fe3++2H2O
B.用小苏打治疗胃酸过多:CO ![]() +2H+═CO2↑+H2O
+2H+═CO2↑+H2O
C.碳酸镁与盐酸反应:CO ![]() +2H+═CO2↑+H2O
+2H+═CO2↑+H2O
D.向Ca(HCO3)2溶液中加入过量的NaOH溶液:Ca2++HCO ![]() +OH﹣═CaCO3↓+H2O
+OH﹣═CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体氧化物燃料电池是以固体氧化锆﹣氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2﹣)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应,下列判断正确的是( ) 
A.有O2参加反应的a极为电池的负极
B.b极的电极反应式为H2+O2﹣﹣2e﹣═H2O
C.a极对应的电极反应式为O2+2H2O+4e﹣═4OH﹣
D.氧化锆的作用是让电子在电池内部通过
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数,下列叙述中正确的是( )
A.在25℃,1.01×105Pa时,11.2L氮气所含的原子数目为NA
B.48g O3 和O2混合气体所含的原子数目为3NA
C.1mol氦气所含的电子数目为4NA
D.2.7g金属铝变成铝离子时失去的电子数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于某酸的酸式盐NaHY的水溶液的下列叙述中,正确的是
A. 该酸式盐的水溶液一定显酸性
B. 在该盐溶液中,离子浓度为:c(Na+)>c(Y2-)>c(HY-)>c(OH-)>c(H+)
C. 若HY-能水解,水解方程式为:HY-+H2O![]() Y2-+H3O+
Y2-+H3O+
D. 若HY-能电离,电离方程式为:HY-+H2O![]() Y2-+H3O+
Y2-+H3O+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学通过查阅资料得知,可利用Na2SO3粉末与70%硫酸溶液在加热条件下反应来快速制取SO2。该同学设计了下图所示装置制取SO2并验证其性质。
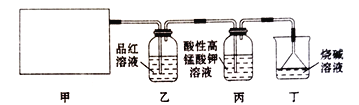
回答下列问题:
(1)根据资料中的相关信息,甲装置应选择下列装置中的____________(填序号)。

(2)实验过程中,丙装置中酸性高锰酸钾溶液紫红色褪去,说明SO2具有_________性,证明SO2具有漂白性的现象为___________________________________。
(3)丁装置的作用是____________,写出其中发生主要反应的化学方程式:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A.将NaHSO4与Ba(OH)2溶液混合至中性:2H++SO42﹣+Ba2++2OH﹣═BaSO4↓+2H2O
B.用惰性电极电解饱和食盐水:2Cl﹣+2H+ ![]() H2↑+C12↑
H2↑+C12↑
C.用氨水溶解氯化银沉淀:Ag++2 NH3?H2O=[Ag(NH3)2]++2H2O
D.盐酸中滴加氨水:H++OH﹣=H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】日本产业技术综合研究所最近研发了一种新型的锂空气电池,它既可用作充电电池又可作锂燃料电池.用作燃料电池时,可更换正极的水性电解液和卡盒以及负极的金属锂就可以连续使用,分离出的氢氧化锂可回收锂而循环使用.下列叙述不正确的是( ) 
A.放电时负极的电极反应式为:Li﹣e﹣=Li+
B.充电时,阳极的电极反应式为:2H2O+O2+4e﹣=4OH﹣
C.充电时,锂极与外电源的负极相连
D.熔融的氢氧化锂用惰性电极电解再生时,在阴极可得到金属锂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置所示的实验中,能达到实验目的是( )
A.![]() 从Mg(OH)2悬浊液中分离出Mg(OH)2
从Mg(OH)2悬浊液中分离出Mg(OH)2
B.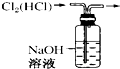 除去Cl2中的HCl
除去Cl2中的HCl
C.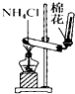 实验室制氨气
实验室制氨气
D. 排水法收集NO
排水法收集NO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com