
【题目】常温下,用0.10mol/L NaOH溶液滴定0.10mol/L HA溶液,滴定曲线如图a所示,混合溶液的pH与离子浓度变化的关系如图b所示,下列叙述错误的是

A. 当滴定至溶液呈中性时,c(A-)>c(HA)B. N点,c(Na+)·c(A-)=![]()
C. Ka(HA)的数量级为10-5D. P-Q过程中,水的电离程度逐渐增大
【答案】B
【解析】
A. lg![]() =0时,c(A-)=c(HA),此时pH<5,结合lg
=0时,c(A-)=c(HA),此时pH<5,结合lg![]() 为增函数分析。
为增函数分析。
B.N点pH=8.72,结合电荷守恒计算;
C. Q点lg![]() =1,pH约为5.8,结合Ka (HA)=
=1,pH约为5.8,结合Ka (HA)=![]() 计算;
计算;
D. P点lg![]() =-1,Q点lg
=-1,Q点lg![]() =1,c(A-)越大,水的电离程度越大。
=1,c(A-)越大,水的电离程度越大。
A.根据图象可知,lg![]() =0时,c(A-)=c(HA),此时pH<5,结合lg
=0时,c(A-)=c(HA),此时pH<5,结合lg![]() 为增函数,pH=7时,lg
为增函数,pH=7时,lg![]() >1,则c(A-)>c(HA),A正确;
>1,则c(A-)>c(HA),A正确;
B.N点pH=8.72,c(H+)=10-8.72mol/L,c(OH-)=![]() ,根据电荷守恒可知:c(Na+)-c(A-)=c(OH-)-c(H+)≈c(OH-)=
,根据电荷守恒可知:c(Na+)-c(A-)=c(OH-)-c(H+)≈c(OH-)=![]() ,B错误;
,B错误;
C.根据图a可知,Q点lg![]() =1,pH约为5.8,则c(H+)=10-5.8mol/L,K a (HA)=
=1,pH约为5.8,则c(H+)=10-5.8mol/L,K a (HA)=![]() 10c(H+)=10-4.8,所以,Ka (HA)的数量级为10-5,C正确;
10c(H+)=10-4.8,所以,Ka (HA)的数量级为10-5,C正确;
D. P点lg![]() =-1,Q点lg
=-1,Q点lg![]() =1,P→Q过程中c(A-)逐渐增大,A-水解促进水的电离,c(A-)越大,水的电离程度越大,D正确;
=1,P→Q过程中c(A-)逐渐增大,A-水解促进水的电离,c(A-)越大,水的电离程度越大,D正确;
故合理选项是B。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】NOx是造成大气污染的主要物质,用还原法将其转化为无污染的物质,对于消除环境污染有重要意义。
(1)已知:2C(s)+O2(g)![]() 2CO(g) △H1= -221.0 kJ/mol
2CO(g) △H1= -221.0 kJ/mol
N2(g)+O2(g)![]() 2NO (g) △H2= +180.5 kJ/mol
2NO (g) △H2= +180.5 kJ/mol
2NO(g)+2CO(g)![]() 2CO2(g)+N2(g) △H3= -746.0 kJ/mol
2CO2(g)+N2(g) △H3= -746.0 kJ/mol
回答下列问题:
①用焦炭还原NO生成无污染气体的热化学方程式为_______。
②在一定温度下,向甲、乙、丙三个恒容密闭容器中加入一定量的NO和足量的焦炭,反应过程中测得各容器中c(NO)(mol/L)随时间(s)的变化如下表。
已知:三个容器的反应温度分别为T甲= 400℃、T乙= 400℃、T丙= a ℃
时间 | 0 s | 10 s | 20 s | 30 s | 40 s |
甲 | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
乙 | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
丙 | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
甲容器中,该反应的平衡常数K=_______。丙容器的反应温度a _______400℃(填“”、“<”或“=”),理由是_______。
(2)用NH3催化还原NOx消除氮氧化物的污染。
已知:8NH3(g)+6NO2(g)![]() 7N2(g) +12H2O(l) △H<0。相同条件下,在2 L密闭容器内,选用不同的催化剂进行反应,产生N2的量随时间变化如图所示。
7N2(g) +12H2O(l) △H<0。相同条件下,在2 L密闭容器内,选用不同的催化剂进行反应,产生N2的量随时间变化如图所示。

①在催化剂A的作用下,0~4 min的v(NH3) = _______。
②该反应活化能Ea(A)、Ea(B)、Ea(C)由大到小的顺序是_______,理由是_______。
③下列说法正确的是_______(填标号)。
a.使用催化剂A达平衡时,△H值更大
b.升高温度可使容器内气体颜色加深
c.单位时间内形成N-H键与O-H键的数目相等时,说明反应已经达到平衡
d.若在恒容绝热的密闭容器中反应,当平衡常数不变时,说明反应已经达到平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】材料是人类文明进步的阶梯,第ⅢA、ⅣA、VA及Ⅷ族元素是组成特殊材料的重要元素。
回答下列问题:
(1)基态B核外电子占据的最高能级的电子云轮廓图形状为________。与硼处于同周期且相邻的两种元素和硼的第一电离能由大到小的顺序为______。
(2)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态氮原子的未成对电子数相同,则其基态原子的价层电子排布式为_____。
(3)经测定发现,N2O5固体由NO2+和NO3-两种离子组成,该固体中N原子杂化类型有__。
(4)MgCO3的热分解温度_____(填“高于”或“低于”)CaCO3的原因是________。
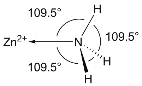
(5)NH3分子在独立存在时H-N-H键角为107°。如图是[Zn(NH3)6]2+离子的部分结构以及H-N-H键角的测量值。解释NH3形成如图配合物后H-N-H键角变大的原因:_________。
(6)某种金属锂的硼氢化物是优质固体电解质,并具有高储氢密度。阳离子为Li+,每个阴离子是由12个硼原子和12个氢原子所构成的原子团。阴离子在晶胞中位置如图所示,其堆积方式为_____,Li+占据阴离子组成的所有正四面体中心,该化合物的化学式为_____(用最简整数比表示)。假设晶胞边长为anm,NA代表阿伏伽德罗常数的值,则该晶胞的密度为_____g/cm3。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸雨的形成是一种复杂的大气化学和光学化学过程,在清洁空气、污染空气中形成硫酸型酸雨的过程如下:

下列有关说法错误的是( )
A. 光照能引发酸雨的形成
B. 所涉及的变化均为氧化还原反应
C. 污染空气能加快酸雨的形成
D. 优化能源结构能有效遏制酸雨污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
①标准状况下,6. 02×1023个分子所占的体积约是22. 4 L
②0. 5 mol H2所占体积为11. 2 L
③标准状况下,1 mol H2 O的体积为22.4 L
④标准状况下,28 g CO与N2的混 合气体的体积约为22. 4 L
⑤各种气体的气体摩尔体积都 约为22. 4 L/mol
⑥标准状况下,体积相同的气体的分子数相同
A.①③⑤B.④⑥C.③④⑥D.①④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四碘化锡(Snl4,M=627g/mol)是一种橙色针状晶体,遇水易发生水解,可在非水溶剂中由Sn和l2直接化合得到,实验装置如图(1)(加热装置略去)所示。

实验步骤如下:
组装仪器并加入药品后,通入冷凝水,加热圆底烧瓶,控制反应温度在80℃左右,保持回流状态,直到反应完全。取下仪器A、B,趁热将溶液倒入干燥的烧杯中,用热的CCl4洗涤圆底烧瓶内壁和锡片,并将洗涤液合并入烧杯内。再将烧杯置于冷水浴中冷却即析出Snl4晶体。
请回答下列问题:
(1)仪器B的名称为___________,冷凝水的进口为____________(填“甲”或“乙”)。为了控制反应温度,对圆底烧瓶适宜的加热方式是____________________。
(2)仪器A中盛放的试剂为无水CaCl2,其作用为____________。
(3)反应完全的现象为__________,用热的CCl4洗涤圆底烧瓶内壁和锡片的目的是_______,从烧杯中获取产品的操作名称为______________。
(4)产品的纯度可用滴定法测定:称取m g产品,加入足量的水,使产品充分水解[SnI4+(2+x)H2O=SnO2·xH2O↓+4HI]。将上层清液全部定容于250mL容量瓶中。移取25.00mL于锥形瓶中,加入少量CCl4和几滴KSCN溶液,用c mol/L的标准FeCl3溶液滴定至终点,平行测定三次,平均消耗标准FeCl3溶液的体积为1mL。(已知:2Fe3++2I-![]() 2Fe2++I2)
2Fe2++I2)
①下列关于滴定分析,不正确的是________。
a.图(2)中为避免滴定管漏液,应将凡士林涂在旋塞的a端和旋塞套内的c端
b.滴定接近终点时,滴定管的尖嘴可以接触锥形瓶的内壁
c.当下层溶液变为紫红色且半分钟不褪色即为滴定终点
d.若不加CCl4,则测得样品的纯度可能偏高
②产品纯度的表达式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】改变0.1mol/L的二元弱酸H2A溶液的pH,溶液中的H2A、HA-、A2-的物质的量分数δ(X)随pH的变化如图所示![]() 。下列叙述正确的是
。下列叙述正确的是

A. Ka2(H2A)的数量级为10- 4
B. 0.1mol/L的NaHA溶液,pH=2.7
C. 向pH=0.5的溶液中逐滴加入强碱至pH=2.7的过程中,每滴一滴强碱,在X点时溶液pH变化最大
D. 0.1mol/LNa2A溶液的pH=8.6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中的一定量混合气体发生反应:xA(g)+yB(g)![]() zC(g)。平衡时测得A的浓度为0.50 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30 mol/L。下列有关判断错误的是 ( )
zC(g)。平衡时测得A的浓度为0.50 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30 mol/L。下列有关判断错误的是 ( )
A. x+y<z B. 平衡向逆反应方向移动
C. B的转化率降低 D. C的体积分数下降
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A. 将饱和FeCl3溶液滴入沸水中制备胶体:Fe3++3H2O![]() Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
B. 用FeS去除废水中的Hg2+:Hg2+ + S2- === HgS↓
C. AlCl3溶液与Na2S溶液混合生成沉淀::2 Al3++3S2-==Al2S3↓
D. NH4Cl溶于D2O中显酸性:NH4++D2O![]() NH3·HDO+D+
NH3·HDO+D+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com