
500 mL NaNO3��Cu(NO3)2�Ļ����Һ��c( NO3- )��0.3 mol��L��1����ʯī���缫������Һ����ͨ��һ��ʱ����������ռ�������1.12 L(��״����)���ٶ�������Һ�����Ϊ500 mL������˵����ȷ����
A��ԭ�����Һ��c(Na��)��0.2 mol��L��1
B��������Һ��c(H��)��0.2 mol��L��1
C�������������й�ת��0.4 mol����
D������õ���Cu�����ʵ���Ϊ0.1 mol
B
�����������⿼���˵��ԭ������ѧ����ȣ����ڿ��鿼���ķ������������������������������ӷŵ�(??��������OH��> NO3- )�����������Ϣ������һ����OH���ŵ磬����0.05 mol������ת��0.2 mol���ӣ��������ӷŵ�������Cu2��>H��>Na��������Cu2���ȷŵ磬Ȼ����H���ŵ磬��������0.05 mol����ʱ��ת��0.1 mol���ӣ����ݵ�ʧ�����غ�֪��Cu2��ת��0.1 mol���ӣ�n(Cu2��)��0.05 mol������ԭ��Һ��n[Cu(NO3)2]��0.05 mol��n( NO3- )��0.3 mol/L��0.5 L��0.15 mol��n(NaNO3)��0.05 mol��ԭ�����Һ��c(Na��)��0.1 mol��L��1��A���������Ϸ���������ܷ���ʽCu2����2H2O Cu��H2����O2����2H����֪������0.05 mol Cu��0.05 mol O2��0.05 mol H2��0.1 mol H����������Һ��c(H��)��
Cu��H2����O2����2H����֪������0.05 mol Cu��0.05 mol O2��0.05 mol H2��0.1 mol H����������Һ��c(H��)��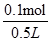 ��0.2 mol��L��1��B����ȷ��D����������������й�ת��0.2 mol���ӣ�C�����
��0.2 mol��L��1��B����ȷ��D����������������й�ת��0.2 mol���ӣ�C�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��2 ���ͣ�ѡ����
������ˮ�����״�л���C4H6O2������˵����ȷ����
A�������ʲ���ʹ���CC14��Һ��ɫ B��������һ�����ܷ���ȡ����Ӧ
C�������ʿ��ܵĽṹ����5�� D����������C2H4O2���ܻ�Ϊͬϵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��16 ���ͣ�ѡ����
�����Ȼ�ѧ����ʽ��д��ȷ����(��H�ľ���ֵ����ȷ)
A��C2H5OH(l)��3O2(g)===2CO2(g)��3H2O(g) ��H����1367.0 kJ��mol��1(ȼ����)
B��NaOH(aq)��HCl(aq)===NaCl(aq)��H2O(l) ��H����57.3 kJ��mol��1(���)
C��2NO2===O2��2NO ��H����116.2 kJ��mol��1(��Ӧ��)
D��S(s)��O2(g)===SO2(g) ��H����296.8 kJ��mol��1(��Ӧ��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��15 ���ͣ�ѡ����
ʵ�飺����ʢ��1 mL 0.1 mol/L MgCl2��Һ�Թ��м�1 mL 0.2 mol/L NaOH��Һ���õ���Һa�����˵õ���Һb�Ͱ�ɫ����c���������c�еμ�0.1mol/LFeCl3��Һ��������Ϊ���ɫ�����з�������ȷ����
A����Һa�д��ڳ����ܽ�ƽ�⣺Mg (OH) 2(s) Mg2��(aq)��2OH��(aq)
Mg2��(aq)��2OH��(aq)
B����Һb�в�����Mg2+
C��������ɫ�仯˵��Mg (OH)2ת��ΪFe(OH)3
D��ʵ�����֤��Fe(OH)3��Mg (OH)2������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��15 ���ͣ�ѡ����
��x mL 2.0 mol��L��1��������Ͷ��a gþ���Ͻ𣬽�����ȫ�ܽ⣬�ټ���y mL 1.0 mol��L��1��NaOH��Һ�����ﵽ���ֵ��������Ϊ(a��1.7) g��������˵������ȷ����
A��x��2y
B��þ���Ͻ������ᷴӦʱת�Ƶ��ӵ���ĿΪ0.1NA
C��þ���Ͻ������ᷴӦ����H2������ڳ��³�ѹ�´���1.12 L
D��a��ȡֵ��ΧΪ0.9 g��a��1.2 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��14 ���ͣ��ƶ���
��ʽ̼��ͭ������������;�㷺�Ļ���ԭ�ϡ�
��1����ҵ�Ͽ������Կ�ʴ��Һ����Ҫ�ɷ���Cu2+��Fe2+��Fe3+��H +��Cl?���Ʊ���ʽ̼��ͭ�����Ʊ��������£�
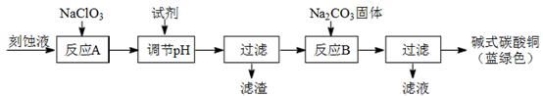
��֪��Cu2+��Fe2+��Fe3+���ɳ�����pH���£�
���� | Cu(OH)2 | Fe (OH)2 | Fe (OH)3 |
��ʼ����pH | 4.2 | 5.8 | 1.2 |
��ȫ����pH | 6.7 | 8.3 | 3.2 |
�������Ƶ������� ��
�ڷ�ӦA�������Һ��pH��ΧӦΪ ��
�۵�һ�ι��˵õ��IJ�Ʒϴ��ʱ������ж��Ѿ�ϴ���� ��
���������ɫ��Ʒ�л���CuO���ʵ�ԭ���� ��
��2��ijѧϰС����ʵ������������ͼ��ʾװ����ȡ������̽�������ʡ�
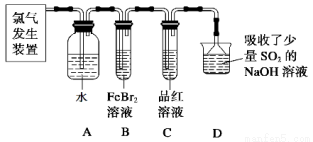
��ʵ�����ö������̺�Ũ���������ȡ����������������Ҫ��©�� ��
����C��Ʒ����Һ��ɫ���ܷ�֤��������ˮ��Ӧ�IJ�����Ư���ԣ�˵��ԭ�� ����ʱBװ���з�����Ӧ�����ӷ���ʽ�� ��
��д��A��Һ�о���ǿ���������Ļ�ѧʽ ������A��Һ�м���NaHCO3��ĩ����۲쵽�������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��14 ���ͣ�ѡ����
��Է�������Ϊ100���л���A�����Ʒ�Ӧ������ȫȼ��ֻ����CO2��H2O����A��һ����̼��������һ�ȴ������ĿΪ�� ��
A��5 B��4 C��3 D��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��13 ���ͣ������
�����ʽṹ�����ʡ�
M��ԭ������<30��һ�ֽ����������ں��ա�����������DZ��ȹ�ҵ���ţ�Mԭ�ӵ�������пչ�������������ܼ����ڵ��Ӱ����״̬��
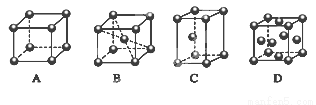
��1��Mԭ�ӵ���Χ�����Ų�ʽΪ__________�������ڱ������� ��Ԫ�ء�
��2��M�Ķѻ���ʽ���ڼ��ͣ��侧��ʾ��ͼΪ______������ţ���
��3��MCl3��6H2O�����ֲ�ͬ��ɫ���칹��
A��[M(H2O)6]Cl3 B��[M(H2O)5Cl]Cl2��H2O��C��[M(H2O)4Cl2]Cl��2H2O��Ϊ�ⶨ����MCl3��Һ�����İ���ɫ�����������칹�壬ȡ0.010 mol MCl3��6H2O�����Һ���μ�����AgNO3��Һ���õ�����2.870 g�����칹��Ϊ ����A��B��C����
��4��MO2Cl2������Ϊ����ɫҺ�壬�۵�-96.5�棬�е�117�棬�����ͪ��CH3COCH3����CCl4��CS2�Ȼ��ܡ�
�ٹ�̬MO2Cl2����________���壻
��CS2��̼ԭ�Ӻͱ�ͪ(CH3COCH3)�ʻ��е�̼ԭ�ӷֱ��ȡ���ӻ���ʽΪ____�ӻ���________�ӻ���
��5����3��M�������K[M(C2O4)2(H2O)2]�У�������______����C2O42-��Ϊ�ȵ�����ķ�����(�ѧʽ)__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��11 ���ͣ������
�����ʽṹ�����ʡ�
����Ԫ�����ڱ��е�������Ԫ�ص����֪ʶ���ش��������⣺
��1����������Ԫ�صĻ�̬ԭ�ӵĵ����Ų���4s�����ֻ��1�����ӵ�Ԫ����________�֣�д��Cu+�ĺ�������Ų�ʽ________��
��2���������Ų����ɽ����ڱ����Ԫ�ػ��ֳ��������������Ԫ��������s����Ԫ����________�֣�����d����Ԫ����________�֡�
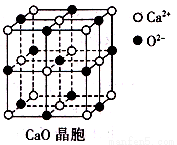
��3��CaO��������ʾ��CaO������Ca2+����λ��Ϊ ��CaO����ɫ��ӦΪש��ɫ��������������ǵĻ�
���ﶼ���Է�����ɫ��Ӧ����ԭ����_______��
��4���ɵ������أ�KN3���ȷֽ�ɵô�N2��2KN3(s)=2K(l)+3N2(g)�������й�˵����ȷ����_______����ѡ����ĸ����
A NaN3��KN3�ṹ���ƣ�ǰ�߾����ܽ�С
B����صľ����ṹ��ͼ��ʾ�� ��ÿ�������з�̯2����ԭ��
��ÿ�������з�̯2����ԭ��
C���ĵ�һ�����ܴ�����
D���������º��ȶ�������Ϊ���ĵ縺��С
��5����������(TiO2)�dz��õġ����нϸߴ����Ժ��ȶ��ԵĹ������O2����������£��ɽ�CN-������CNO-��CN-�ĵ���ʽΪ_______,CNO-������ԭ�ӵ��ӻ���ʽΪ______��
��6����CrCl3��Һ�У�һ�������´������Ϊ[CrCln(H2O)6��n]x�� (n��x��Ϊ���������������ӣ�����ͨ�������ӽ�����֬��R-H)���ɷ������ӽ�����Ӧ��
[CrCln(H2O)6-n]X++ xR- Rx[CrCln(H2O)6��n]+xH+������0.0015 mol[CrCln(H2O)6��n]x������Һ����R-H��ȫ�������к����ɵ�H+��Ũ��Ϊ0.1200 mol��L-1NaOH��Һ25.00 mL����������ӵĻ�ѧʽΪ_______��
Rx[CrCln(H2O)6��n]+xH+������0.0015 mol[CrCln(H2O)6��n]x������Һ����R-H��ȫ�������к����ɵ�H+��Ũ��Ϊ0.1200 mol��L-1NaOH��Һ25.00 mL����������ӵĻ�ѧʽΪ_______��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com