
【题目】汽车尾气中含有CO、NO、NO2、碳氢化合物等多种污染物。回答下列问题:
(1)汽车燃料中不含氮元素,尾气中所含NO产生的原因是_________________________(用化学方程式表示)。
(2)已知:2C4H10(g)+13O2(g)=8CO2(g)+10H2O(g) △H1=-5316 kJ·mol-1
N2(g)+O2(g)=2NO(g) △H2
2NO(g)+2CO(g)=N2(g)+2CO2(g) △H3=-746 kJ·mol-1
①若H2O(l)=H2O(g) △H=+44 kJ·mol-1,则表示正丁烷燃烧热的热化学方程式为__________________。
②部分化学键键能数据为:氧分子中氧氧键的键能为494 kJ·mol-1;C=O的键能为799 kJ·mol-1;CO分子中碳氧键的键能为1076 kJ·mol-1;请计算出反应2CO(g)+O2(g)=2CO2(g)的△H=______________kJ·mol-1,由此可以计算△H2=__________kJ·mol-1
(3)1573K时,N2+O2![]() 2NO平衡常数为2.0×10-6,若测得内燃机内平衡混合气中氮气、氧气的物质的量分别为0.2mol、0.001mol,则生成NO的物质的量为_____________mol,N2的转化率为____________。
2NO平衡常数为2.0×10-6,若测得内燃机内平衡混合气中氮气、氧气的物质的量分别为0.2mol、0.001mol,则生成NO的物质的量为_____________mol,N2的转化率为____________。
(4)T<500K时,反应NO2(g)+CO(g)=NO(g)+CO2(g)分两步进行:
第一步:NO2(g)+NO2(g)=NO3(g)+NO(g) (慢反应)
第二步:NO3(g)+CO(g)=NO(g)+CO2(g) (快反应)
下列表述正确的是__________(填标号)
A.反应速率与NO2浓度有关 B.反应速率与NO浓度有关
C.反应的中间产物只有NO3 D.第一步反应活化能较低
【答案】N2+O2![]() 2NO C4H10(g) +
2NO C4H10(g) +![]() O2 (g) = 4CO2(g) + 5H2O(l) ΔH=-2878 kJ·mol-1 -550 +196 2.0×10-5 0.005% AC
O2 (g) = 4CO2(g) + 5H2O(l) ΔH=-2878 kJ·mol-1 -550 +196 2.0×10-5 0.005% AC
【解析】
(1)进入气缸的气体是空气,含有氮气和氧气在高温下反应;
(2)①根据盖斯定律计算;
②△H=反应物的总键能-生成物的总键能;
(3)利用平衡常数和三段式进行计算;
(4)利用反应原理分析;
(1)进入气缸的气体是空气,含有氮气和氧气在高温下反应生成一氧化氮,污染空气,方程式是N2+O2![]() 2NO ,
2NO ,
故答案是:N2+O2![]() 2NO ;
2NO ;
(2)① ①2C4H10(g)+13O2(g)=8CO2(g)+10H2O(g) △H1=-5316 kJ·mol-1
②H2O(l)=H2O(g) △H=+44 kJ·mol-1,
(①-②×10)÷2得
C4H10(g) +![]() O2 (g) = 4CO2(g) + 5H2O(l) ΔH=-2878 kJ·mol-1
O2 (g) = 4CO2(g) + 5H2O(l) ΔH=-2878 kJ·mol-1
故答案为:C4H10(g) +![]() O2 (g) = 4CO2(g) + 5H2O(l) ΔH=-2878 kJ·mol-1 ;
O2 (g) = 4CO2(g) + 5H2O(l) ΔH=-2878 kJ·mol-1 ;
②△H=反应物的总键能-生成物的总键能=2×1076 kJ·mol-1+494 kJ·mol-1-2×2×799 kJ·mol-1=-550 kJ·mol-1;
①2CO(g)+O2(g)=2CO2(g) △H=-550kJ·mol-1
②2NO(g)+2CO(g)=N2(g)+2CO2(g) △H3=-746 kJ·mol-1
有盖斯定律得:①-②得N2(g)+O2(g)=2NO(g) △H2=196 kJ·mol-1
故答案为:-550;+196;c(NO)2
(3) N2+O2![]() 2NO,K=
2NO,K=![]() =
=![]() =2.0×10-6,解得n(NO)=2.0×10-5,
=2.0×10-6,解得n(NO)=2.0×10-5,
消耗的氮气的物质的量是1.0×10-5,氮气的转化率=![]() ×100%= 0.005%
×100%= 0.005%
故答案为:2.0×10-5 ;0.005%;
(4)A.第一步是慢反应,决定整个反应的速率快慢,所以反应速率与二氧化氮的浓度有关,故A正确;
B.第二步是快反应,不能决定整个反应速率,故反应速率与一氧化氮的浓度无关,故B错误;
C.第一步反应生成的有三氧化氮,三氧化氮又作了第二个反应的反应物,所以是中间产物,故C正确;
D.第一步反应较慢,说明活化能较高,故D错误;
故选:AC。


科目:高中化学 来源: 题型:
【题目】用水稀释0.1mol/L氨水时,溶液中随着水量的增加而减小的是( )
A. c(OH-)/c(NH3·H2O) B. n(OH-)
C. c(NH3·H2O)/c(OH-) D. c(H﹢)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氧化二钴主要用作颜料、釉料及磁性材料,利用铜钴矿石制备Co2O3的工艺流程如图所示。
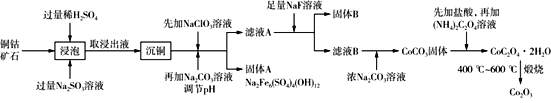
已知:铜钴矿石主要含有CoO(OH)、CoCO3、Cu2(OH)2CO3和SiO2,其中还含有一定量的Fe2O3、MgO和CaO等。请回答下列问题:
(1)“浸泡”过程中可以加快反应速率和提高原料利用率的方法是_______(写出2种即可)。
(2)“浸泡”过程中,加入Na2SO3溶液的主要作用是____________。
(3)向“沉铜”后的滤液中加入NaClO3溶液,写出滤液中的金属离子与NaClO3反应的离子方程式________________。
(4)温度、pH对铜、钴浸出率的影响如图1、图2所示:
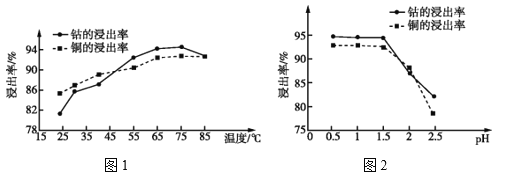
①“浸泡”铜钴矿石的适宜条件为__________________。
②图2中pH增大时铜、钴浸出率下降的原因可能是___________。
(5)CoC2O4·2H2O在空气中高温煅烧得到Co2O3的化学方程式是________。
(6)一定温度下,向滤液A中加入足量的NaF溶液可将Ca2+、Mg2+沉淀而除去,若所得滤液B中c(Mg2+)=1.0×10-5 mol/L,则滤液B中c(Ca2+)为______。[已知该温度下Ksp(CaF2)=3.4×10-11,Ksp(MgF2)=7.1×10-11]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应N2O4(g)![]() 2NO2(g) ΔH=+57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是
2NO2(g) ΔH=+57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是

A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.A、B两点气体的平均相对分子质量:A>B
D.B、C两点化学平衡常数:B<C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写不正确的是
A.向CaCl2 溶液中通入少量CO2气体:Ca2+ + CO2 + H2O=CaCO3↓ + 2H+
B.大理石与醋酸反应:CaCO3 + 2CH3COOH= Ca2+ + 2CH3COO-+ H2O + CO2↑
C.制备Fe(OH)3胶体:Fe3+ + 3H2O![]() Fe(OH)3(胶体)+ 3H+
Fe(OH)3(胶体)+ 3H+
D.少量碳酸氢钠溶液与足量石灰水反应:Ca2+ + OH-+ HCO3-=CaCO3↓ + H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废弃物的资源化回收再利用,可以更大限度地发挥原材料的价值。某教师在指导学生做研究性学习时,拟利用废铁屑在实验室制备FeSO4溶液,再与等物质的量的(NH4)2SO4反应,制备补血剂硫酸亚铁铵晶体[(NH4)2Fe(SO4)2·6H2O,相对分子质量为392]。硫酸亚铁铵晶体比一般亚铁盐稳定,在空气中不易被氧化,易溶于水,不溶于乙醇。
(1)废铁屑的净化:将废铁屑投入10%的碳酸钠溶液中并加热5~10min,通过倾析法弃去纯碱溶液,并用蒸馏水洗净废铁屑,待用。
(2)酸浸净化后的废铁屑:将2gFe粉、10mL3mol·L-1的H2SO4溶液加入烧瓶中反应,用如图所示装置制备FeSO4溶液。保持温度70~80℃,适当添加水以补充被蒸发掉的水分,并控制溶液的pH,至反应无明显气泡产生,停止加热,过滤,称量残留固体质量。
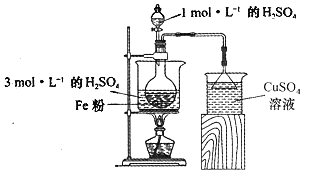
①反应过程中会产生少量H2S、PH3等气体,需使用封闭装置。写出用CuSO4溶液吸收H2S气体的化学反应方程式:____________________________
②反应过程中使用过量铁粉的目的是____________________________
(3)制备(NH4)2Fe(SO4)2·6H2O:向FeSO4溶液中加入一定质量的(NH4)2SO4固体,70~80℃条件下溶解后,趁热倒入50mL乙醇中,析出晶体。
实验中,需对过滤出产品的母液(pH<1)进行处理。室温下,分别取母液并向其中加入指定物质,反应后的溶液中主要存在的一组离子正确的是_____ (填序号)。
A.通入过量Cl2:Fe2+、H+、NH4+、Clˉ、SO42ˉ
B.加入过量KSCN溶液:K+、NH4+、Fe3+、SO42ˉ、SCNˉ
C.加入过量NaOH溶液:Na+、Fe2+、NH4+、SO42ˉ、OHˉ
D.加入过量NaClO和NaOH的混合溶液:Na+、SO42ˉ、Clˉ、ClOˉ、OHˉ
(4)产品纯度测定:称取ag产品溶于水,配制成500mL溶液,取25.00mL待测液,用浓度为cmol·L-1的酸性KMnO4溶液滴定。重复上述操作2次实验结果如下:

该产品的纯度为____________________________(用含a、c的代数式表示)。
有同学提出,测定产品中SO42ˉ的含量也可测定产品的纯度,请补充完整实验方案:称取约0.4g样品,溶于70mL水,__________________________________________________,将沉淀移入坩埚,灼烧至恒重,记录数据(实验中必须使用的试剂有:2mol·L-1的HCl溶液、BaCl2溶液、AgNO3溶液)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】检验甲醛含量的方法有很多,其中银﹣Ferrozine法灵敏度较高。测定原理为甲醛把氧化银还原成Ag,产生的Ag与Fe3+定量反应生成Fe2+,Fe2+与菲洛嗪(Ferrozine)形成有色配合物,通过测定吸光度计算出甲醛的含量。某学习小组类比此原理设计如下装置测定新装修居室内空气中甲醛的含量(夹持装置略去)。

已知:甲醛能被银氨溶液氧化生成CO2,氮化镁与水反应放出NH3,毛细管内径不超过1 mm。请回答下列问题:
(1)A装置中反应的化学方程式为___________,用饱和食盐水代替水制备NH3的原因是___________________。
(2)B中装有AgNO3溶液,仪器B的名称为________。
(3)银氨溶液的制备。关闭K1、K2,打开K3,打开______,使饱和食盐水慢慢滴入圆底烧瓶中,当观察到B中白色沉淀恰好完全溶解时,________。
(4)室内空气中甲醛含量的测定。
①用热水浴加热B,打开K1,将滑动隔板慢慢由最右端抽到最左端,吸入1 L室内空气,关闭K1;后续操作是______________;再重复上述操作3次。毛细管的作用是__________。
②向上述B中充分反应后的溶液中加入稀硫酸调节溶液pH=1,再加入足量Fe2(SO4)3溶液,充分反应后立即加入菲洛嗪,Fe2+与菲洛嗪形成有色物质,在562 nm处测定吸光度,测得生成Fe2+1.12 mg,空气中甲醛的含量为____mg·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组用如图装置探究甲烷与氯气反应同时收集副产品盐酸,下列说法正确的是( )
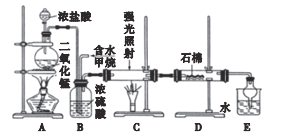
A.浓硫酸在整套装置中的作用是干燥气体
B.采用200mL8mol/L盐酸与足量二氧化锰反应最多可得0.4molCl2
C.石棉上可滴加饱和食盐水,用于吸收氯气
D.光照一段时间,装置C硬质玻璃管内壁出现的黑色小颗粒可能是碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得。下列叙述正确的是( )
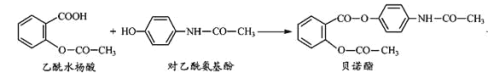 +H2O
+H2O
A.贝诺酯分子中有三种含氧官能团
B.贝诺酯与足量 NaOH 溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠
C.乙酰水杨酸和对乙酰氨基酚均能与 NaHCO3溶液反应
D.可用 FeCl3 溶液区别乙酰水杨酸和对乙酰氨基酚
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com