
分析 (1)依据配制一定物质的量浓度溶液一般步骤选择需要仪器;依据配制溶液体积选择容量瓶规格,依据m=CVM计算溶质的质量;
(2)分析操作对溶质物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析;
(3)反应中MnO4-→Mn2+,锰元素化合价由+7价降低为+2价,共降低5价,H2C2O4→CO2,碳元素化合价由+3价升高为+4价,共升高2价,化合价升降最小公倍数为10,据此结合电荷守恒、原子守恒配平方程式;
(4)根据滴定数据及钙离子与高锰酸钾的关系式计算出血液样品中Ca2+的浓度.
解答 解:(1)用固体配制一定物质的量浓度溶液一般步骤:计算、称量、溶解、移液、洗涤、定容、摇匀等,用到的仪器:托盘天平、药匙、烧杯、玻璃棒、容量瓶、胶头滴管,需要450ml 0.02mol/L酸性KMnO4标准溶液,应选择500mL容量瓶,实际配制500mL溶液,所以还需要的仪器:500ml容量瓶; 胶头滴管;需要高锰酸钾质量m=0.02mol/L×0.5L×158g/mol=1.6g;
故答案为:500ml容量瓶; 胶头滴管;1.6;
(2)A.没有冷却至室温就转移液体到容量瓶并完成定容,导致溶液体积偏小,溶液浓度偏高,故A选;
B.使用容量瓶配制溶液,定容时,俯视刻度线,导致溶液体积偏小,溶液浓度偏高,故B选;
C.没有用蒸馏水洗涤烧杯2-3次,并将溶液移入容量瓶中,导致溶质的物质的量偏小,溶液浓度偏低,故C不选;
D.容量瓶刚用蒸馏水洗净,没有烘干就用来配制溶液,对溶质的物质的量和溶液体积都不产生影响,溶液浓度不变,故D不选;
E.定容时,滴加蒸馏水,不慎液面略高于刻度线,吸出少量水使凹液面最低点与刻度线相切,导致溶质的物质的量偏小,溶液浓度偏大,故E不选;
故选:AB;
(3)反应中MnO4-→Mn2+,锰元素化合价由+7价降低为+2价,共降低5价,H2C2O4→CO2,碳元素化合价由+3价升高为+4价,共升高2价,化合价升降最小公倍数为10,结合电荷守恒、原子守恒配平方程式为:2KMnO4+5H2C2O4+3H2SO4=2MnSO4+1K2SO4+8H2O+10CO2;
故答案为:2、5、3、2、1、8、10;
(4)血样20.00mL经过上述处理后得到草酸,草酸消耗的消耗的高锰酸钾的物质的量为:0.020mol/L×0.013L=2.6×10-4mol,根据反应方程式2KMnO4+5H2C2O4+3H2SO4=2MnSO4+2K2SO4+10H2O+8CO2,及草酸钙的化学式CaC2O4,可知:n(Ca2+)=n(H2C2O4)=$\frac{5}{2}$n(MnO4-)=2.5×2.6×10-4mol=6.5×10-4mol,
Ca2+的质量为:40g/mol×6.5×10-4mol=0.026g,钙离子的浓度为:$\frac{0.026g}{20mL}$=0.0012g/cm3=1.2mg/cm3,
故答案为:1.3.
点评 本题考查了配制一定物质的量浓度的方法及误差分析,氧化还原滴定,明确配置一定物质的量浓度原理和操作步骤、明确氧化还原滴定原理和操作是解题关键,侧重考查学生对实验基本知识的掌握情况,题目难度中等.


 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:解答题



 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
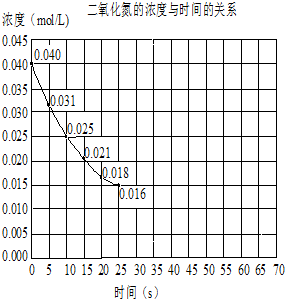
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 700℃ | 900℃ | |
| K1 | 1.47 | 2.15 |
| K2 | 2.38 | 1.67 |
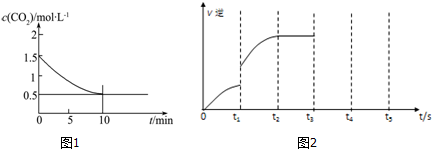
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 强电解质溶液的导电性一定比弱电解质溶液的导电性强 | |
| B. | 水溶液中导电能力差的电解质一定是弱电解质 | |
| C. | 强电解质在稀的水溶液中全部以离子的形态存在 | |
| D. | 强电解质都是离子化合物,而弱电解质都是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ②③⑤⑨ | C. | ④⑤⑥⑦ | D. | ②③⑧⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某无色溶液中可能大量存在H+、Cl-、MnO4- | |
| B. | pH=2的溶液中可能大量存在Na+、NH4+、SiO32- | |
| C. | 冷的氢氧化钠溶液中通入氯气:Cl2+2OH-═ClO-+Cl-+H2O | |
| D. | 稀硫酸和氢氧化钡溶液反应:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过氧化氢电子式: | B. | F-的结构示意图: | ||
| C. | 邻羟基苯甲酸的结构简式: | D. | 中子数为28的钙原子:${\;}_{20}^{28}$Ca |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com