
| A、摩尔是物质的数量单位 |
| B、氢气的摩尔质量是2g |
| C、1molNH3的质量是17g |
| D、1mol气体所占的体积约为22.4L |
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2:1:1 |
| B、2:2:4 |
| C、1:2:2 |
| D、2:3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、75 mL 2 mol/L的CaCl2 |
| B、150 mL 3 mol/L的KCl |
| C、150 mL 1 mol/L的NaCl |
| D、75mL 2 mol/L的NH4Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、混合物:盐酸、生铁、空气 |
| B、化合物:CaCl2、NaOH、HCl |
| C、碱:苛性钠、纯碱、氢氧化钾 |
| D、单质:Ca、O3、石墨 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、+184.6kJ?mol-1 |
| B、-92.3kJ?mol-1 |
| C、-369.2kJ?mol-1 |
| D、+92.3kJ?mol- |
查看答案和解析>>
科目:高中化学 来源: 题型:
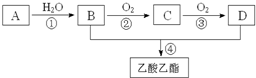 已知:A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平.现以A为主要原料合成乙酸乙酯,其合成路线如图所示.
已知:A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平.现以A为主要原料合成乙酸乙酯,其合成路线如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原固体混合中n[(NH4)2SO4]=0.05 mol |
| B、原固体混合中m(NH4NO3)=16 g |
| C、若完全溶解后溶液的体积为100 mL,则c(NH4NO3)=4 mol?L-1 |
| D、原固体混合中n(NH4NO3):n[(NH4)2SO4]=4:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com