
【题目】如图装置中,a、b都是惰性电极,通电一段时间后,a极附近溶液呈红色.

(1)电源的负极是_____,B中的阳极是_____。
(2)电极质量增加的是_____,A溶液的pH_____(填“增大”“减小”或“不变”)。
(3)B装置用U形管的原因是_________________________。
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z为短周期主族元素,在周期表中的相应位置如图所示,下列说法不正确的是( )

A.若X为金属元素,则其与氧元素形成的化合物中阴阳离子个数比可能是1∶2
B.若Z、Y能形成气态氢化物,则稳定性一定是ZHn>YHn
C.若Y是金属元素,则其氢氧化物既能和强酸反应又能和强碱反应
D.三种元素的原子半径:r(X)>r(Y)>r(Z)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯碱厂以食盐等为原料,生产烧碱、盐酸等化工产品。工艺流程可简单表示如图:
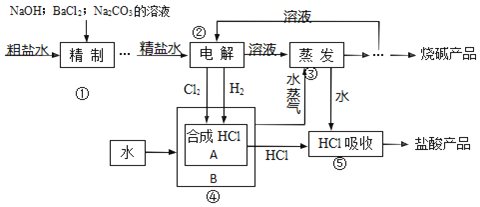
完成下列填空:
(1)粗盐水中含有 MgCl2、CaCl2、Na2SO4 等可溶性杂质,①步骤必须先后加入稍过量的 NaOH、BaCl2、Na2CO3溶液后过滤除杂。试写出加入 Na2CO3溶液时发生反应的离子方程式:______。写出②步骤发生反应的化学方程式:______。
(2)③步骤之后获得干燥的烧碱产品的有关操作有______。进行④步骤的生产设备 A、B之间传递的是(选填编号)______。
A.只有物料
B.既有物料又有能量
C.只有能量
D.既无物料也无能量
(3)如果用下列装置在实验室进行⑤步骤的实验,正确的是(选填编号)______。

若检验烧碱产品中是否含有少量 NaCl 杂质的实验方案是______。
(4)为测定烧碱产品的纯度,准确称取 5.000g 样品(杂质不含碱性物质)置于烧杯中,加水搅拌,冷却至室温后,将溶液全部转移入 1000mL 的容量瓶之后的一步操作是______。从所配得的溶液中每次都取出 20.00mL,用 0.12mol/L的盐酸滴定(选用常用指示剂),两次分别用去盐酸溶液19.81mL 和 19.79mL.判断滴定终点的依据是______,根据实验数据计算此烧碱产品的纯度为(保留两位小数)______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合物G的合成路线如下:

已知:C为烃
(1)A中含氧官能团名称为:____________。
(2)E的化学名称为:__________________。
(3)F→G的反应类型___________________。
(4)F的结构简式_____________________________。
(5)写反应①的化学方程式________________________________。
(6)写出D生成E的化学方程式________________________________。
(7)满足下列条件B的同分异构体有________种,其中核磁共振氢谱图中峰的面积之比为1∶2∶2∶3的结构为__________________(任意写一种)。①含苯环结构;②只有一种官能团。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某离子反应中涉及H2O、ClO-、NH4+、H+、N2、Cl-六种微粒,其中N2的物质的量随时间变化的曲线如图所示,下列判断正确的是( )

A. 该反应的还原剂是Cl-
B. 反应后溶液的酸性明显增强
C. 消耗1mol还原剂,转移6mol电子
D. 氧化剂与还原剂的物质的量之比为2∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:还原性HSO3->I-,氧化性IO3-> I2 。
(1)在NaIO3溶液中滴加少量NaHSO3溶液,发生下列反应。配平反应方程式并标出电子转移的方向和数目_______。
囗NaIO3+囗NaHSO3→ 囗I2+囗Na2SO4+囗H2SO4+囗H2O
(2)在NaIO3溶液中滴加过量NaHSO3溶液,反应完全后,推测反应后溶液中的还原产物为_______(填化学式);
(3)在含5molNaHSO3的溶液中逐滴加入NaIO3溶液。加入NaIO3的物质的量和析出I2单质的物质的量的关系曲线如图所示。写出反应过程中与AB段曲线对应的离子方程式_______;当溶液中I-与I2的物质的量之比为5:3时,加入的NaIO3为_______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米Fe3O4在磁流体、催化剂、医学等领域具有广阔的应用前景。氧化共沉淀制备纳米Fe3O4的方法如下:
Ⅰ.Fe2+的氧化:将FeSO4溶液用NaOH溶液调节pH至a,再加入H2O2溶液,立即得到FeO(OH)红棕色悬浊液。
(1)①若用NaOH溶液调节pH过高会产生灰白色沉淀,该反应的离子方程式是___。
②上述反应完成后,测得a值与FeO(OH)产率及其生成后溶液pH的关系,结果如下:
a | 7.0 | 8.0 | 9.0 |
FeO(OH)的产率 | <50% | 95% | >95% |
FeO(OH)生成后pH | 接近4 | 接近4 | 接近4 |
用离子方程式解释FeO(OH)生成后溶液pH下降的原因:___。
(2)经检验:当a=7时,产物中存在大量Fe2O3。对Fe2O3的产生提出两种假设:
i.反应过程中溶液酸性增强,导致FeO(OH)向Fe2O3的转化;
ii.溶液中存在少量Fe2+,导致FeO(OH)向Fe2O3的转化。
①分析,假设i不成立的实验依据是___。
②其他条件相同时,向FeO(OH)浊液中加入不同浓度Fe2+,30 min后测定物质的组成,结果如表:
c(Fe2+)/molL-1 | FeO(OH)百分含量/% | Fe2O3百分含量/% |
0.00 | 100 | 0 |
0.01 | 40 | 60 |
0.02 | 0 | 100 |
以上结果表明:___。
(3)a=7和a=9时,FeO(OH)产率差异很大的原因是___。
Ⅱ.Fe2+和Fe3+共沉淀:向FeO(OH)红棕色悬浊液中同时加入FeSO4溶波和NaOH浓溶液进行共沉淀,再将此混合液加热回流、冷却、过滤、洗涤、干燥,得到纳米Fe3
(4)共沉淀时的反应条件对产物纯度和产率的影响极大。
①共沉淀pH过高时,会导致FeSO4溶液被快速氧化;共沉淀pH过低时,得到的纳米Fe3O4中会混有的物质是___。
②已知N=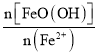 ,其他条件一定时,测得纳米Fe3O4的产率随N的变化曲线如图所示:
,其他条件一定时,测得纳米Fe3O4的产率随N的变化曲线如图所示:
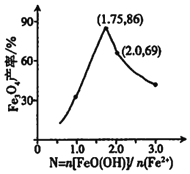
经理论分析,N=2共沉淀时纳米Fe3O4产率应最高,事实并非如此的可能原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积为2L的密闭容器中,进行如下化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g)。其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g)。其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=________________。
(2)该反应为____________反应(选填吸热、放热),原因是_____________________。
(3)能判断该反应是否达到化学平衡状态的依据是________________(多选扣分)。
a.容器中压强不变 b.混合气体中 c(CO)不变
c.υ正(H2)=υ逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为 _______________℃。该温度下,若向容器中分别加入2mol H2和2molCO2,10s后达到平衡,则这段时间内υ(H2)=_______________, CO2的转化率为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在指定溶液中,能大量共存的是( )
![]() 无色溶液中:
无色溶液中:![]()
![]()
![]()
![]()
![]()
![]() 的溶液中:
的溶液中:![]()
![]()
![]()
![]()
![]()
![]() 水电离的
水电离的![]() 浓度为
浓度为![]() 的溶液中:
的溶液中:![]()
![]()
![]()
![]()
![]()
![]() 加入铝粉放出氢气的溶液中:
加入铝粉放出氢气的溶液中:![]()
![]()
![]()
![]()
![]()
![]()
![]() 使甲基橙变红的溶液中:
使甲基橙变红的溶液中:![]()
![]()
![]()
![]()
![]()
![]() 中性溶液中:
中性溶液中:![]()
![]()
![]()
![]()
![]() 能溶解铜粉的溶液:
能溶解铜粉的溶液:![]()
![]()
![]()
![]()
![]()
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com