
����Ŀ��ijͬѧ���ʵ����̽��Ԫ�����ʵĵݱ���ɣ�ʵ��װ����ͼ��ʾ��
ʵ����������Ԫ����ۺ����������ǿ��̽��Ԫ�طǽ����Եݱ���ɡ�
��֪Aװ�õ���ƿ��װ�д���ʯ����Һ©����װ��ϡHNO3��Bװ����װ�б���̼��������Һ��װ��C��װ��Na2SiO3��Һ���Իش�
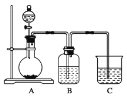
��1��A�з�Ӧ�����ӷ���ʽΪ________________________________________________��C�пɹ۲쵽��������_____________________________________________________��
��2��Bװ�õ�������__________________��
��3������ʵ��������֪̼���衢������Ԫ�طǽ����Ե�ǿ��˳����_____________________��
ʵ��������֪�����¸��������Ũ�����Ͽɲ������������ø�װ��̽���Ⱥ���Ԫ�صķǽ�����ǿ����
��4��д��Bװ���з�����Ӧ�����ӷ���ʽ��________________________________________��
��5��Cװ�õ�������_______________________________________��
��6��ʵ����ۣ������ԣ�_________________���ǽ����ԣ�___________________��
���𰸡�CaCO3+2H+=Ca2++CO2��+H2O ��Һ����� ��ȥ������̼�л��е��������� N��C��Si Cl2��2Br��=Br2��2Cl�� ����β������ֹ��Ⱦ���� Cl2��Br2 Cl��Br
��������
ʵ���Ԫ����ۺ����������ǿ���ж�Ԫ�طǽ�����ǿ��������Խǿ���ǽ�����Խǿ��A�з�Ӧ��̼��ƺ�ϡ���ᷴӦ���ɶ�����̼��֤�����ǽ����Դ���̼��Bװ����Ϊ�����ջӷ�������������������Ӱ��֤��̼�ķǽ����Դ��ڹ��ʵ�飬C��ΪNa2SiO3��Һ��������̼ͨ���������Һ��Ӧ���ɹ��������֤��̼�ķǽ����Դ��ڹ裻
ʵ���̽���ȡ���ķǽ�����ǿ���ĵݱ���ɣ�����ʵ��װ��ͼ��֪��ʵ��ԭ��ΪAװ�ã�Ũ�����������ط�Ӧ��������������ͨ��װ��B���廯����Һ�У���Һ���ֺ�ɫ�����嵥�����ɣ�˵���ȵķǽ�����ǿ���壬װ���лӷ�����������������ж�������Ⱦ����������Ҫ��װ��C������������Һ���ա�
(1)A�з�Ӧ��̼��ƺ�ϡ���ᷴӦ���ɶ�����̼����Ӧ�����ӷ���ʽΪ��CaCO3+2H+=Ca2++CO2��+H2O������ǿ����ȡ�����ԭ�������������ǿ��̼�ᣬ���ᡢ̼��ֱ�ΪN��C����ۺ����ᣬ���Կ�֤�����ǽ����Դ���̼��C��ΪNa2SiO3��Һ��ͨ�������̼��Ӧ���ɹ������������ǿ����ȡ�����ԭ����̼�������ǿ�ڹ��ᣬ̼�ᡢ����ֱ�ΪC. Si����ۺ����ᣬ���Կ�֤��̼�ķǽ����Դ��ڹ裬Cװ���й۲쵽��Һ����ǣ�
(2)�����ӷ�����ȡ�Ķ�����̼�к������ᣬ������ȥ���ᣬ��˵��Cװ���й۲쵽��Һ���������������η�Ӧ������̼������η�Ӧ������Bװ����Ϊ�����ջӷ���������������
(3)A�з�Ӧ��̼��ƺ�ϡ���ᷴӦ���ɶ�����̼��C��ΪNa2SiO3��Һ��ͨ�������̼��Ӧ���ɹ��������֤��̼�������ǿ�ڹ��ᣬ����̼�ᡢ���ᡢ���������ǿ��˳�������ᡢ̼�ᡢ���ᣬ����ʵ�������Ԫ����ۺ����������ǿ���ж�Ԫ�طǽ�����ǿ��������Խǿ���ǽ�����Խǿ����֪C��N��Si����Ԫ�طǽ����Ե�ǿ��ΪN��C��Si��
(4)Aװ�ã�Ũ�����������ط�Ӧ��������2KMnO4+16HCl(Ũ)=2KCl+2MnCl2+5Cl2��+8H2O������ͨ��װ��B:�廯����Һ�У�2Br+Cl2Br2+2Cl��Һ���ֺ�ɫ�����嵥�����ɣ�˵���ȵķǽ�����ǿ���壻
(5)װ���лӷ�����������������ж�������Ⱦ���������������������嵥�ʡ�����������Ҫ��װ��C:����������Һ���գ�
(6)���ʵ�������Խǿ����Ԫ�طǽ�����Խǿ�����ݷ�Ӧ��Cl2+2Br�TBr2+2Cl���õ������ԣ�Cl2��Br2���ǽ����ԣ�Cl��Br��


 ǧ�������������ĩ�����Ծ�����ϵ�д�
ǧ�������������ĩ�����Ծ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ�����������ȷ���� ��
A. 2-�����Ľṹ��ʽ��![]()
B. ����ʽ ![]() : ���Ա�ʾ�ǻ���Ҳ���Ա�ʾ����������
: ���Ա�ʾ�ǻ���Ҳ���Ա�ʾ����������
C. ����ģ�� ![]() �����Ա�ʾ������ӣ�Ҳ���Ա�ʾ���Ȼ�̼����
�����Ա�ʾ������ӣ�Ҳ���Ա�ʾ���Ȼ�̼����
D. �۱�ϩ�Ľṹ��ʽ�� ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и���Ƚ���ǰ�߸���(����ڻ�ǿ��)���ߵ���
A. ����Mg���������ܶѻ����ͽ���Cu�������������ܶѻ����Ŀռ�������
B. BF3��CH4����ԭ�ӵļ۲���Ӷ���
C. Si-O��C-O�ļ���
D. ���ǻ�����ȩ��![]() �������ǻ�����ȩ��
�������ǻ�����ȩ��![]() ���ķе�
���ķе�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I. ����ʵ�鷽����������________��
A������������Һ����һ����AgNO3��Һ�У��μӰ�ˮ������ǡ���ܽ�
B���ڼ���ȩ������Cu(OH)2����Һʱ����һ����CuSO4��Һ�У���������NaOH��Һ
C����֤RXΪ����飬��RX���ռ�ˮ��Һ��ϼ��ȣ�����Һ��ȴ���ټ�����������Һ
D����ˮ�Ҵ���Ũ���Ṳ�ȵ�170 �棬���Ƶõ�����ͨ�����Ը�����أ��ɼ����Ƶõ������Ƿ�Ϊ��ϩ
E�������л�����ϩ��ͨ��������һ�������·�Ӧ��ʹ��ϩת��Ϊ����
F����ȥ���ڱ��е��������ӣ����������ˮ������
G��ʵ������ȡ��ϩʱ���뽫�¶ȼƵ�ˮ������뷴ӦҺ�У��ⶨ��ӦҺ���¶�
II.ij��ѧС���������������������װ��(����ͼ)���Ի������Ʊ�����ϩ��
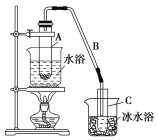
��֪��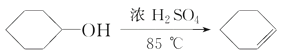 +H2O
+H2O
�ܶ�(g��cm��3) | �۵�(��) | �е�(��) | �ܽ��� | |
������ | 0.96 | 25 | 161 | ������ˮ |
����ϩ | 0.81 | ��103 | 83 | ������ˮ |
(1)�Ʊ���Ʒ��
��12.5 mL�����������Թ�A�У��ټ���1 mLŨ���ᣬҡ�Ⱥ�������Ƭ��������������Ӧ��ȫ�����Թ�C�ڵõ�����ϩ��Ʒ��
��A�����Ƭ��������________________���ڵ���B���˵�������е�������__________��
(2)�Ʊ���Ʒ��
�ٻ���ϩ��Ʒ�к��л������������������ʵȡ����뱥��ʳ��ˮ�������á��ֲ㣬����ϩ��________(��ϡ����¡�)�㣬��Һ����______(����)ϴ�ӡ�
a��KMnO4��Һ�� b��ϡH2SO4�� c��Na2CO3��Һ
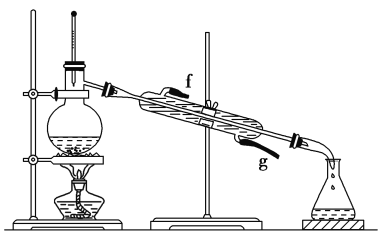
���ٽ�����ϩ����ͼװ��������ȴˮ��________(�f����g��)�ڽ��롣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ӱ�����ǵ������뽡����ij�����������п��ܺ������¼��ֿ�����������:Na+��NH4+��Mg2+��Al3+��SO42-��NO3-��Cl-��ijͬѧ�ռ���������������Ҫ��Ԥ�������������Һ,��Ʋ���������µ�ʵ�顣��������µ�ʵ������������жϸ�ͬѧ�ó��Ľ��۲���ȷ����
��֪:3NO3-+8Al+5OH-+2H2O=3NH3��+8AlO2-

A. ������һ������NH4+��Mg2+��SO42-��NO3-
B. ����1������2�ɷ�һ����ͬ
C. �����п��ܺ���Al3+
D. �������п��ܴ���NH4NO3��NaCl��MgSO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25 ��ʱ����Na2S����Cu2����Zn2�����ֽ���������(M2��)������S2�����Ũ�ȵĶ���ֵlgc(S2��)��lgc(M2��)�Ĺ�ϵ��ͼ��ʾ������˵������ȷ����(����)
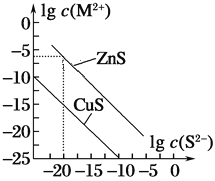
A.��Cu2��Ũ��Ϊ1��10��5 mol��L��1�Ĺ�ҵ��ˮ�м���ZnS��ĩ������CuS��������
B.25 ��ʱ��Ksp(CuS)ԼΪ1��10��35
C.��100 mL Zn2����Cu2��Ũ�Ⱦ�Ϊ1��10��5 mol��L��1�Ļ����Һ����μ���1��10��4 mol��L��1��Na2S��Һ��Cu2���ȳ���
D.Na2S��Һ�У�c(S2��)��c(HS��)��c(H2S)��2c(Na��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ִ������а�����Խ��Խ��Ҫ�Ľ�ɫ������β����̼�⻯����������Pһ����̼�ȣ������Ļ�����ȾԽ��Խ���ԣ������������ŷ��ѳ�Ϊ���д�����Ⱦ����Ҫ��Դ��
��1�������ͳɷ�ΪC8H18�������������������ѽ��������Ͷ�ϩ��д���÷�Ӧ�Ļ�ѧ����ʽ____
��2������������NO�ķ�ӦΪ��N2(g)+O2(g) ![]() 2NO(g) ��H ��0
2NO(g) ��H ��0
�������������������¶�Խ�ߣ���λʱ����NO�ŷ���Խ��ԭ����___________��
��1mol�����к���0.8molN2��0.2molO2��1300��ʱ�ں�1mol�������ܱ������ڷ�Ӧ�ﵽƽ�⡣���NOΪ8��10��4mol��������¶��µ�ƽ�ⳣ��K��_____________��
��3��β���е�CO��Ҫ���������Ͳ���ȫȼ�ա�
���������밴���з�Ӧ��ȥCO��2CO(g)=2C(s)+O2(g) ��H=+221kJ��mol��1, �����������ܷ�ʵ�ֵ����ݣ�______________��
�ڲ�������β����Ũ�ȳ��õ绯ѧ����������������CO������������ͼ��ʾ�������������ĵ缫��ӦΪ______��

��4��������β��ϵͳ�а�װ��ת����������Ч����β���е�CO��NOx ��̼�⻯����ȷ�����
��֪��N2(g)��O2(g)=2NO(g) ��H1=��180kJ/mol
CO(g) ��1/2O2(g)= CO2(g) ��H2=��283kJ/mol
2NO(g)�� 2CO(g) = 2CO2(g) �� N2(g) ��H3
����H3 =__________kJ��mol��1��
��5���⻯ѧ��������������ȩ�ࡢ���������������ȣ�������β���������������·����⻯ѧ��Ӧ���ɵĶ�����Ⱦ�д��2����ϩ����������ʵ���֮��Ϊ1��2��Ӧ������ȩ�������Ļ�ѧ����ʽ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2019��4�£���Զ���⽨��������������Ŀ����Ч�����Ͼ���ɫ��Ⱦ���⡣��֪�Ͼ�������������ţ���ṹ��ͼ��ʾ�������ʸ߶��°�������˵����ȷ���ǣ� ��
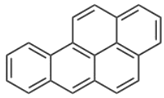
A. �����ʵķ���ʽΪC20H18
B. �÷���������̼ԭ�ӹ���
C. ��������Ϊ����ͬϵ��
D. �÷�����ʹ������Ȼ�̼��Һ��ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ۺ�����������ĩ�Ļ���ﹲ9.2�ˣ����뵽150������ϡ�����У�ǡ����ȫ��Ӧ���õ�����2.24��(��״��)����
��1�������������������___
��2��ԭϡ��������ʵ���Ũ�ȣ�___
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com