
【题目】(1)X、Y、Z三种物质存在如图所示转化。回答下列问题。
若X为黑色固体单质,A为O2,写出Z→Y的化学方程式_________________。
②若X为NaOH溶液,则写出Y→Z的化学方程式_______________________。
(2)已知常温下在溶液中可发生如下两反应:
Ce4++Fe2+=Fe3++Ce3+;Sn2++2Fe3+=2Fe2++Sn4+
由此可以确定Ce4+、Sn4+、Fe3+三种离子的氧化性由强到弱的顺序是 。
(3)Mn2+、Bi3+、BiO3-、MnO4-、H+、H2O组成的一个氧化还原反应体系中,发生BiO3-→Bi3+的反应过程。
①该反应中,被氧化的元素是_____________,氧化剂是_______________。
将以上物质分别填入下面对应的横线上,组成一个未配平的化学方程式。
________+ ______+ ________![]() ______+ ________+ H2O
______+ ________+ H2O
反应中若产生0.2mol的还原产物,则有_______mol电子转移。
【答案】(1)①CO2+C![]() 2CO;②CO2+Na2CO3+H2O=2NaHCO3;
2CO;②CO2+Na2CO3+H2O=2NaHCO3;
(2)Ce4+>Fe3+>Sn4+;
(3)①Mn,BiO3-;②BiO3-+Mn2++H+![]() Bi3++MnO4-+H2O;③0.4。
Bi3++MnO4-+H2O;③0.4。
【解析】
试题分析:(1)①X是黑色固体单质,因此X为C,Z为CO2,Y为CO,因此反应方程式为:CO2+C![]() 2CO;②X为NaOH,A为CO2,因此Y为Na2CO3,Z为NaHCO3,因此反应方程式N2CO3+CO2+H2O=2NaHCO3;(2)根据氧化剂的氧化性强于氧化产物的氧化性,Ce4+化合价降低,作氧化剂,Fe2+化合价升高,Fe3+作氧化产物,即Ce4+>Fe3+,Sn2+的化合价升高,作还原剂,Sn4+作氧化产物,Fe3+作氧化剂,Fe3+>Sn4+,因此有Ce4+>Fe3+>Sn4+;(3)①被氧化的元素,失去电子化合价升高,BiO3-→Bi3+,化合价降低,因此Mn的化合价升高,Mn被氧化,氧化剂是得到电子,化合价降低,即BiO3-作氧化剂;②根据①的分析,Mn2++BiO3-+H+→MnO4-+Bi3++H2O;③还原产物是Bi3+,转移电子物质的量为0.2×(5-3)mol=0.4mol。
2CO;②X为NaOH,A为CO2,因此Y为Na2CO3,Z为NaHCO3,因此反应方程式N2CO3+CO2+H2O=2NaHCO3;(2)根据氧化剂的氧化性强于氧化产物的氧化性,Ce4+化合价降低,作氧化剂,Fe2+化合价升高,Fe3+作氧化产物,即Ce4+>Fe3+,Sn2+的化合价升高,作还原剂,Sn4+作氧化产物,Fe3+作氧化剂,Fe3+>Sn4+,因此有Ce4+>Fe3+>Sn4+;(3)①被氧化的元素,失去电子化合价升高,BiO3-→Bi3+,化合价降低,因此Mn的化合价升高,Mn被氧化,氧化剂是得到电子,化合价降低,即BiO3-作氧化剂;②根据①的分析,Mn2++BiO3-+H+→MnO4-+Bi3++H2O;③还原产物是Bi3+,转移电子物质的量为0.2×(5-3)mol=0.4mol。


 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.化学反应中,物质变化的同时不一定发生能量变化
B.反应焓变(△H)的大小与方程式中各物质的化学计量系数无关
C.反应产物的总焓大于反应物的总焓时,反应吸热,△H>0
D.吸热反应中,形成化学键释放的能量大于断裂化学键吸收的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对外加电流的金属保护中,被保护的金属( )
A. 与电源的正极相连 B. 表面上发生氧化反应
C. 与电源的负极相连 D. 与另一种活泼性较差的金属相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关原子结构的说法,正确的是 ( )
A. 稀有气体元素原子的最外层电子数都是8 B. 非金属元素的最外层电子数都大于3
C. 金属元素的最外层电子数都小于4 D. 氢原子的电子云是球形对称的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于分液漏斗的使用,下列说法正确的是( )
A. 可在分液漏斗内用四氯化碳萃取碘酒中的碘单质
B. 分液漏斗在使用前只需检查旋塞芯处是否漏水即可
C. 在分液漏斗中加入萃取剂后应上下颠倒摇匀使萃取剂与溶质充分接触
D. 放出下层液体时,应打开上方的玻璃塞,并使下端管口紧贴烧杯内壁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酸广泛应用于制药和化工行业,某同学尝试用甲苯的氧化反应制备苯甲酸。反应原理:
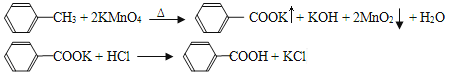
己知甲苯的熔点为-95°C,沸点为110.6°C,易挥发,密度为0.866g/cm3;苯甲酸的熔点为122.4°C,在25°C和95°C下溶解度分别为0.3g和6.9g。
【制备产品】将30.0mL甲苯和25.0mLlmol/L高锰酸钾溶液在100°C下反应30min,装置如图所示。
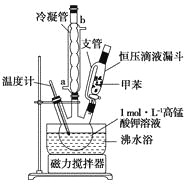
(1)图中冷凝管的进水口为________(填“a”或“b”)。支管的作用是___________。
(2)在本实验中,三领烧瓶最合适的容积___________(填字母)。
A.50mL | B.I00mL | C.200mL | D.250mL |
相对于用酒精灯直接加热,用沸水浴加热的优点是___________________。
【分离产品】该同学设计如下流程分离粗产品苯甲酸和回收甲苯
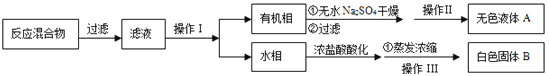
(3)操作Ⅰ的名称是 ;含有杂志的产物经操作Ⅱ进一步提纯得无色液体甲苯,则操作Ⅱ的名称是 。
(4)测定白色固体的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,该同学推测白色固体是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确。请完成表中内容。
序号 | 实验方案 | 实验现象 | 结论 |
① | 将白色固体加入水中,加热溶解,______。 | 得到白色晶体和无色溶液 | |
② | 取少重滤液于试管中,________。 | 生成白色沉淀 | 滤液含Cl- |
③ | 干燥白色晶体,________。 | _____________________ | 白色晶体是苯甲酸 |
纯度测定:称取1.220g产品,配成100ml甲醇溶液,取25.00ml溶液,用0.1000mol/L KOH标准溶液滴定,重复滴定四次,每次消耗的体积如下表所示。
第一次 | 第二次 | 第三次 | 第四 | |
体积(mL) | 24.00 | 24.10 | 22.40 | 23.90 |
(5)滴定操作中,如果对装有KOH标准溶液的滴定管读数时,滴定前仰视,滴定后俯视则测定结果______________(填“偏大”、“偏小”或“不变”)。计算样品中苯甲酸纯度为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示装置,室温下密闭容器内分别充入空气和H2、O2的混合气体在可移动的活塞两边,在标准状况下若将H2、O2的混合气体点燃引爆,活塞先左移,恢复原温度后,活塞右移并停留于容器的中央,则原来H2、O2的体积比最接近于( )
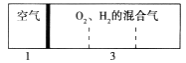
①2:7 ②5:4 ③4:5 ④7:2
A.①② B.③④ C.②④ D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】容量瓶是一种定量仪器,其瓶身上标有:①温度、②浓度、③容量、④压强、⑤刻度线、⑥密度
这六项中的( )
A.②④⑥
B.③⑤⑥
C.①②④
D.①③⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com