
【题目】二甲醚作为燃料电池的原料,可通过以下途径制取:
I.2CO(g)+4H2(g)![]() CH3OCH3(g)+H2O(g) ΔH
CH3OCH3(g)+H2O(g) ΔH
II.2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g) ΔH
CH3OCH3(g)+3H2O(g) ΔH
(1)已知:①CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH1=-41.0kJ·mol-1
CO2(g)+H2(g) ΔH1=-41.0kJ·mol-1
②CO2(g)+3H2(g)![]() CH3OH(g)+ H2O(g) ΔH2=-49.0kJ·mol-1
CH3OH(g)+ H2O(g) ΔH2=-49.0kJ·mol-1
③CH3OCH3(g)+ H2O(g)![]() 2CH3OH(g) ΔH3=+23.5kJ·mol-1
2CH3OH(g) ΔH3=+23.5kJ·mol-1
则反应I的ΔH=_______kJ·mol-1
(2)在恒容密闭容器里按体积比为1:2充入一氧化碳和氢气发生反应2CO(g)+4H2(g)![]() CH3OCH3(g)+H2O(g),一定条件下反应达到平衡状态。当改变反应的某一个条件后,下列变化能说明平衡一定向正反应方向移动的是________。
CH3OCH3(g)+H2O(g),一定条件下反应达到平衡状态。当改变反应的某一个条件后,下列变化能说明平衡一定向正反应方向移动的是________。
A.新平衡后c(CH3OCH3)增大
B.正反应速率先增大后减小
C.反应物的体积百分含量减小
D.化学平衡常数K值增大
(3)在10L恒容密闭容器中,均充入4molCO2和7molH2,分别以铱(Ir)和铈(Ce)作催化剂,通过反应II:2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g)制二甲醚,反应进行相同的时间后测得的CO2的转化率α(CO2)随反应温度的变化情况如图所示。
CH3OCH3(g)+3H2O(g)制二甲醚,反应进行相同的时间后测得的CO2的转化率α(CO2)随反应温度的变化情况如图所示。
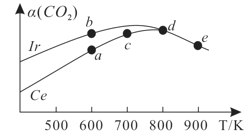
①根据图1,下列说法不正确的是________。
A.反应II的ΔH<0,ΔS>0
B.600K时,H2的速率:v(b)正>v(a)逆
C.分别用Ir、Ce作催化剂时,Ce使反应II的活化能降低更多
D.从状态d到e,α(CO2)减小的原因可能是温度升高平衡逆向移动
②状态e(900K)时,α(CO2)=50%,则此时的平衡常数K=______(保留3位有效数字)。
(4)写出二甲醚碱性(电解质溶液为KOH溶液)燃料电池的负极电极反应式__________。该电池工作时,溶液中的OH-向______极移动,该电池工作一段时间后,测得溶液的pH减小。
(5)己知参与电极反应的电极材料单位质量放出电能的大小称为该电池的比能量.关于二甲醚碱性燃料电池与乙醇碱性燃料电池,下列说法正确的是________。
A.两种燃料互为同分异构体,分子式和摩尔质量相同,比能量相同
B.两种燃料所含共价键数目相同,断键时所需能量相同,比能量相同
C.两种燃料所含共价键类型不同,断键时所需能量不同,比能量不同
【答案】-203.5 BD A、C 6.75×104 CH3OCH3+16OH--12e-=2CO32-+11H2O 负极 C
【解析】
(1)根据盖斯定律,①×2+②×2-③可得反应I,所以△H=(-41.0 kJmol-1)×2+(-49.0kJmol-1)×2-(+23.5kJmol-1)=-203.5kJmol-1;
(2)A.向平衡体系中再充入一定量的CH3OCH3气体,平衡逆向移动,但新平衡c(CH3OCH3)增大,故A不选;
B.正反应速率先增大后减小说明正反应速率大于逆反应速率,平衡正向移动,故B选;
C.移走反应物可以使反应物的体积百分含量减小,但平衡会逆向移动,故C不选;
D.该反应焓变小于零,正反应为放热反应,K值增大说明温度降低,降低温度会使平衡正向移动,故D选;
综上所述选BD;
(3)据图可知随温度上升二氧化碳的转化率先上升后下降,说明在温度较低时相同时间内反应还未达到平衡,平衡后随温度上升二氧化碳转化率随温度上升而下降;
①A.由图中信息可知,当温度高于800K时,CO2转化率α(CO2)随反应温度升高而减小,说明该反应为放热反应,△H>0,同时该反应气体体积减小,△S<0,故A错误;
B.由图可知,b点CO2转化率α(CO2)大于a点,所以生成物浓度b点大于a点,故v(b)逆>v(a)逆,由于b点未平衡且正向进行,v(b)正>v(b)逆,所以v(b)正>v(a)逆,故B正确;
C.由图中信息可知,当温度为400K~800K时,反应进行相同时间后测得Ir作催化剂的CO2转化率α(CO2)较高,说明Ir的催化效率更高,所以用Ir、Ce作催化剂时,反应的活化能降低更多的是Ir,故C错误;
D.状态d、e都是平衡状态,从d到e,该反应为放热反应,升温平衡逆向移动,α(CO2)减小,故D正确。
故答案为:AC;
②初始投料为4molCO2和7molH2,状态e(900K)时,α(CO2)=50%,则转化的CO2为2mol,列三段式有:

容器的体积为10L,则平衡常数K=![]() =6.75×104;
=6.75×104;
(4)二甲醚燃料电池中二甲醚被氧化生成二氧化碳,所以通入二甲醚的电极为负极,得电子发生还原反应,由于电解质为KOH溶液,所以最终产物为碳酸根,电极方程式为:CH3OCH3+16OH--12e-=2CO32-+11H2O;该电池工作时为原电池,原电池中阴离子流向负极;
(5)不同的化学键断裂或形成时的能量变化不同,二甲醚和乙醇虽然为同分异构体且摩尔质量相同,但分子中化学键类型不同,所以单位质量的二甲醚和乙醇反应过程中放出的能量不同,所以C正确。


科目:高中化学 来源: 题型:
【题目】25℃,向20.00mL 0.100 mol·L![]() HX中滴加0.100 mol·L
HX中滴加0.100 mol·L![]() NaOH过程中,pH变化如下图所示。
NaOH过程中,pH变化如下图所示。
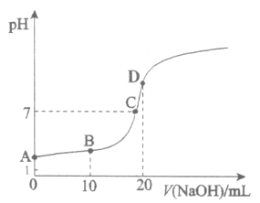
(1)写出HX的电离方程式:__________。
(2)下列有关B点溶液的说法正确的是__________(填字母序号)。
a. 溶质为:HX、NaX
b. 微粒浓度满足:c(Na+)+c(H+)=c(X-)+c(OH-)
c. 微粒浓度满足:c(Na+)=c(HX)+c(X-)
d. 微粒浓度满足:c(X-)>c(Na+)>c(H+)>c(OH-)
(3)A、C两点水的电离程度:A__________C(填“>”、“<”或“=”)。
(4)C点对应离子浓度由大到小的顺序为__________。
(5)用离子方程式解释D点溶液pH>7的原因:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】治理SO2、CO、NOx污染是化学工作者研究的重要课题。
Ⅰ.硫酸厂大量排放含SO2的尾气会对环境造成严重危害。
(1)工业上可利用废碱液(主要成分为Na2CO3)处理硫酸厂尾气中的SO2,得到Na2SO3溶液,该反应的离子方程式为______。
Ⅱ.沥青混凝土可作为反应;2CO(g)+O2(g)2CO2(g)的催化剂。如图表示在相同的恒容密闭容器、相同起始浓度、相同反应时间段下,使用同质量的不同沥青混凝土(α型、β型)催化时,CO的转化率与温度的关系。
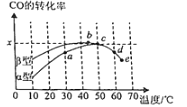
(2)a、b、c、d四点中,达到平衡状态的是______。
(3)已知c点时容器中O2浓度为0.02molL-1,则50℃时,在α型沥青混凝土中CO转化反应的平衡常数K=______(用含x的代数式表示)。
(4)观察分析图,回答下列问题:

①CO转化反应的平衡常数K(a)______K(c)。
②在均未达到平衡状态时,同温下β型沥青混凝土中CO转化速率比α型要______(填“大”、“小”)。
③______点时CO与O2分子之间发生有效碰撞的几率在整个实验过程中最高。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄酒中的酒精是葡萄果实中的糖发酵后的产物(C6H12O6![]() 2CH3CH2OH+2CO2↑)。
2CH3CH2OH+2CO2↑)。
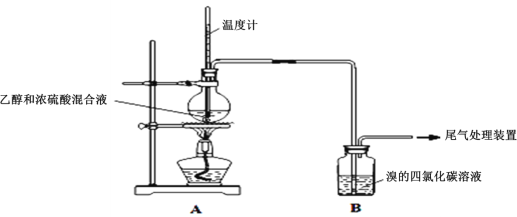
Ⅰ.已知:实验室制乙烯原理为CH3CH2OH![]() CH2=CH2↑+H2O,产生的气体能使Br2的四氯化碳溶液褪色,甲、乙同学用下列实验验证。(气密性已检验,部分夹持装置略)。实验操作和现象:
CH2=CH2↑+H2O,产生的气体能使Br2的四氯化碳溶液褪色,甲、乙同学用下列实验验证。(气密性已检验,部分夹持装置略)。实验操作和现象:
操作 | 现象 |
点燃酒精灯,加热至170℃ | Ⅰ:A中烧瓶内液体渐渐变黑 Ⅱ:B内气泡连续冒出,溶液逐渐褪色 |
…… | |
实验完毕,清洗烧瓶 | Ⅲ:A中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 |
(1)溶液“渐渐变黑”,说明浓硫酸具有___性。
(2)对产生的气体进行分析,甲认为是C2H4,乙认为不能排除SO2的作用。
①写出实验室制取SO2的化学反应方程式是___;
②乙根据现象认为实验中产生的SO2和___,使B中有色物质反应褪色。
③为证实各自观点,甲、乙重新实验,设计与现象如下:
甲:在A、B间增加一个装有某种试剂的洗气瓶;现象:Br2的CCl4溶液褪色。
乙:用下列装置按一定顺序与A连接:(尾气处理装置略)
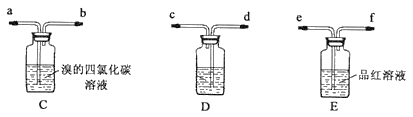
现象:C中溶液由红棕色变为浅红棕色时,E中溶液褪色。
请回答下列问题:
a.甲设计实验中A、B间洗气瓶中盛放的试剂是___;乙设计的实验D中盛放的试剂是___,装置连接顺序为___ (用仪器接口字母编号)。
b.能说明确实是SO2使E中溶液褪色的实验是___。
c.乙为进一步验证其观点,取少量C中溶液,加入几滴BaCl2溶液,振荡,产生大量白色沉淀,浅红棕色消失,发生反应的离子方程式是___。由此可得出的干燥的SO2不能使Br2的四氯化碳溶液褪色。
Ⅱ.葡萄酒中常用Na2S2O5做抗氧化剂。
(3)0.5molNa2S2O5溶于水配成1L溶液,该溶液的pH=4.5。溶液中部分微粒浓度随溶液酸碱性变化如图所示。写出Na2S2O5溶于水时溶液中离子浓度由大到小的排列顺序___。
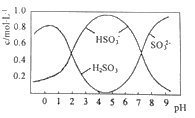
(4)已知:Ksp[BaSO4]=1×10-10,Ksp[BaSO3]=5×10-7。把部分被空气氧化的该溶液的pH调为10,向溶液中滴加BaCl2溶液使SO42-沉淀完全[c(SO42-)≤1×10-5mol·L-1],此时溶液中c(SO32-)≤___mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种钌(Ru)基配合物光敏染料敏化太阳能电池的工作原理及电池中发生的主要反应如图所示。下列说法错误的是

A. 电池工作时,光能转变为电能,X为电池的负极
B. 镀铂导电玻璃上发生氧化反应生成I-
C. 电解质溶液中发生反应:2Ru3++3I-![]() 2Ru2++I3-
2Ru2++I3-
D. 电池工作时,电解质溶液中I-和I3-的浓度基本不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是制备和研究乙炔性质的实验装置图。下列说法不正确的是
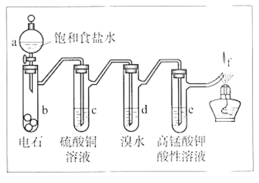
A.制备乙炔的反应原理是CaC2+2H2O→Ca(OH)2+C2H2↑
B.c的作用是除去影响后续实验的杂质
C.e中的现象说明乙炔能被高锰酸钾酸性溶液氧化
D.f处观察到的现象是安静燃烧,火焰呈淡蓝色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、R、D都是周期表中前四周期的元素,它们的原子系数依次增大。其中A元素基态原子第一电离能比B元素基态原子的第一电离能大,B的基态原子的L层、R基态原子的M层均有2个单电子,D是第Ⅷ族中原子序数最小的元素。
(1)写出基态D原子的电子排布式__________。
(2)已知高纯度R的单质在现代信息技术与新能源开发中具有极为重要的地位。工业上生产高纯度R的单质过程如下:
![]()
写出过程③的反应方程式___________,已知RHCl3的沸点是31.5oC,则该物质的晶体类型是__________,中心原子的轨道杂化类型为__________,该物质的空间构型是______。
(3)A的第一电离能比B的第一电离能大的原因是_________,A、B两元素分别与R形成的共价键中,极性较强的是________。A、B两元素间能形成多种二元化合物,其中与A3-互为等电子体的物质的化学式为_______。
(4)已知D单质的晶胞如图所示,则晶体中D原子的配位数为______,一个D的晶胞质量为____,已知D原子半径为r pm,则该晶胞的空间利用率为_____________ (写出计算过程)。
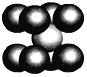
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高分子材料聚酯纤维H的一种合成路线如下:

已知:CH2=CHCH3![]() CH2=CHCH2Cl+HCl
CH2=CHCH2Cl+HCl
请回答下列问题:
(1)C的名称是____,D的结构简式为____。
(2)E—F的反应类型是____,E分子中官能团的名称是 ___。
(3)写出C和G反应生成H的化学方程式____。
(4)在G的同分异构体中,同时满足下列条件的结构有 ___种(不考虑立体异构)。
①属于芳香族化合物,能发生银镜反应和水解反应,遇FeCl3溶液发生显色反应
②1mol该有机物与3molNaOH恰好完全反应
③分子结构中不存在![]()
其中,核磁共振氢谱显示4组峰的结构简式为____。
(5)参照上述流程,以1-丁烯为原料合成HOCH2(CHOH)2CH2OH,设计合成路线____(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】EDTA(乙二胺四乙酸)是一种能与Ca2+、Mg2+等结合的螯合剂。某高三研究性学习小组在实验室制备EDTA,并用其测定某地下水的硬度。制备EDTA的实验步骤如下:
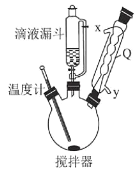
步骤1:称取94.5g(1.0mol)ClCH2COOH于1000mL三颈烧瓶中(如图),慢慢加入50%Na2CO3溶液,至不再产生无色气泡;
步骤2:加入15.6g(0.26mol)H2NCH2CH2NH2,摇匀,放置片刻,加入2.0mol·L-1NaOH溶液90mL,加水至总体积为600mL左右,温度计50℃加热2h;
步骤3:冷却后倒入烧杯中,加入活性炭脱色,搅拌、静置、过滤。用盐酸调节滤液至pH=1,有白色沉淀生成,抽滤,干燥,制得EDTA。测地下水硬度:取地下水样品250mL进行预处理后,用EDTA进行检测。实验中涉及的反应有M2+(金属离子)+Y4-(EDTA)=MY2-;M2+(金属离子)+EBT(铬黑T,蓝色)=MEBT(酒红色);MEBT+Y4-(EDTA)=MY2-+EBT(铬黑T)。
回答下列问题:
(1)步骤1中发生反应的离子方程式为_____。
(2)仪器Q的名称是_____,冷却水从_____接口(填“x”或“y”)流出。
(3)用NaOH固体配制上述NaOH溶液,配制时使用的仪器有托盘天平、药匙、烧杯、玻璃棒、_____和_____,需要称量NaOH固体的质量为_____。
(4)将处理后的水样转移到锥形瓶中,加入氨水-氯化铵缓冲溶液调节pH为10,滴加几滴铬黑T溶液,用0.0100mol·L-1EDTA标准溶液进行滴定。
①确认达到滴定终点的现象是_____。
②滴定终点时共消耗EDTA溶液15.0mL,则该地下水的硬度=_____度(水硬度的表示方法是将水中的Ca2+和Mg2+都看作Ca2+,并将其折算成CaO的质量,通常把1L水中含有10mgCaO称为1度)。
③若实验时装有EDTA标准液的滴定管只用蒸馏水洗涤而未用标准液润洗,则测定结果将_____ (填“偏大“偏小”或“无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com