
����Ŀ���������仯����������������������Ҫ����;���ش��������⣺
��1����������Ԫ��ǿ�ᣬ�������ǿ��ʱ�ɷ������Ӽ����ˮ���ɽ����ᣨH4P2O7�����������ᣨH5P3O10������ֱ��������ᣮ��ֱ��������������Pԭ����Ϊ20ʱ���仯ѧʽ��_________��ֱ��������᳣������ȡ��ȼ��
��2��PH3��һ���������õ�Ѭ���������ڳ��δ����ﺦ�森
����ͬ����Ԫ�ص��⻯��NH3��ȣ��е㣺PH3 ___NH3�������������=�������ȶ��ԣ�PH3 __NH3�����������������=������ ʵ������ȡPH3��ѡ��PH4I��______����������𣩷�Ӧ�õ���
��PH3���巢�����г�������ˮ�⣬�仯ѧ��Ӧ����ʽ��_____________��
��3��������������������Һ��Ӧ����ˮƿ���ڱڶ������������Ͽ�֪��������Һ�д���ƽ�⣺Ag+��aq��+2NH3��aq��Ag��NH3��2+��aq�����÷�Ӧƽ�ⳣ��K��[Ag��NH3��2+]=1.10��107������֪Ksp[AgCl]=1.45��10��20��������淴ӦAgCl��s��+2NH3��aq��Ag��NH3��2+��aq��+Cl����aq���Ļ�ѧƽ�ⳣ��K=________������2λ��Ч���֣���1L 1mol/L��ˮ���������ܽ�AgCl____mol������2λ��Ч���֣���
��4�������ӹ�ҵ��NF3�������������ʴ�̼�����ҵ��ͨ����⺬NH4F�ȵ���ˮ����������NF3������ԭ����ͼ��ʾ��
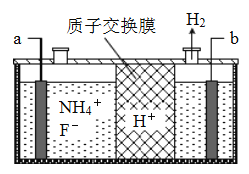
a�缫Ϊ���ص�___���������������������缫��ӦʽΪ____________________���������л����������������Լ�ǿ�����嵥�ʣ�������ķ���ʽ��______��
���𰸡� H22P20O61 �� �� �� AlP+3H2O=Al��OH��3��+PH3�� 1.6��10��3 0.04 �� NH4++3F����6e��=NF3+4H+ F2
����������1�������ӵ�������ȥһ���ӵ�ˮ��������������ȥ�����ӵ�ˮ�����߾�������Pԭ����Ϊ20ʱ��Ϊ20��������Ӽ���ȥ19��ˮ���ӣ������ԭ���غ��֪�߾�����ķ���ʽΪ��H22P20O61����2����NH3����֮����γ�������ʷе�ߣ���Ԫ�طǽ�����ǿ����NH3�ȶ���ǿ��ʵ������ȡPH3������NH3���ƣ���ʵ������ȡPH3��ѡ��PH4I��Ӧ��������ˮ��ķ���ʽΪAlP+3H2O��Al��OH��3��+PH3������3��Ag+��aq��+2NH3��aq��Ag��NH3��2+��aq����AgCl��s��Ag+��aq��+Cl-��aq����ӿ��Եõ���AgCl��s��+2NH3��aq��Ag��NH3��2+��aq��+Cl-��aq����ƽ�ⳣ������ʽK=c([Ag(NH3)2]+)c(Cl)/c2(NH3)��c([Ag(NH3)2]+)c(Cl)��c��Ag+��/c2(NH3)��c��Ag+����1.10��107��1.45��10-10=1.6��10-3�����ܽ�xmolAgCl����Ag(NH3)2]+Ϊxmol/L��Cl-Ϊxmol/L����Һ��NH3��aq��Ϊ��1-2x��mol/L����x2/(12x)2=1.6��10-3�����x=0.04����4����ͼ��֪����������b���õ�����������������bΪ��������ôaΪ������������笠�ʧȥ��������NF3���缫��Ӧ����ʽΪ��NH4++3F����6e����NF3+4H+�����ݵ��ԭ����֪��������Ҳ����ʧȥ�������ɷ����ʣ��������Խ�ǿ�ĵ���Ϊ������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ����CO��H2Ϊԭ�Ϻϳɼ״��ķ�Ӧ��CO(g)+2H2(g)![]() CH3OH(g) ��H��0�����ݻ�Ϊ1 L�ĺ��������У��ֱ���T1��T2��T3�����¶��ºϳɼ״�����ͼ�����������¶��²�ͬH2��CO����ʼ��ɱȣ���ʼʱCO�����ʵ�����Ϊ1mol����COƽ��ת���ʵĹ�ϵ������˵����ȷ����
CH3OH(g) ��H��0�����ݻ�Ϊ1 L�ĺ��������У��ֱ���T1��T2��T3�����¶��ºϳɼ״�����ͼ�����������¶��²�ͬH2��CO����ʼ��ɱȣ���ʼʱCO�����ʵ�����Ϊ1mol����COƽ��ת���ʵĹ�ϵ������˵����ȷ����
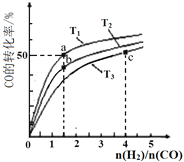
A. H2ת���ʣ�a��b��c
B. ���������¶�֮���ϵΪT1��T2��T3
C. a��״̬����ͨ��0.5 mol CO��0.5 mol CH3OH��ƽ�����������ƶ�
D. c��״̬����ͨ��1 molCO��4 mol H2����ƽ����CH3OH�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ��������84����Һ��˵���е��䷽������NaClO��������480mL��NaClO25%���ܶ�Ϊ1.19g/cm3������Һ������˵����ȷ����
A. ���ƹ���ֻ��Ҫ���������������
B. ����ƿ������ˮϴ��������ɲ���������Һ������
C. ����ʱ��������ƿ�Ŀ̶��ߣ������������Һ���ʵ���Ũ��ƫ��
D. ����������ƽ������NaClO���������Ϊ148.8g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��
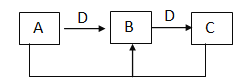
��AΪ�������壬DΪ�������ʣ������Ϸ�Ӧ��Ϊ������ԭ��Ӧ����B�ǣ�___________D�ǣ�_____(��ѧʽ)
��DΪNaOH�������Ϸ�Ӧ��Ϊ��������ԭ��Ӧ����A��B��C������ͬһ�ֽ���Ԫ�صĻ������A�ǣ�______��(��ѧʽ) B��D��Ӧ�Ļ�ѧ����ʽ��______________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ����һ���������ォ��ˮ�е�����(H2NCONH2)ֱ��ת��Ϊ�Ի����Ѻ����ʵ�ԭ���װ�á������ü�װ�ò����ĵ��ܶ���װ���еı���ʳ��ˮ���е��(A��B��Ϊʯī�缫)������˵���в���ȷ���ǣ� ��

��M�缫��Ӧʽ��H2NCONH2+H2O+6e-=CO2��+N2��+6H+
�ڵ�A�缫����11.2mL����(���)ʱ����N�缫����25��10-4mol����
�ۼ���H+�����ӽ���Ĥ���������ƶ�
��A�缫Ӧ��X������
�ݷ�Ӧһ��ʱ�����װ��U���е���ҺpH���
A. �٢� B. �٢ۢ� C. �٢ڢ� D. �ڢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ͼʾ���ó��Ľ��۲���ȷ����

A. ͼ����CO(g)+H2O(g)![]() CO2(g)+H2(g)��ƽ�ⳣ���뷴Ӧ�¶ȵĹ�ϵ������˵���÷�Ӧ����H<0
CO2(g)+H2(g)��ƽ�ⳣ���뷴Ӧ�¶ȵĹ�ϵ������˵���÷�Ӧ����H<0
B. ͼ����������H2O2���ֽ�ų������ķ�Ӧ��c(H2O2 )�淴Ӧʱ��仯��������˵�����ŷ�Ӧ�Ľ���H2O2�ֽ�������С
C. ͼ������������0.1000 mol��L1NaOH��Һ�ζ�20.00 mL 0.1000 mol��L1ijһԪ��HX�ĵζ�������˵��HX��һԪǿ��
D. ͼ������������Na2SO4��ȥ��Һ��Ba2+�ﵽ�����ܽ�ƽ��ʱ����Һ��c(Ba2+ )��c(SO42)�Ĺ�ϵ������˵����Һ��c(SO42 )Խ��c(Ba2+ )ԽС
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ģ������ģ�һ���¶������������ݻ���ͬ�ĺ����ܱ������а���ͬ��ʽͶ�뷴Ӧ����������Ӧ2SO2(g)+ O2(g)![]() 2SO3(g)(����Ӧ����)����÷�Ӧ���������������
2SO3(g)(����Ӧ����)����÷�Ӧ���������������
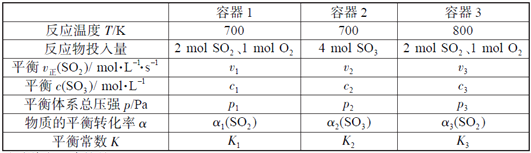
����˵����ȷ����
A. v1< v2��c2< 2c1 B. K1> K3��p2> 2p3
C. v1< v3����1(SO2 ) >��3(SO2 ) D. c2> 2c3����2(SO3 )+��3(SO2 )<1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ��װ�ò��ܴﵽʵ��Ŀ�ĵ���
A | B | C | D |
|
|
|
|
ʵ������ȡ����ˮ | ��SO2��NaOH��Һ����Ȫʵ�� | ֤��Na2CO3�����ȶ��Ա�NaHCO3�� | ֤��ͭ��Ũ����ķ�Ӧ�Ƿ��ȷ�Ӧ |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com