
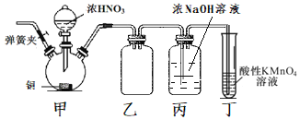
【题目】工业上亚硝酸钠可用作媒染剂、缓蚀剂等。实验室以铜、浓硝酸、氢氧化钠为原料制备亚硝酸钠的装置如图所示(部分夹持装置略)。已知:NO和NO2均能被酸性KMnO4溶液氧化为NO3-。
(1)连接装置后首先要进行的操作是___,然后装入药品。
(2)装置甲中反应的离子方程式为___。
(3)装置乙的作用是___。
(4)实验结束后,打开甲装置的弹簧夹,通入N2,其目的是___。
(5)装置丁的作用是___。
(6)为了测定丙中NaNO2的浓度,取丙中溶液20.00mL,用0.1000mol/L的酸性KMnO4溶液进行滴定,消耗KMnO4溶液10.00mL。请回答:
①酸性KMnO4溶液盛放在___滴定管中。
②判断滴定达终点时的依据为___。
③写出上述反应的离子方程式___,计算出NaNO2的浓度为___mol/L。
④配制酸性KMnO4溶液定容时,俯视容量瓶的刻度线,NaNO2的浓度___。(填“偏高”、“偏低”或“无影响”)
【答案】检查装置的气密性 Cu+4H++2NO3-=Cu2++2NO2↑+2H2O 安全瓶,防止倒吸 排尽装置中残留有毒气体(防止污染环境) 吸收尾气,防止污染环境 酸式 当滴入最后一滴标准液后,锥形瓶中的溶液由无色变为紫色,且半分钟内不褪 5NO2+2MnO4-+6H+=5NO3-+2Mn2++3H2O 0.125 偏低
【解析】
甲装置由Cu和浓硝酸制备NO2,乙装置为安全瓶防止NO2与氢氧化钠溶液反应而产生倒吸,丙装置由NO2和NaOH制备NaNO2,丁装置用酸性高锰酸钾吸收未反应完的NO2和生成的NO气体,据此解答。
(1)装置中有气体参与,故连接好装置之后,应检查装置气密性;
(2)铜和浓硝酸反应生成硝酸铜、二氧化氮和水,离子反应方程式为:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O;
(3)为防止NO2与氢氧化钠溶液反应而产生倒吸,因此装置乙的作用是安全瓶,防止倒吸;
(4)实验中产生的NO和NO2有毒,不能排放到空气中,要全部除去,打开甲装置的弹簧夹,通入N2,其目的是排尽装置中残留有毒气体(防止污染环境);
(5)装置丁的作用是吸收尾气,防止污染环境;
(6)①酸性KMnO4溶液具有氧化性,只能使用酸式滴定管盛装;
②酸性KMnO4自身可做指示剂,当滴入最后一滴标准液后,锥形瓶中的溶液由无色变为紫色,且半分钟内不褪,即为达到终点;
③亚硝酸根离子与酸性高锰酸钾发生氧化还原反应得到硝酸根离子和锰离子,离子反应为:5NO2+2MnO4-+6H+=5NO3-+2Mn2++3H2O,滴定时消耗KMnO4溶液10.00mL,高锰酸钾的物质的量=0.01L×0.1000mol/L=0.001mol,则亚硝酸钠的物质的量=![]() ×0.001mol=0.0025mol,其浓度为
×0.001mol=0.0025mol,其浓度为![]() =0.125mol/L;
=0.125mol/L;
④配制酸性KMnO4溶液定容时,俯视容量瓶的刻度线,高锰酸钾溶液的体积偏小,浓度偏大,滴定时消耗高锰酸钾的体积偏小,计算的NaNO2的浓度偏低。


科目:高中化学 来源: 题型:
【题目】(1)某温度(t℃)时,测得0.01mol/L的NaOH溶液的pH=11,则该温度下水的KW=_______。在此温度下,将pH=a的NaOH溶液Va L与pH=b的H2SO4溶液Vb L混合,若所得混合液为中性,且a+b=12,则Va:Vb=___________。
(2)25℃时,0.1mol/L的HaA溶液中c(H+)/c(OH-)=1010,请回答下列问题:
①HaA是___________(填“强电解质”或“弱电解质”)。
②在加水稀释HaA溶液的过程中,随着水量的增加而增大的是__________(填字母)
A.c(HaA) B.c(H+)/c(HaA) C.c(H+)与c(OH-)的乘积 D.c(OH-)
③NanA溶液显__________(填“酸性”、“中性”或“碱性”),理由是(用离子方程式表示)____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作或现象不能用勒夏特列原理解释的是
A. 配制FeCl3溶液
配制FeCl3溶液
B. 酯水解程度比较
酯水解程度比较
C. 探究石灰石与稀盐酸在密闭环境下的反应
探究石灰石与稀盐酸在密闭环境下的反应
D. 卤化银沉淀的转化
卤化银沉淀的转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】七水硫酸镁(MgSO4·7H2O)在印染、造纸和医药等工业上有重要的用途。硼镁泥是硼镁矿生产硼砂的废渣,其主要成分是MgCO3,还含有MgO、CaO、Fe2O3、FeO、MnO2、Al2O3、SiO2等杂质,工业上用硼镁泥制取七水硫酸镁的工艺流程如图:
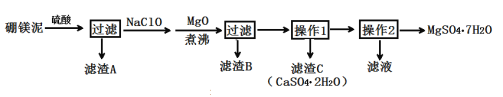
已知:①MnO2不溶于稀硫酸。
②CaSO4和MgSO4·7H2O在不同温度下的溶解度(g)数据如下表所示:
温度/℃ 物质 | 10 | 30 | 40 | 50 | 60 |
CaSO4 | 0.19 | 0.21 | 0.21 | 0.21 | 0.19 |
MgSO4·7H2O | 30.9 | 35.5 | 40.8 | 45.6 | —— |
(1)开始用到硫酸的质量分数为70%,密度为1.61g/cm3,则该硫酸溶液的物质的量浓度为___。
(2)滤渣A中除含少量CaSO4·2H2O外,还有___。
(3)加入MgO后,加热煮沸的目的是___。
(4)若滤渣B的主要成分为Al(OH)3和Fe(OH)3。则加入NaClO发生氧化还原反应的离子方程式为___。
(5)流程中操作1为蒸发浓缩、趁热过滤,这样即可得到CaSO4·2H2O,又防止___。
(6)获取MgSO4·7H2O的操作2为:___、___、过滤洗涤。
(7)已知开始硼镁泥样品的质量为ag,制取七水硫酸镁的质量为bg,据此能计算出硼镁泥中镁元素的含量吗?若能,请写出表达式;若不能,请说明理由。___(能或不能),表达式(或理由)为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香草醛是一种食品添加剂,可由愈创木酚作原料合成,合成路线如图所示。下列说法正确的是( )
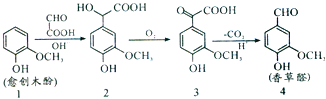
A.反应1→2中发生了取代反应
B.化合物2在一定条件下可发生缩聚反应
C.检验制得的香草醛中是否混有化合物3可用银氨溶液
D.等物质的量的四种化合物分别与足量H2反应,消耗H2物质的量之比为3:4:5:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用下列装置进行乙醇催化氧化的实验。
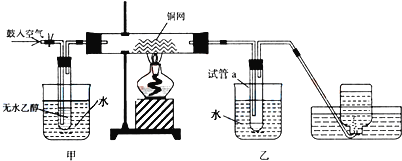
(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学反应方程式:___,__。
(2)在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇的氧化应是__反应。
(3)甲和乙两个水浴作用不相同。甲的作用是__;乙的作用是__。
(4)反应进行一段时间后,试管a中能收集到不同的物质,它们是__。集气瓶中收集到的气体的主要成分是___。(写名称)
(5)若试管a中收集到的液用紫色石蕊试纸检验,试纸显红色,说明液体中还含有__。除去该物质,可先在混合液中加入___(填写字母)。
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
然后,再通过___(填实验操作名称)即可除去。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为短周期元素,它们在周期表中的位置如图所示。已知Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是( )
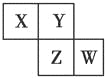
A. 原子半径:W>Z>Y>X
B. 最高价氧化物对应水化物的酸性:Z>W>X
C. 氢化物的稳定性:X>Y>Z
D. 四种元素的单质中,Z单质的熔、沸点最高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中反应①是制备SiH4的一种方法,其副产物MgCl2·6NH3是优质的镁资源。下列说法错误的是
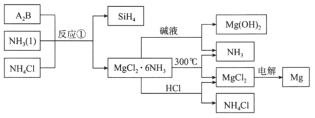
A.A2B的化学式为Mg2Si
B.该流程中可以循环使用的物质是NH3和NH4Cl
C.利用MgCl2·6NH3制取镁的过程中发生了化合反应、分解反应
D.分别将MgCl2溶液和Mg(OH)2悬浊液加热、灼烧,最终得到的固体相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国际能源期刊报道了一种正在开发中的绿色环保“全氢电池”,有望减少废旧电池产生污染。其工作原理如图所示。下列说法正确的是
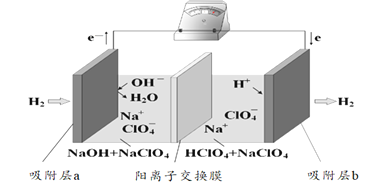
A.“全氢电池”工作时,将酸碱反应的中和能转化为电能
B.吸附层b发生的电极反应:H2 – 2e- + 2 OH-= 2H2O
C.Na+ 在装置中从右侧透过阳离子交换膜向左侧移动
D.“全氢电池”的总反应: 2H2 + O2 =2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com