
【题目】根据实验要求,从下列物质的分离或提纯方法中,选择恰当的实验方法将其序号填在空格处。
A.萃取分液 B.过滤 C.加热分解 D.蒸馏
(1)除去![]() 固体中少量的
固体中少量的![]() :_____________________。
:_____________________。
(2)分离食盐水与沙子的混合物:___________________。
(3)从碘水中提取碘:________________________。
(4)分离四氯化碳(沸点![]() )和甲苯(沸点
)和甲苯(沸点![]() )的混合物:___________________。
)的混合物:___________________。
科目:高中化学 来源: 题型:
【题目】如图是甲醇燃料电池的结构示意图。甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为2CH3OH +3O2![]() 2CO2+ 4H2O。下列说法不正确的是
2CO2+ 4H2O。下列说法不正确的是
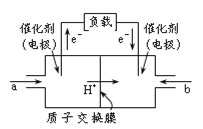
A.左电极为电池的负极,a处通入的物质是甲醇
B.正极反应式为:O2+ 2H2O + 4e-= 4OH-
C.负极反应式为:CH3OH + H2O-6e- = CO2+ 6H+
D.该电池提供1mole-,消耗氧气0.25mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白桦脂酸对白血病等恶性肿瘤细胞有抑制作用,其结构简式如图所示,在白桦脂酸中加入合适的试剂检验其官能团(必要时可加热),下列试剂、现象、结论都正确的一项是

选项 | 试剂 | 现象 | 结论 |
A | 氯化铁溶液 | 溶液变色 | 含有羟基 |
B | 银氨溶液 | 有银镜产生 | 含有醛基 |
C | 碳酸氢钠溶液 | 有气泡产生 | 含有羧基 |
D | 酸性KMnO4溶液 | 溶液褪色 | 含有碳碳双键 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用化合价推测物质的性质是化学研究的重要手段。
(1)![]() 的性质___________(填字母序号,下同)。
的性质___________(填字母序号,下同)。
A.只有氧化性 B.只有还原性 C.既有氧化性又有还原性
(2)将![]() 通入酸性
通入酸性![]() 溶液中,溶液由紫色变成无色(
溶液中,溶液由紫色变成无色(![]() 元素以
元素以![]() 形式存在)。反应结束后,硫元素的存在形式合理的是_______________。
形式存在)。反应结束后,硫元素的存在形式合理的是_______________。
A.![]() B.
B.![]() C.
C.![]() D.
D. ![]()
(3)将![]() 通入氯水中,因发生氧化还原反应生成
通入氯水中,因发生氧化还原反应生成![]() ,写出该反应的化学方程式____________。
,写出该反应的化学方程式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物A(C11H8O4)在氢氧化钠溶液中加热反应后再酸化可得到化合物B和C.回答下列问题:
(1)B的分子式为C2H4O2,分子中只有一个官能团.则B的结构简式是 ,B与乙醇在浓硫酸催化下加热反应生成D,该反应的化学方程式是 ,该反应的类型是 ;写出两种能发生银镜反应的B的同分异构体的结构简式 .
(2)C是芳香化合物,相对分子质量为180,其碳的质量分数为60.0%,氢的质量分数为4.4%,其余为氧,则C的分子式是 .
(3)已知C的芳环上有三个取代基,其中一个取代基无支链,且还有能使溴的四氯化碳溶液褪色的官能团及能与碳酸氢钠溶液反应放出气体的官能团,则该取代基上的官能团名称是 .另外两个取代基相同,分别位于该取代基的邻位和对位,则C的结构简式是 .
(4)A的结构简式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2H2O(l)=2H2(g)+O2(g) ΔH=+571.0kJ/mol。以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制H2的过程如下:
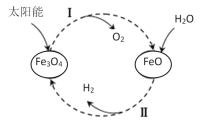
过程Ⅰ:2Fe3O4(s)=6FeO(s)+O2(g) ΔH=+313.2kJ/mol
过程Ⅱ:……
下列说法不正确的是( )
A.过程Ⅰ中每消耗232gFe3O4转移2mol电子
B.过程Ⅱ热化学方程式为:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH=-128.9kJ/mol
C.过程Ⅰ、Ⅱ中能量转化的形式依次是:太阳能→化学能→热能
D.铁氧化合物循环制H2具有成本低、产物易分离等优点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】东晋《华阳国志南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)文明中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的价电子排布式为_________,3d能级上的未成对的电子数为______。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中SO42-的立体构型是_____。
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为______ ,提供空轨道的中心微粒是_____。
③氨的沸点_____(“高于”或“低于”)膦(PH3),原因是______;氨是_____分子(填“极性”或“非极性”),中心原子的轨道杂化类型为_______。
(3)单质铜及镍都是由______键形成的晶体:元素铜与镍的第二电离能分别为:ICu=1958kJ/mol,INi=1753kJ/mol,ICu>INi的原因是______。
(4)某镍白铜合金的立方晶胞结构如图所示。
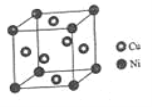
①晶胞中镍原子与铜原子的数量比为_____。
②若合金的密度为dg/cm3,晶胞参数a=________nm
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中可以获得淡水、食盐,并可提取镁和溴等物质。
(1)海水淡化的方法有_______(填一种)。
(2)写出元素钠在元素周期表中的位置:_______。
(3)从海水中提取镁的流程如下图所示:
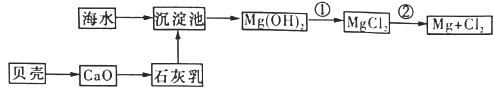
反应①的离子方程式为_______________。
反应②的化学方程式为_______________。
(4)从海水中提取溴的主要步骤是向浓缩的海水中通人氯气,将溴离子氧化,该反应的离子方程式为_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com