
【题目】用NA表示阿伏伽德罗常数的值.下列判断正确的是( )
A.32克O2和O3组成的混合气体中含有的氧原子数目为2NA
B.常温常压下,22.4 L乙醇含有的分子数目为NA
C.1 mol Na变为Na+时得到的电子数目为NA
D.44克14C16O2含氧原子数为2NA
科目:高中化学 来源: 题型:
【题目】阿塞那平用于治疗精神分裂症,可通过以下方法合成(部分反应条件略去);

(1)阿塞那平中的含氧官能团为_______(填官能团的名称)。由F→阿塞那平的反应类型为______________。
(2)化合物X的分子式为C4H9NO2,则由B→C反应的另一产物的化学式_______________________。
(3)由D生成E的过程中先后发生加成反应和消去反应,则加成反应后中间体的结构简式为____________。
(4)写出同时满足下列条件的B的一种同分异构体的结构简式:________。
I.属于芳香化合物,分子中含有5种不同化学环境的氢;
II.能发生银镜反应和水解反应,水解产物能与FeCl3溶液发生显色反应。
(5)已知: ![]() ,卤代烃碱性条件下不与醇反应。请写出以CH3Cl、CH3NH2和
,卤代烃碱性条件下不与醇反应。请写出以CH3Cl、CH3NH2和![]() 为原料制备
为原料制备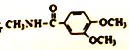 的合成路线流程图(无机试剂任用)。_____________
的合成路线流程图(无机试剂任用)。_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、氮和氯元素及其化合物与人类的生产、生活密切相关。
I.碳的化合物的转换在生产、生活中具有重要的应用。特别是CO2的低碳转型对抵御气候变化具有重要意义。

在三个容积均为1L的密闭容器中以不同的氢碳比n(H2)/n(CO2)充入H2和CO2,在一定条件下发生反应:
2CO2(g) + 6H2(g) ![]() C2H4(g) + 4H2O(g) △H,CO2的平衡转化率与温度的关系如图所示(①、②、2.0分别代表三种氢碳比时的变化曲线)。
C2H4(g) + 4H2O(g) △H,CO2的平衡转化率与温度的关系如图所示(①、②、2.0分别代表三种氢碳比时的变化曲线)。
请回答下列问题:
(1)反应的△H_____0,氢碳比①________②,Q点v(正)_____v(逆)(填“大于”或“小于”)
(2)若起始时,CO2的浓度为0.5mol/L,氢气的浓度为1.0mol/L;则P点对应温度的平衡常数的值为_____________________。
II.氯的化合物合成、转化一直是科学研究的热点。
①一定条件下,氯气与氨气反应可以制备氯胺[NH2Cl(g)],已知部分化学键的键能:
则上述反应的热化学方程式为_______________________________________________________。
化学键 | N—H | Cl—Cl | N—Cl | H—Cl |
键能/kJ·mol-1 | 391.3 | 243.0 | 191.2 | 431.8 |
②氯胺是一种长效缓释含氯消毒剂,有缓慢而持久的杀菌作用,可以杀死H7N9禽流感病毒,其消毒原理为与水缓慢反应生成强氧化性的物质,该反应的化学方程式为
_________________________________________________________。
III.用氨水除去SO2
(1)已知25℃时,NH3·H2O的Kb=1.8×10-5,H2SO3的Ka1=1.3×10-2,Ka2=6.2×10-8.若氨水的浓度为2.0mol/L,则溶液中的c(OH-)=_________mol/L.将SO2通入该氨水中,当c(OH-)降至1.0×10-7mol/L时,溶液中的c(SO32-)/c(HSO3-)=_____________.
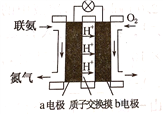
(2)利用氨气与空气催化氧化法制取联氨N2H4.如图是由“联氨-空气”形成的绿色燃料电池,以石墨为电极的电池工作原理示意图,b电极为____________极(填“正”或“负”),写出该电池工作时a电极的电极反应式___________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大,其中Y、W处于同一主族,Y、Z的原子最外层电子数之和等于9,X 的简单氢化物与W的单质组成的混合气体见光可生成W的氢化物和油状混合物。下列说法正确的是
A. 简单离子半径:Y>W>Z
B. W 的氧化物对应的水化物的酸性一定比X 的强
C. Y的简单气态氢化物的热稳定性一定比W的强
D. Y 分别与X、Z形成的化合物,其所含化学键的类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有反应:CO(g)+H2O(g)CO2(g)+H2(g)△H<0,在850℃时,平衡常数K=1.现在850℃时,向2L的密闭容器中充入CO、H2O(g)各4mol,试回答下列问题(写出具体的计算过程):
(1)达平衡时,CO转化率为多少?
(2)H2的体积分数为多少?
(3)若温度仍为850℃,初始时CO浓度为2mol/L,H2O(g)为6mol/L,则平衡时CO转化率为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中药狼巴草的成分之一M具有清炎杀菌作用,M的结构简式如图所示: 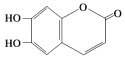 ,下列叙述正确的是( )
,下列叙述正确的是( )
A.M的分子式为C9H6O4
B.1 mol M最多能与2 mol Br2发生反应
C.1 molM最多能与4 mol氢氧化钠反应
D.M既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】防治禽流感病毐目前人类面临的-个重大课题。八角茴香属于草本植物,是我国民间常用做烹调的香料。医学研究成果显示,从八角茴香中可提取到莽草酸. 莽草酸有抗炎, 镇痛作用,也是合成对禽流感病爯毒有一定抑制作用的—种药物“达菲”的前体。莽草酸的结构式如下图所示,下列关于莽草酸的说法正确的是

A. 莽草酸的分子式为C7H4O5
B. 莽草酸的分子之间可能发生酯化反应
C. 莽草酸中含有苯环
D. 莽草酸不能使溴水褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某气态烃A能使溴的四氣化碳溶液褪色,其密度为相同条件下H2密度的14倍,完全燃烧产生等物质的里的CO2和H2O, A有如下转化关系,回答下列问题:
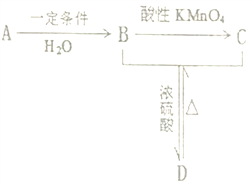
(1)A 的结构简式_______;B中含有的官能团名称______。
(2)A→B的反应类型为_______; C中含有的化学键类型_______。
(3)写出B+C→D的化学方程式_______;
(4)比A多一个碳的A的同系物与HCl气体反应得到的产物的同分异构体有_________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组用凯氏定氮法(Kjeldahl method)来测定农产品中氮的含量,测定过程如下:
I.用热浓硫酸处理0.25g谷物样品,把有机氮转化为铵盐。
II.用下图所示装置处理上述铵盐(夹持装置略去)。
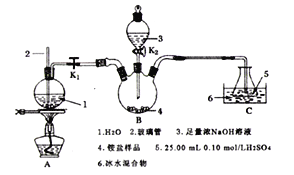
回答下列问题:
(1)实验前要检验B装置的气密性,具体操作为______________________________。
(2)盛放氢氧化钠溶液的仪器名称为__________________;玻璃管2的作用是___________________;圆底烧瓶中碎瓷片的作用是_________________________________________。
(3)将“谷物处理后所得的铵盐”加入三颈瓶中,打开玻璃塞、旋开K2,加入足量氢氧化钠溶液,关闭K2,打开K1,点燃酒精灯使水蒸气进入B装置。
①B装置中反应的离子方程式为_______________________________。
②C装置冰水混合物的作用是__________________________________。
III.滴定、计算氮的含量
(4)取下锥形瓶,加入指示剂,用0.10mol/L的NaOH溶液滴定,重复滴定3次,平均消耗19.30mLNaOH溶液。
①该滴定的指示剂应选择____________________。
a.甲基橙 b.配酞 c.甲基橙或酚酞
②该谷物样品中氮的百分含量为_____________。(保留2位小数)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com