
【题目】1,2-二氯丙烷(CH2ClCHClCH3)是一种重要的化工原料,工业上可用丙烯加成法制备,主要副产物为3-氯丙烯(CH2=CHCH2Cl),反应原理为:
I.CH2=CHCH3(g)+Cl2(g) ![]() CH2ClCHClCH3(g) H1=-134kJ·mol-1
CH2ClCHClCH3(g) H1=-134kJ·mol-1
II.CH2=CHCH3(g)+Cl2(g) CH2=CHCH2Cl(g)+HCl(g) H2=-102kJ·mol-1
请回答下列问题:
(1)已知CH2=CHCH2Cl(g)+HCl(g) ![]() CH2ClCHClCH3(g)的活化能Ea(正)为132kJ·mol-1,则该反应的活化能Ea(逆)为___________kJ·mol-1。
CH2ClCHClCH3(g)的活化能Ea(正)为132kJ·mol-1,则该反应的活化能Ea(逆)为___________kJ·mol-1。
(2)一定温度下,密闭容器中发生反应I和反应II,达到平衡后增大压强,CH2ClCHClCH3的产率____________(填“增大”“减小”或“不变”),理由是_________________________________。
(3)起始时向某恒容绝热容器中充入1 mol CH2=CHCH3和1 mol Cl2发生反应II,达到平衡时,容器内气体压强_________________(填“增大”“减小”或“不变”)。
(4)某研究小组向密闭容器中充入一定量的CH2=CHCH3和Cl2,分别在A、B两种不同催化剂作用下发生反应,一段时间后测得CH2ClCHClCH3的产率与温度的关系如图所示。p点是否为对应温度下CH2ClCHClCH3的平衡产率,_________填“是”或“否”)判断理由是_______________________。

(5)一定温度下,向恒容密闭容器中充入等物质的量的CH2=CHCH3(g)和Cl2(g)。在催化剂作用下发生反应I,容器内气体的压强随时间的变化如下表所示。
时间/min | 0 | 60 | 120 | 180 | 240 | 300 | 360 |
压强/kPa | 80 | 74.2 | 69.4 | 65.2 | 61.6 | 57.6 | 57.6 |
①用单位时间内气体分压的变化来表示反应速率,即![]()
②该温度下,若平衡时HCl的体积分数为![]() ,则丙烯的平衡总转化率
,则丙烯的平衡总转化率![]() ____________;反应I的平衡常数Kp=____________________kPa-1(Kp为以分压表示的平衡常数,保留小数点后2位)。
____________;反应I的平衡常数Kp=____________________kPa-1(Kp为以分压表示的平衡常数,保留小数点后2位)。
【答案】164 增大 反应I是一个气体物质的量减小的反应,达到平衡后增大压强,反应I正向移动,CH2ClCHClCH3的产率增大 增大 否 因为生成CH2ClCHClCH3的反应为放热反应,温度越低平衡转化率越高,而450℃的产率高于p点产率,所以p点不是对应温度下CH2ClCHClCH3的平衡产率 0.09 74% 0.21
【解析】
(1)用反应I-反应II得到CH2=CHCH2Cl(g)+HCl(g) ![]() CH2ClCHClCH3(g) △H=-32kJ·mol-1,△H= Ea(正) —Ea(逆)= 132kJ·mol-1-Ea(逆)= -32kJ·mol-1,Ea(逆)= 164kJ·mol-1。答案为:164;
CH2ClCHClCH3(g) △H=-32kJ·mol-1,△H= Ea(正) —Ea(逆)= 132kJ·mol-1-Ea(逆)= -32kJ·mol-1,Ea(逆)= 164kJ·mol-1。答案为:164;
(2)反应I是一个气体物质的量减小的反应,反应II气体物质的量不变,达到平衡后增大压强,反应I正向移动,CH2ClCHClCH3的产率增大。答案为:增大;反应I是一个气体物质的量减小的反应,达到平衡后增大压强,反应I正向移动,CH2ClCHClCH3的产率增大;
(3)反应II为放热反应,由于体系为绝热容器,随着反应进行,体系的温度升高,容器内气体压强增大。答案为:增大;
(4)p点不是对应温度下CH2ClCHClCH3的平衡产率,因为生成CH2ClCHClCH3的反应为放热反应,温度越低平衡转化率越高,而450℃的产率高于p点产率,所以p点不是对应温度下CH2ClCHClCH3的平衡产率。答案为:否;因为生成CH2ClCHClCH3的反应为放热反应,温度越低平衡转化率越高,而450℃的产率高于p点产率,所以p点不是对应温度下CH2ClCHClCH3的平衡产率;
(5)①压强的减小由反应I引起CH2=CHCH3(g)+Cl2(g) ![]() CH2ClCHClCH3(g)反应120min的压强的变化为10.6kPa,故v(CH2ClCHClCH3)=
CH2ClCHClCH3(g)反应120min的压强的变化为10.6kPa,故v(CH2ClCHClCH3)=![]() =0.09 kPa·min-1;
=0.09 kPa·min-1;
②设起始CH2=CHCH3(g)和Cl2(g)的物质的量各为1mol,平衡时气体的总物质的量为![]() =1.44 mol,生成的n(CH2ClCHClCH3)=0.56 mol,反应I消耗的CH2=CHCH3(g)和Cl2(g)的物质的量各为0.56 mol,根据平衡时HCl的体积分数为
=1.44 mol,生成的n(CH2ClCHClCH3)=0.56 mol,反应I消耗的CH2=CHCH3(g)和Cl2(g)的物质的量各为0.56 mol,根据平衡时HCl的体积分数为![]() ,计算反应Ⅱ生成的n(HCl)= n(CH2=CHCH2Cl)=0.18mol,参与反应的CH2=CHCH3(g)和Cl2(g)的物质的量各为0.18 mol ,则丙烯的平衡总转化率
,计算反应Ⅱ生成的n(HCl)= n(CH2=CHCH2Cl)=0.18mol,参与反应的CH2=CHCH3(g)和Cl2(g)的物质的量各为0.18 mol ,则丙烯的平衡总转化率![]()
![]() =74%;平衡时,反应CH2=CHCH3(g)+Cl2(g)
=74%;平衡时,反应CH2=CHCH3(g)+Cl2(g) ![]() CH2ClCHClCH3(g)中,n(
CH2ClCHClCH3(g)中,n(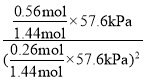 =0.21。答案为:0.09;74%;0.21。
=0.21。答案为:0.09;74%;0.21。


 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:高中化学 来源: 题型:
【题目】二氧化锰不仅是活性好的催化剂,也被广泛用作干电池的正极材料。某化学小组设计用高硫锰矿(主要成分为锰的化合物和硫化亚铁)为原料制取二氧化锰的工艺流程如图:
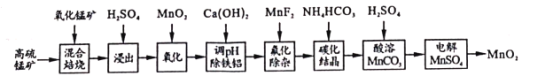
已知:①“混合焙烧”后的烧渣含MnSO4、Fe2O3及少量FeO、MgO、Al2O3
②在该条件下,金属离子开始沉淀和完全沉淀的pH如表:
金属离子 | Fe3+ | Fe2+ | Al3+ | Mn2+ |
开始沉淀 | 1.8 | 6.8 | 4.0 | 7.5 |
完全沉淀 | 3.2 | 8.0 | 5.0 | 8.4 |
(1)写出浸出时与铝元素有关的离子反应方程式____。
(2)上述“氧化”步骤是否可省略____(填“是”或“否”),你的依据是 _____。
(3)“调pH除铁铝’’时,生成沉淀的pH范围为____;“氟化除杂”中除去的离子为____。
(4)请用平衡移动原理解释除杂处理后的Mn2+用NH4HCO3转化成MnCO3沉淀的过程___(用文字和离子方程式表达)。
(5)用惰性电极电解MnSO4制备MnO2时,其阳极反应式为____;整个流程中能够循环利用的物质除MnO2外还有___(写名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
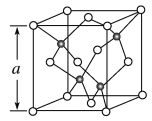
【题目】(1)Cu的一种氯化物晶胞结构如图所示(黑球表示铜原子,白球表示氯原子),该氯化物的化学式是__。若该晶体的密度为ρg·cm-3,以NA表示阿伏加德罗常数的值,则该晶胞的边长a=__nm。
(2)一种四方结构的超导化合物的晶胞如图1所示,晶胞中Sm和As原子的投影位置如图2所示。
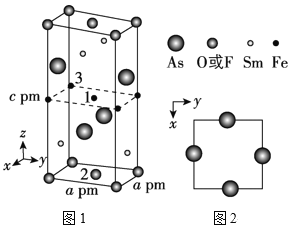
图中F-和O2-共同占据晶胞的上下底面位置,若两者的比例依次用x和1x代表,则该化合物的化学式表示为__,通过测定密度ρ和晶胞参数,可以计算该物质的x值,完成它们关系表达式:ρ=__g·cm-3。
以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图1中原子1的坐标为(![]() ,
,![]() ,
,![]() ),则原子2和3的坐标分别为__、__。
),则原子2和3的坐标分别为__、__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某容器中发生一个化学反应,反应过程中存在H2O、ClO-、CN-、HCO3-、N2、Cl-六种离子。在反应过程中测得ClO-和N2的物质的量随时间变化的曲线如图所示。下列有关判断中不正确的是

A.还原剂是含CN-的物质,氧化产物不只有N2
B.氧化剂是ClO-,还原产物是HCO3-
C.参与反应的氧化剂与还原剂的物质的量之比为2:5
D.标准状况下若生成2.24LN2则转移电子为1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙胺卡因(H)是一种局部麻醉药物,实验室制备H的一种合成路线如下:
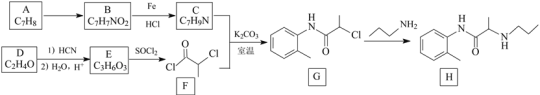
已知:![]()
![]()
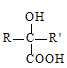 (R和R'为烃基或H)
(R和R'为烃基或H)
回答下列问题:
(1)B的化学名称是___________,H的分子式是____________。
(2)C中所含官能团的名称为_______________,由G生成H的反应类型是___________。
(3)C与F反应生成G的化学方程式为___________。反应中使用K2CO3的作用是_______。
(4)化合物X是E的同分异构体,X能与NaOH溶液反应,其核磁共振氢谱只有1组峰。X的结构简式为________。
(5)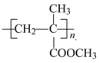 (聚甲基丙烯酸甲酯)是有机玻璃的主要成分,写出以丙酮(CH3COCH3)和甲醇为原料制备聚甲基丙烯酸甲酯单体的合成路线___________。(无机试剂任选)
(聚甲基丙烯酸甲酯)是有机玻璃的主要成分,写出以丙酮(CH3COCH3)和甲醇为原料制备聚甲基丙烯酸甲酯单体的合成路线___________。(无机试剂任选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对伞花烃(a)常用作染料、医药、香料的中间体,a可转化为b(如图)。下列说法错误的是( )

A.常温下对伞花烃呈液态且难溶于水
B.b物质的一氯代物有5种
C.对伞花烃分子中最多有9个碳原子共平面
D.图中氢化反应既是加成反应也是还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:将![]() 溶液用
溶液用![]() 盐酸滴定时,若用酚酞做指示剂,终点时消耗盐酸
盐酸滴定时,若用酚酞做指示剂,终点时消耗盐酸![]() ;若用甲基橙做指示剂,终点时消耗盐酸
;若用甲基橙做指示剂,终点时消耗盐酸![]() 。现有一份白色粉末,可能含有
。现有一份白色粉末,可能含有![]() 、
、![]() 、
、![]() 的一种或两种。现取一定量的该粉未配成适当浓度的稀溶液并分成两等份,分别用
的一种或两种。现取一定量的该粉未配成适当浓度的稀溶液并分成两等份,分别用![]() 盐酸滴定。一份用酚酞做指示剂,消耗盐酸
盐酸滴定。一份用酚酞做指示剂,消耗盐酸![]() ;另一份用甲基橙做指示剂,消耗盐酸
;另一份用甲基橙做指示剂,消耗盐酸![]() 。下列说法正确的是( )
。下列说法正确的是( )
①若![]() ,则固体中只含有
,则固体中只含有![]()
②若![]() ,则固体中只含
,则固体中只含![]()
③若![]() ,则固体中含有
,则固体中含有![]() 、
、![]()
④若![]() ,则固体中含有
,则固体中含有![]() 、
、![]()
A.①②③④B.③④C.①②D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列反应可用于检测司机是否酒后驾驶:![]()
![]() 。
。
①配合物![]() 中,与
中,与![]() 形成配位键的原子是__________(填元素符号)。
形成配位键的原子是__________(填元素符号)。
②![]() 中
中![]() 原子的杂化轨道类型是________;
原子的杂化轨道类型是________;![]()
![]() 含有
含有![]() 键的数目为_______。
键的数目为_______。
(2)![]() 分子中,
分子中,![]() 原子的杂化轨道类型是__________;写出由3个原子组成且与
原子的杂化轨道类型是__________;写出由3个原子组成且与![]() 具有相同空间构型的离子:___________(填一个即可)。
具有相同空间构型的离子:___________(填一个即可)。
(3)石墨烯(结构如图1所示)是一种由单层碳原子构成的具有平面结构的新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯(结构如图2所示)。

氧化石墨烯中2号![]() 原子的杂化方式是_________,该
原子的杂化方式是_________,该![]() 原子与相邻
原子与相邻![]() 原子形成的键角______(填“>”“<”或“=”)石墨烯中1号
原子形成的键角______(填“>”“<”或“=”)石墨烯中1号![]() 与相邻
与相邻![]() 形成的键角。
形成的键角。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧化锂是制取锂和锂的化合物的原料,用电解法制备氢氧化锂的工作原理如图所示:
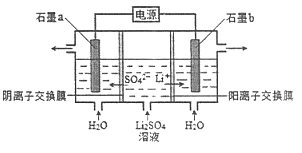
下列叙述不正确的是
A.b极附近溶液的pH增大
B.a极发生的反应为2H2O-4e-=O2↑+4H+
C.该法制备LiOH还可得到硫酸和氢气等产品
D.b极是电解池的阳极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com