
ЁОЬтФПЁПгЁЫЂЕчТЗАхЪЧгЩгаЛњИДКЯВФСЯКЭЭВИДКЯЙЙГЩЃЌПЬжЦгЁЫЂЕчТЗЪБЃЌвЊгУFeCl3ШмвКзїЮЊЁАИЏЪДвКЁБЃЌбаОПЦфжЦБИМАаджЪЪЧвЛИіживЊЕФПЮЬтЁЃ
(1)ТШЛЏЬњОЇЬхЕФжЦБИ(МаГжМАМгШШзАжУЪЁТд)
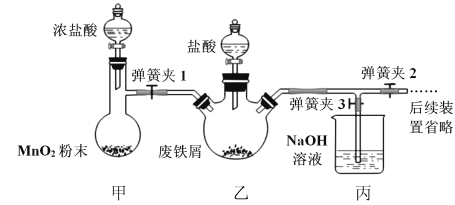
ЂйЪЕбщЙ§ГЬжазАжУМзжаЗЂЩњЗДгІЕФРызгЗНГЬЪН_________________________________ЁЃ
ЂкЮЊЫГРћДяГЩЪЕбщФПЕФЃЌЩЯЪізАжУжаМзжаЛюШћЁЂввжаЛюШћЁЂЕЏЛЩМа1ЁЂ2ЁЂ3ДђПЊКЭЙиБеЕФЫГађЮЊ__________ЁЃ
ЂлЗДгІНсЪјКѓЃЌНЋввжаШмвКБпМгШы___________ЃЌБпНјааМгШШХЈЫѕЁЂ___________ЁЂЙ§ТЫЁЂЯДЕгЁЂИЩдяМДЕУЕНВњЦЗЁЃ
(2)ТШЛЏЬњЕФаджЪЬНОПЃК
вбжЊЃКЂйТШЛЏЬњЕФШлЕуЮЊ306ЁцЁЂЗаЕуЮЊ315ЁцЃЌвзЩ§ЛЊЃЌЦјЬЌFeCl3ЛсЗжНтГЩFeCl2КЭCl2ЂкFeCl2ШлЕу670Ёц)

ВйзїВНжш | ЪЕбщЯжЯѓ | НтЪЭдвђ |
ДђПЊKЃЌГфШыЕЊЦј | DжагаЦјХнВњЩњ | ЂйГфШыN2ЕФдвђ___________ |
ЙиБеKЃЌМгШШжС600ЁцЃЌГфЗжзЦЩеЙЬЬх | BжаГіЯжзиЛЦЩЋЙЬЬх | ЂкВњЩњЯжЯѓЕФдвђ___________ЁЃ |
ЪЕбщНсЪјЃЌеёЕДCОВжУ | Ђл___________ | Ђм___________(гУЗНГЬЪННтЪЭ) |
ЁОД№АИЁП4HClЃЈХЈЃЉ+MnO2![]() Cl2Ёќ+MnCl2+2H2O ДђПЊЕЏЛЩМа2ЁЂДђПЊввжаЛюШћЁЂЙиБеввжаЛюШћЁЂЙиБеЕЏЛЩМа2ЁЂДђПЊЕЏЛЩМа3ЁЂДђПЊМзжаЛюШћЁЃ ХЈбЮЫс РфШДНсОЇ ХХОЛзАжУФкЕФПеЦјЁЃ Щ§ЛЊFeCl3РфФ§ГЩЙЬЬЌЁЃ ШмвКЗжВуЃЌЯТВуЮЊГШКьЩЋЁЃ Cl2+2BrЁЊ == Br2+2ClЁЊ
Cl2Ёќ+MnCl2+2H2O ДђПЊЕЏЛЩМа2ЁЂДђПЊввжаЛюШћЁЂЙиБеввжаЛюШћЁЂЙиБеЕЏЛЩМа2ЁЂДђПЊЕЏЛЩМа3ЁЂДђПЊМзжаЛюШћЁЃ ХЈбЮЫс РфШДНсОЇ ХХОЛзАжУФкЕФПеЦјЁЃ Щ§ЛЊFeCl3РфФ§ГЩЙЬЬЌЁЃ ШмвКЗжВуЃЌЯТВуЮЊГШКьЩЋЁЃ Cl2+2BrЁЊ == Br2+2ClЁЊ
ЁОНтЮіЁП
(1) ЂйЪЕбщЪвжЦШЁТШЦјЕФЗДгІЃЌЗНГЬЪНД№АИЮЊ4HClЃЈХЈЃЉ+MnO2=Ёї= Cl2Ёќ+MnCl2+2H2OЃЛ
ЂкЪЕбщЙ§ГЬЃЌЯШжЦШЁFeCl2ЃЌдйгУТШЦјбѕЛЏFeCl2ЕУЕНFeCl3ЃЌвЊзЂвтЯШКѓЃЌЯШДђПЊЮќЪезАжУЃЌдйДђПЊЗЂЩњзАжУЃЌЙиБеЕФЪБКђЯШЙиБеЗЂЩњзАжУЃЌдйЙиБеЮќЪезАжУЁЃЫљвдЪЕбщжаЯШжЦШЁFeCl2ЃЌДђПЊЕЏЛЩМа2ЁЂДђПЊввжаЛюШћЃЛдйЙиБеввжаЛюШћЁЂЙиБеЕЏЛЩМа2ЃЛдйжЦШЁТШЦјЃЌТШЦјЮЊгаЖОЦјЬхгУNaOHЮќЪеЃЌЫљвдДђПЊЕЏЛЩМа3ЁЂДђПЊМзжаЛюШћЃЌ Д№АИЮЊДђПЊЕЏЛЩМа2ЁЂДђПЊввжаЛюШћЁЂЙиБеввжаЛюШћЁЂЙиБеЕЏЛЩМа2ЁЂДђПЊЕЏЛЩМа3ЁЂДђПЊМзжаЛюШћЃЛ
ЂлFeCl3дкжЦШЁОЇЬхЕФЙ§ГЬжаЃЌгЩгкFe3+взЗЂЩњЫЎНтЃЌзюжеЛсЕУЕНFe2O3ЃЌвђДЫвЊвжжЦЫЎНтЃЌвЊВЛЖЯМгШыХЈбЮЫсЃЌеєЗЂНсОЇЕФЙ§ГЬжаМгШШХЈЫѕКѓУцЮЊРфШДНсОЇЁЃД№АИЮЊХЈбЮЫсЁЂРфШДНсОЇЃЛ
(2) ЂйЗДгІЧАЭЈШывЛАуЪЧЮЊСЫХХГ§зАжУжаПеЦјЃЌИУЗДгІжаЛсЩњГЩFeCl2ЃЌвзБЛбѕЦјбѕЛЏЃЌД№АИЮЊХХОЛзАжУФкЕФПеЦјЃЛ
ЂкBжаГіЯжзиЛЦЩЋЙЬЬхЮЊFeCl3ЕФбеЩЋЃЌгЩгкFeCl3взЩ§ЛЊЃЌЕНBзАжУжаРфФ§ЯТРДГЪЯжзиЛЦЩЋЃЌД№АИЮЊЩ§ЛЊFeCl3РфФ§ГЩЙЬЬЌЃЛ
ЂлFeCl3ЗжНтБфГЩCl2КЭFeCl2ЃЌCl2ЛсКЭNaBrЗЂЩњЗДгІЃЌЕУЕНBr2ЃЌCCl4ЛснЭШЁфхЕЅжЪЃЌCCl4УмЖШБШЫЎДѓЃЌдкЯТВуЃЌГЪЯжГШКьЩЋЁЃД№АИЮЊШмвКЗжВуЃЌЯТВуЮЊГШКьЩЋЃЛ
ЂмCl2ЛсКЭNaBrЗЂЩњЗДгІЃЌЕУЕНBr2ЕФЗДгІЃЌД№АИЮЊCl2+2BrЁЊ= Br2+2ClЁЊЁЃ


 ЧЇРяТэзпЯђМйЦкЦкФЉЗТецЪдОэКЎМйЯЕСаД№АИ
ЧЇРяТэзпЯђМйЦкЦкФЉЗТецЪдОэКЎМйЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПДгдЊЫиЛЏКЯМлЩ§НЕЕФНЧЖШЗжЮіЃЌЯТСаВЛЪєгкбѕЛЏЛЙдЗДгІЕФЪЧ
A. H2+Cl2![]() 2HCl B. 2HClO
2HCl B. 2HClO![]() 2HCl+O2
2HCl+O2
C. 2NaI+Br2=2NaBr+I2 D. CaCl2+Na2CO3=CaCO3Ё§+2NaCl
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПРБНЗЫиѕЅЪЧРБНЗЕФЛюадГЩЗжЃЌгаНЕбЊбЙКЭЕЈЙЬДМЕФзїгУЁЃРБНЗЫиѕЅРрЛЏКЯЮяЕФНсЙЙПЩвдБэЪОЮЊ (RЮЊЬўЛљ)ЁЃЭМ27ЮЊвЛжжРБНЗЫиѕЅJЕФКЯГЩТЗЯпЃК
(RЮЊЬўЛљ)ЁЃЭМ27ЮЊвЛжжРБНЗЫиѕЅJЕФКЯГЩТЗЯпЃК

ЛиД№ЯТСаЮЪЬтЃК
(1)AЕФУћГЦЪЧ___________ЃЌGКЌгаЕФЙйФмЭХУћГЦЪЧ___________ЁЃ
(2)FКЭIЩњГЩJЕФЗДгІРраЭЪЧ___________ЁЃ
(3)EЕФНсЙЙМђЪНЮЊ____________________ЁЃ
(4)CЩњГЩDЕФЛЏбЇЗНГЬЪНЮЊ_________________________________ЃЛHЩњГЩIЕФЕкЂйВНЗДгІЕФЛЏбЇЗНГЬЪНЮЊ_________________________________ЁЃ
(5)GЕФЭЌЗжвьЙЙЬхжаЃЌБНЛЗЩЯЕФвЛТШДњЮяжЛгавЛжжЃЌЧвКЫДХЙВеёЧтЦзЯдЪО2зщЗхЕФЪЧ___________(аДНсЙЙМђЪН)ЁЃ
(6)ВЮееЩЯЪіТЗЯпЃЌЩшМЦвЛЬѕвдБНМзШЉКЭввДМЮЊдСЯ(ЮоЛњЪдМСШЮбЁ)КЯГЩШтЙ№Ыс
(![]() )ЕФКЯГЩТЗЯпЁЃ___________________
)ЕФКЯГЩТЗЯпЁЃ___________________
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЖўМзУбжЦБИСНжжЗНЗЈдРэШчЯТ
ЕквЛжжЗНЗЈЃКЕЄТѓTopspeЙЄвеЕФКЯГЩЦјвЛВНЗЈЃЌЪЧзЈУХеыЖдЬьШЛЦјдСЯПЊЗЂЕФвЛЯюаТММЪѕЁЃ
Ђй2CH4(g)+O2(g)![]() CH3OCH3(g)+H2O(g) ЁїH1
CH3OCH3(g)+H2O(g) ЁїH1
ЕкЖўжжЗНЗЈЃКЖўМзУбЩњВњЖўВНЗЈЃЌМДЯШКЯГЩМзДМЃЌМзДМдкДпЛЏМСЯТжЦЖўМзУбЁЃ
ЂкCO(g)+2H2(g)![]() CH3OH(g) ЁїH2
CH3OH(g) ЁїH2
Ђл2CH3OH(g)![]() CH3OCH3 (g)+H2O(g) ЁїH3
CH3OCH3 (g)+H2O(g) ЁїH3
(1)ШєгЩКЯГЩЦј(COЁЂH2)жБНгжЦБИ 1molCH3OCH3(g)ЃЌЧвЩњГЩH2O(1)ЃЌећИіЙ§ГЬжаЗХГіЕФШШСПЮЊ244kJЃЌдђЁїH2=___________kJЁЄmolЃ1ЁЃ(вбжЊЃКH2O(1)=H2O(g) ЁїH=+44.0 kJ/mol)
(2)ЯТСагаЙиЗДгІЂйа№ЪіВЛе§ШЗЕФЪЧ___________
a.ДяЕНЦНКтКѓЃЌЩ§ИпЮТЖШЃЌІЭе§МѕЩйЁЂІЭФцдіДѓЃЌЦНКтФцЯђвЦЖЏ
b.ЕБЫФжжЮяжЪЕФХЈЖШЯрЕШЃЌЗДгІДяЕНЛЏбЇЦНКтзДЬЌ
c.ШєИФБфЬѕМўЃЌЗДгІЮяЕФзЊЛЏТЪвЛЖЈдіДѓЃЌе§ЗДгІЫйТЪвЛЖЈДѓгкФцЗДгІЫйТЪ
d.ЕБДяЕНЦНКтЪБ2vе§(O2)=vФц(CH4)
e.ЯђИУКуШнЦНКтЬхЯЕжаГфШыыВЦјЃЌІЭе§ЁЂІЭФцОљдіДѓЃЌЦНКтЯђгввЦЖЏ
(3)гаШЫФЃФтжЦБИдРэЂђЃЌЛцжЦШчЭММзЭМЯёЃК
iЫЕУїCOЕФзЊЛЏТЪЫцЮТЖШЩ§ИпЯШдіДѓКѓМѕаЁЕФдвђЃК______________________ЁЃ
ii.ЗДгІЂкздЗЂНјааЕФЬѕМўЪЧ______________________ЁЃ
iii.Шєдк350ЁцЪБЕФ2LЕФУмБеШнЦїжаГфШы2 mol COКЭ6molH2ЃЌ8minДяЕНЦНКтЃЌc(CH3OCH3)=0.3molЁЄLЃ1ЃЌгУH2БэЪОЗДгІЂкЕФЫйТЪЪЧ___________ЃЛПЩФцЗДгІЂлЕФЦНКтГЃЪ§K3=___________ЁЃ
iv.Шє350ЁцЪБВтЕУШнЦїжаn(CH3OH)=n(CH3OCH3)ЃЌДЫЪБЗДгІЂлv(е§)___________ІЭ(Фц)ЃЌЫЕУїдвђ_________ЁЃ
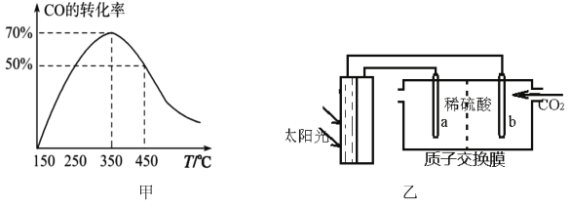
(4)ЙтФмДЂДцвЛАуЪЧжИНЋЙтФмзЊЛЛЮЊЕчФмЛђЛЏбЇФмНјааДЂДцЃЌРћгУЬЋбєЙтЁЂCO2ЁЂH2OЩњГЩЖўМзУбЕФЙтФмДЂДцзАжУШчЭМввЫљЪОдђbМЋЕФЕчМЋЗДгІЪНЮЊ___________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвдЯТЪЧЪЕбщЪвГЃгУЕФВПЗжвЧЦїЃЌЧыЛиД№ЯТСаЮЪЬтЃК
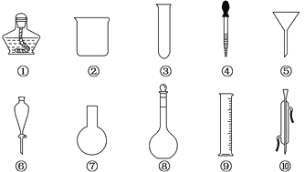
ЃЈ1ЃЉађКХЮЊЂрКЭЂтЕФвЧЦїЕФУћГЦЗжБ№ЮЊ______ЁЂ_______ЁЃ
ЃЈ2ЃЉдкЗжвКВйзїжаЃЌБиаыгУЕНЩЯЪівЧЦїжаЕФ__________ЃЈЬюађКХЃЉЁЃ
ЃЈ3ЃЉФмзїЗДгІШнЦїЧвПЩжБНгМгШШЕФвЧЦїЪЧЩЯЪіжаЕФ__________ЃЈЬюУћГЦЃЉЁЃ
ЃЈ4ЃЉХфжЦвЛЖЈЮяжЪЕФСПХЈЖШЕФШмвКЪБвЊгУЕНЕФвЧЦїЪЧ____________ЃЈЬюађКХЃЉЁЃ
ЃЈ5ЃЉШчЭМЪЧЮТЖШМЦЁЂСПЭВЁЂЕЮЖЈЙмЕФвЛВПЗжЃЌЯТЪіЖСЪ§ЃЈащЯпЖдгІПЬЖШЃЉМАЫЕЗЈе§ШЗЕФЪЧ_________ЁЃ

AЃЎЂйЪЧСПЭВЃЌЖСЪ§ЮЊ 2.5 mL BЃЎЂкЪЧСПЭВЃЌЖСЪ§ЮЊ 2.5 mL
CЃЎЂлЪЧЕЮЖЈЙмЃЌЖСЪ§ЮЊ 2.5 mL DЃЎЂкЪЧЮТЖШМЦЃЌЖСЪ§ЮЊ 2.5 Ёц
ЃЈ6ЃЉГ§ШЅбѕЛЏИЦжаЕФЬМЫсИЦПЩгУЪВУДЗНЗЈЃП______________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЙигкХЈСђЫсЕФЫЕЗЈВЛе§ШЗЕФЪЧ
A.ФмИЩдяТШЦј
B.ОпгаЧПИЏЪДад
C.ПЩгыН№ЪєЗДгІжЦШЁЧтЦј
D.МгШШЪБФмгыФОЬПЗЂЩњЗДгІ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПНќФъРДЃЌФђЫиЕчбѕЛЏЗЈДІРэИЛКЌФђЫиЕФЙЄвЕЗЯЫЎКЭЩњЛюЮлЫЎЕУЕНСЫЙуЗКЙизЂЃЌИУЗЈОпгаВйзїМђвзЁЂДІРэСПДѓЁЂдЫаажмЦкГЄЕШгХЕуЃЌЧвИУЙ§ГЬдкМюадЬѕМўЯТВњЩњЮоЖОЕФC02ЁЂN2.ЕчГиЙЄзїЪБЃЌЯТСаЫЕЗЈДэЮѓЕФЪЧЃЈ ЃЉ

A. ИКМЋЗЂЩњЕФЗДгІЮЊЃК![]()
B. е§МЋИННќШмвКЕФpHдіДѓ
C. ИєФЄжЛдЪаэбєРызгЭЈЙ§
D. ДІРэЕєЗЯЫЎжаФђЫи1.0gЪБЯћКФO2 0.56LЃЈБъзМзДПіЃЉ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПСђДњСђЫсФЦЪЧвЛжжживЊЕФЛЏЙЄВњЦЗЁЃФГаЫШЄаЁзщФтжЦБИСђДњСђЫсФЦОЇЬх(Na2S2O3ЁЄ5H2O)ЁЃВщдФзЪСЯжЊЃК
ЂйNa2S2O3ЁЄ5H2OЪЧЮоЩЋЭИУїОЇЬх,взШмгкЫЎ,ЦфЯЁШмвКгыBaCl2ШмвКЛьКЯЮоГСЕэЩњГЩЁЃ
ЂкЯђNa2CO3КЭNa2SЛьКЯШмвКжаЭЈШыSO2ПЩжЦЕУNa2S2O3ЁЃ
ЂлBaSO3ФбШмгкЫЎ,ПЩШмгкЯЁHClЁЃ
ЪЕбщзАжУШчЭМЫљЪО(ЪЁТдМаГжзАжУ)
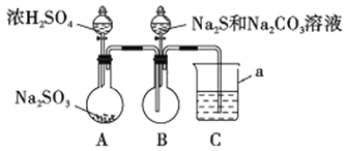
ЃЈ1ЃЉвЧЦїaЕФУћГЦЪЧ_________;CжаЕФЪдМСПЩвдЪЧ______ (бЁЬюЯТСазжФИБрКХ)ЁЃ
AЃЎЯЁH2SO4 BЃЎЫсадKMnO4ШмвК CЃЎБЅКЭNaHSO3ШмвК DЃЎNaOHШмвК
ЃЈ2ЃЉДЫЪЕбщзАжУЩшМЦгаШБЯн,ЦфИФНјЗНЗЈЪЧ_________________________ЁЃ
ЃЈ3ЃЉаДГіBжаЗДгІЕФРызгЗНГЬЪН_________________________________________ЁЃ
ЃЈ4ЃЉAЁЂBжаЗДгІЭъКѓ,дкВ№зАжУЧАЃЌгІНЋЦфжаЮлШОПеЦјЕФгаЖОЦјЬхГ§ШЅ,ВЩгУЕФЗНЗЈКЭОпЬхВйзїЪЧ________________________________________ЁЃ
ЃЈ5ЃЉИУЗЈЫљЕУВњЦЗжаГЃКЌгаЩйСПNa2SO3КЭNa2SO4ЁЃЮЊбщжЄВњЦЗжаКЌгаNa2SO3КЭNa2SO4,ИУаЁзщЩшМЦСЫвдЯТЪЕбщЗНАИ,ЧыНЋЗНАИВЙГфЭъећЁЃ(ЫљашЪдМСДгЯЁHNO3ЁЂЯЁH2SO4ЁЂЯЁHClЁЂеєСѓЫЎжабЁдё)
ШЁЪЪСПВњЦЗХфГЩЯЁШмвКЃЌМгзуСПBaCl2ШмвК,гаАзЩЋГСЕэЩњГЩЃЌ_______________ЃЌШєГСЕэЮДЭъШЋШмНт,ВЂгаДЬМЄадЦјЮЖЕФЦјЬхВњЩњ,дђПЩШЗЖЈВњЦЗжаКЌгаNa2SO3КЭNa2SO4ЁЃ
ЃЈ6ЃЉВтЖЈВњЦЗДПЖШЃКзМШЗГЦШЁWgВњЦЗ,гУЪЪСПеєСѓЫЎШмНт,вдЕэЗлзїжИЪОМС,гУ0.1000mol/LЕтЕФБъзМШмвКЕЮЖЈЁЃ(ЗДгІдРэЮЊЃК2S2O32-+I2=S4O62-+2I-)
ЂйЕЮЖЈжСжеЕуЪБ,ШмвКбеЩЋЕФБфЛЏЪЧ_______________________ЁЃ
ЂкЕЮЖЈМЧТМЪ§ОнШчЯТБэЃК
ЕЮЖЈЧАЖСЪ§/mL | ЕЮЖЈКѓЖСЪ§/mL | |
ЕквЛДЮ | 0.10 | 16.12 |
ЕкЖўДЮ | 1.10 | 17.08 |
ЕкШ§ДЮ | 1.45 | 19.45 |
ЕкЫФДЮ | 0.00 | 16.00 |
ЂлВњЦЗЕФДПЖШЮЊ(ЩшNa2S2O3ЁЄ5H2OЯрЖдЗжзгжЪСПЮЊM)______________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдкtЁцЪБЃЌAg2CrO4ЃЈщйКьЩЋЃЉдкЫЎШмвКжаЕФГСЕэШмНтЦНКтЧњЯпШчЭМЫљЪОЃЎгжжЊAgClЕФKsp=1.8ЁС10-10ЁЃЯТСаЫЕЗЈВЛе§ШЗЕФЪЧЃЈЁЁЁЁЃЉ

A. tЁцЪБЃЌYЕуКЭZЕуЪБAg2CrO4ЕФKspЯрЕШ
B. БЅКЭAg2CrO4ШмвКжаМгШыK2CrO4ВЛФмЪЙШмвКгЩYЕуБфЮЊXЕу
C. tЁцЪБЃЌAg2CrO4ЕФKspЮЊ1ЁС10-8
D. tЁцЪБЃЌНЋ0.01molЁЄL-1 AgNO3ШмвКЕЮШы20mL0.01molЁЄL-1 KClКЭ0.01molЁЄL-1 K2CrO4ЕФЛьКЯШмвКжаЃЌCl-ЯШГСЕэ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com