
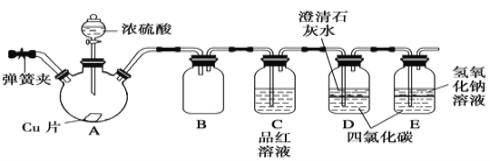
【题目】某学习小组设计如下实验方案研究Cu与浓H2SO4的反应(装置中的固定仪器和酒精灯均未画出):
请回答下列问题:
(1)仪器A的名称_________。Cu与浓H2SO4的反应的化学方程式为________________。
(2)D、E中CCl4的作用是___________________。
(3)加热过程中,随着反应的进行,A容器下有少量白色沉淀生成,你认为该沉淀物是_________,分析可能的原因是________________________________________。
(4)实验结束,打开A容器上的弹簧夹,通入一段时间空气,目的是______________。
(5)以下提供了三种制取CuSO4溶液的方法,你认为最合理的是____________(填序号),并且写出该方法对应的化学方程式_____________________________。
① 用铜与浓硫酸制备硫酸铜溶液。
② 将铜片在空气中加热,再溶解在稀硫酸中即可得到硫酸铜溶液。
③ 在硫酸和铜的混合容器中滴加 H2O2 溶液,过滤得硫酸铜溶液。
【答案】三颈烧瓶或三颈瓶 Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O 防止倒吸 CuSO4 浓硫酸中含水少,生成的硫酸铜较多,浓硫酸的吸水作用 将装置中的残留的SO2赶到E中,全部被氢氧化溶液吸收,防止空气污染 ③ Cu+H2SO4+H2O2= CuSO4+2H2O
CuSO4+SO2↑+2H2O 防止倒吸 CuSO4 浓硫酸中含水少,生成的硫酸铜较多,浓硫酸的吸水作用 将装置中的残留的SO2赶到E中,全部被氢氧化溶液吸收,防止空气污染 ③ Cu+H2SO4+H2O2= CuSO4+2H2O
【解析】
本实验利用如图所示的装置探究Cu与浓硫酸的反应并验证反应产物,Cu和浓硫酸反应生成二氧化硫气体,C装置用于验证产生的气体是否为二氧化硫,E装置用于吸收二氧化硫气体,防止污染空气,利用D、E所示的装置,装置中将导气管插入到四氯化碳中,二氧化硫不溶于四氯化碳,可以防止倒吸,据此分析。
(1)根据图示,仪器A的名称为三颈烧瓶;浓硫酸和Cu共热反应生成硫酸铜、二氧化硫、水,化学方程式为Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O,故答案为:三颈烧瓶;Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O,故答案为:三颈烧瓶;Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O;
CuSO4+SO2↑+2H2O;
(2)二氧化硫和强碱的反应使容器内压强减小,二氧化硫不溶于四氯化碳,可以采用四氯化碳来达到防止倒吸的目的,故答案为:防止倒吸;
(3)铜和浓硫酸反应生成硫酸铜,加热的情况下,由于A容器中出现大量白色烟雾,导致溶剂减少,且浓硫酸具有吸水性,所以会析出白色固体硫酸铜,故答案为:CuSO4;浓硫酸中含水少,生成的硫酸铜较多,浓硫酸的吸水作用;
(4)实验结束,打开A容器上的弹簧夹,通入一段时间空气,目的是将装置中的残留的SO2赶到E中,全部被氢氧化溶液吸收,防止空气污染,故答案为:将装置中的残留的SO2赶到E中,全部被氢氧化溶液吸收,防止空气污染;
(5)方法①用铜直接和浓硫酸反应,反应过程中生成二氧化硫气体,污染空气;方法②先将铜片在空气中加热生成氧化铜,再将氧化铜溶解在稀硫酸中,加热过程只能将铜片表面的Cu氧化为氧化铜,并不能将内部全部氧化,当表面上的氧化铜被硫酸反应完全后,内部的铜不能和稀硫酸反应;方法③在硫酸和铜的混合溶液中加入双氧水,双氧水这时起到氧化Cu的作用,这样生成物中就没有污染性气体出现,反应产物为硫酸铜和水,综上利用方法③制备硫酸铜最为合理,其反应方程式为Cu+H2SO4+H2O2=CuSO4+2H2O,故答案为:③;Cu+H2SO4+H2O2=CuSO4+2H2O。


 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:
【题目】化合物M是二苯乙炔类液晶材料的一种,最简单的二苯乙炔类化合物是![]() 。以互为同系物的单取代芳烃A、G为原料合成M的一种路线(部分反应条件略去)如下:
。以互为同系物的单取代芳烃A、G为原料合成M的一种路线(部分反应条件略去)如下:

回答下列问题:
(1)A的分子式为____________。
(2)D中含有的官能团是____________,分子中最多有____________个碳原子共平面。
(3)①的反应类型是____________,③的反应类型是____________。
(4)⑤的化学方程式为________________________________________________。
(5)B的同分异构体中能同时满足如下条件:①苯环上有两个取代基,②能发生银镜反应,共有________种(不考虑立体异构),其中核磁共振氢谱为5组峰,且峰面积比为6:2:2:1:1的是________(写结构简式)。
(6)参照上述合成路线,设计一条由苯乙烯和甲苯为起始原料制备![]() 的合成路线: _____________。
的合成路线: _____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室从含碘的废液(除H2O外,含有CCl4、I2、I 等)中回收碘,其实验过程如下,下列各项操作选用的装置不正确的是( )

选项 | A | B | C | D |
操作 | 操作X | 氧化 | 操作Y | 操作Z(加热及夹持装置略去) |
装置 |
|
|
|
|
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下KClO3与浓盐酸反应放出氯气,现按下图进行卤素的性质实验。玻璃管内装有分别滴有不同溶液的白色棉球,反应一段时间,对图中各部位颜色描述正确的是

选项 | ① | ② | ③ | ④ |
A | 黄绿色 | 橙色 | 白色 | 蓝色 |
B | 无色 | 橙色 | 白色 | 紫色 |
C | 黄绿色 | 橙色 | 无色 | 蓝色 |
D | 黄绿色 | 无色 | 无色 | 紫色 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,请回答下列问题
(1)基态B原子的电子排布式为_________;B和N相比,电负性较大的是_________,BN中B元素的化合价为_________;
(2)在BF3分子中,F-B-F的键角是_______,B原子的杂化轨道类型为_______,BF3和过量NaF作用可生成NaBF4,BF4-的立体结构为_______;
(3)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为________,层间作用力为________;
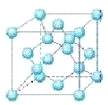
(4)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5pm,立方氮化硼晶胞中含有______各氮原子、________各硼原子,立方氮化硼的密度是_______g·cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Y、Z是金属单质,F、M是极易溶于水的气体,I元素是地壳中含量仅次于氧的非金属元素,化合物L是一种可用于制造发动机的新型无机非金属材料,其相对分子质量为140,其中I元素的质量分数为60%。这些物质间的相互转化关系如框图所示(部分产物已略去),根据框图及提示的信息回答下列问题。

(1)写出I元素在元素周期表中的位置_________________________________。
(2)K和F反应生成L和M的化学方程式_________________________________________。
(3)将5.2 g 金属Z与足量的X的稀溶液充分反应无气体放出,再向溶液中加入过量的NaOH溶液并加热,收集到0.448L气体F(标准状况),则整个过程中转移的电子数为_________。
(4)C是空气质量报告中的一种气体污染物,易形成酸雨;P气体是形成另一类型酸雨的主要污染物。实验室中若想用酸性高锰酸钾溶液除尽P气体,观察到的现象应是____________________,写出相应的离子方程式______________________________ 。
(5)已知向B的溶液中加入NaOH溶液时,先产生白色沉淀,迅速变为灰绿色,最后变为红褐色,请写出过量金属Y与X的稀溶液充分反应的离子方程式 ______________,该反应中被还原的X与未被还原的X的物质的量之比为___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示对应化学反应的离子方程式正确的是
A. 碳酸钙溶于稀醋酸:CaCO3+2H+=Ca2++H2O+CO2↑
B. 铜与稀硝酸反应:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O
C. 向NH4HCO3溶液中滴加过量Ba(OH)2溶液:HCO3-+OH-+Ba2+=H2O+BaCO3↓
D. 用银氨溶液检验乙醛中的醛基:CH3CHO+[Ag(NH3)2]++2OH- ![]() CH3COO-+NH4++NH3+ Ag↓+H2O
CH3COO-+NH4++NH3+ Ag↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等,实验室制备少量Mg(ClO3)2·6H2O的流程如下:

已知:①卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。
②四种化合物的溶解度(S)随温度(T)变化曲线如图所示。

(1)过滤所需要的主要玻璃仪器有___,加MgO后过滤所得滤渣的主要成分为___。
(2)加入BaCl2的目的是除去SO42-,如何检验SO42-已沉淀完全?答:___。
(3)加入NaClO3饱和溶液发生反应为:MgCl2+2NaClO3=Mg(ClO3)2+2NaCl↓,再进一步制取Mg(ClO3)2·6H2O的实验步骤依次为:①___;②___;③___;④过滤、洗涤。
(4)产品中Mg(ClO3)2·6H2O含量的测定:
步骤1:准确称量3.50 g产品配成100 mL溶液。
步骤2:取10 mL于锥形瓶中,加入10 mL稀硫酸和20 mL 1.000 mol·L-1的FeSO4溶液,微热。
步骤3:冷却至室温,用0.100 mol·L-1K2Cr2O7溶液滴定至终点,此过程中反应的离子方程式为:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O。
步骤4:将步骤2、3重复两次,平均消耗K2Cr2O7溶液15.00 mL。
①写出步骤2中发生反应的离子方程式:___
②产品中Mg(ClO3)2·6H2O的质量分数为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸亚乙烯酯是锂离子电池低温电解液的重要添加剂,其结构如图,下列有关该物质的说法正确的是
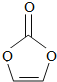
A. 分子式为C3H4O3
B. 1mol该分子能与2molH2加成
C. 分子中只有极性键
D. 标准状况下8.6g该物质完全燃烧得到6.72LCO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com