
【题目】书写下列描述中所发生化学反应的离子方程式
(1)稀硫酸与氢氧化钡反应:_________________________________。
(2)向澄清石灰水中加入少量碳酸氢钠溶液:___________________________。
(3)向硫酸氢钠溶液中加氢氧化钠溶液至中性:____________________。
(4)生活中可以用醋酸除去水垢:________________________________________。
(5)西汉刘安《淮南万毕术》中记载“曾青得铁则化为铜”,是湿法炼铜的最早描述:______________________。
(6)向饱和的碳酸钠溶液中通入CO2生成碳酸氢钠的沉淀______________________。
【答案】![]()
![]()
![]() 2CH3COOH+CaCO3=2CH3COO-+Ca2++CO2↑+H2O
2CH3COOH+CaCO3=2CH3COO-+Ca2++CO2↑+H2O ![]()
![]()
【解析】
(1)稀硫酸与氢氧化钡反应生成硫酸钡沉淀和水,发生反应的离子方程式为![]() ;
;
(2)向澄清石灰水中加入少量碳酸氢钠溶液,发生反应的离子方程式为![]() ;
;
(3)向硫酸氢钠溶液中加氢氧化钠溶液至中性,发生反应的离子方程式为![]() ;
;
(4)生活中可以用醋酸除去水垢,发生反应的离子方程式为2CH3COOH+CaCO3=2CH3COO-+Ca2++CO2↑+H2O;
(5)湿法炼铜即为Fe和硫酸铜溶液反应生成Cu和硫酸亚铁,发生反应的离子方程式为![]() ;
;
(6)向饱和的碳酸钠溶液中通入CO2生成碳酸氢钠的沉淀,发生反应的离子方程式为![]() 。
。


科目:高中化学 来源: 题型:
【题目】某盐酸的密度为![]() ,HCl的质量分数为
,HCl的质量分数为![]() ,试计算:
,试计算:
(1)该盐酸的物质的量浓度是多少?(小数点后保留两位)_________
(2)在足量的该盐酸溶液中,加入镁粉和铝粉混合物![]() ,充分反应共生成
,充分反应共生成![]() 气体(标准状况),求混合物中镁和铝的质量各为多少?____________,_______________
气体(标准状况),求混合物中镁和铝的质量各为多少?____________,_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
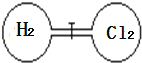
【题目】室温下如图,关闭活塞,在左右两室(体积相同)各充入一定量H2和Cl2,且恰好使两容器内气体密度相同,打开活塞,点燃使H2与Cl2充分反应生成氯化氢气体:H2+Cl2=2HCl,恢复到原温度后,下列判断正确的是
A. 开始时左右两室分子数相同
B. 最终容器内无H2存在
C. 反应前后H2室压强相同
D. 最终容器内密度与原来相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①标准状况下,1体积水中最多能溶解500体积的HCl;②饱和NaCl溶液的浓度约为5.00mol·L-1。
(1)在标准状况下,将448LHCl气体溶于1 L水中,所得溶液A的密度为1.20 g·cm-3,则溶液A中HCl的物质的量浓度为____。(本题计算结果均取三位有效数字)
(2)若使1L饱和氯化钠溶液中Cl-浓度与溶液A中的Cl-浓度相等,则在1LNaCl饱和溶液中还应溶解约___L标准状况下HCl气体(溶液体积变化忽略不计,不考虑氯化钠析出)。
(3)若将10.0mL溶液A稀释成500mL溶液B,则溶液B中HCl的物质的量浓度为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素R、X、Y、Z的原子序数依次增大,由这些元素组成的物质之间的转化关系如图所示,其中c、d为单质,a、b、g为二元化合物。b是10电子分子,g是18电子分子。下列说法正确的是

A. 同温同浓度的e和f溶液,后者pH较大
B. 含X、R、Z三种元素的化合物只有一种
C. 0.1mol的d与足量的e溶液反应转移电子数约为 1.204×1023
D. e和f含化学键类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中,溶质的物质的量浓度为1molL-1 的是( )
A.将40gNaOH溶于1 L 水所得的溶液
B.往100mL2molL-1的NaNO3溶液中加入100 mL水所得的溶液
C.将16g CuSO4·5H2O溶于水配成100mL的溶液
D.含K+为2 molL-1的K2SO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钛(Ti)具有硬度大、熔点高、耐酸碱腐蚀的优点,被广泛用于航空航天、医疗卫生及日常生活中。以钛铁矿(主要成分为FeTiO3)为主要原料冶炼金属钛的生产工艺如图所示。

回答下列有关问题:
(1)钛铁矿(精矿)中加入浓硫酸除生成TiOSO4外,还生成水和另外一种硫酸盐,且反应前后Fe的化合价不变,则FeTiO3中Ti的化合价为____。
(2)上述流程图中加入“铁屑”的目的是___(填字母)。
A.防止Fe2+被氧化 B.与Fe3+反应
C.防止Fe2+水解 D.防止Fe3+水解
(3)溶液Ⅰ经“操作a”可得固体副产品甲,则操作a的名称为_______,副产品甲的化学式是_____。
(4)已知钛酸难溶于水,其化学式为H2TiO3。则溶液Ⅱ中加入水,加热时发生的化学方程式为_____。
(5)“操作b”为加热,则中间产品乙的化学式为______。
(6)一定条件下,利用气体丙与氢气可合成甲醇,该合成反应的化学方程式为____________,甲醇的电子式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素 X、Y、Z、W 原子序数依次增大,X 是地壳中含量最多的元素,Y 原子的最外层只有一个电子,Z 位于元素周期表ⅢA族,W 与X属于同一主族。下列说法正确的是
A. 原子半径:r(W) > r(Z) > r(Y)
B. 由X、Y 组成的化合物中均不含共价键
C. Y 的最高价氧化物的水化物的碱性比Z的弱
D. X 的简单气态氢化物的热稳定性比W的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Ca3(PO4)2与SiO2、C高温共热可以反应得到CaSiO3、P4蒸气和CO.反应如下:Ca3(PO4)2+SiO2+C![]() CaSiO3+P4↑+CO↑
CaSiO3+P4↑+CO↑
(1)配平该反应方程式,并标出电子转移方向和数目____________.
_____Ca3(PO4)2+_____SiO2+_____C![]() _____CaSiO3+_____P4↑+_____CO↑
_____CaSiO3+_____P4↑+_____CO↑
(2)该反应中被还原的元素是_____,氧化产物是_____.
(3)每消耗24.0g碳时,有_____个电子发生转移,生成P4_____g.
(4)反应所得混合气体,折算成标况下,其气体密度为_____g/L(保留两位小数).与该反应中涉及到的磷元素相同主族的氮元素,是造成水体富营养化的主要原因.若某污水中NH4Cl含量为180mg/L.
(5)写出NH4Cl的电子式_____.
(6)为除去废水中的NH4+,向103L该污水中加入0.1mol/LNaOH溶液,发生如下反应:NH4++OH﹣→NH3+H2O.则理论上需要NaOH溶液的体积为_____L(计算结果保留两位小数)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com