
【题目】下列配制的溶液浓度偏高的是( )
A.配制硫酸用量筒量取硫酸时俯视刻度线
B.配制盐酸定容时,仰视容量瓶刻度线
C.NaOH溶解后未经冷却即注入容量瓶至刻度线
D.称量4gNaOH配制0.1mol/L NaOH溶液1000mL时,砝码错放左盘
 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)陶瓷是一种新型无机非金属材料,利用它较高的体积电阻率、绝缘强度大、导热性能好,可用作大功率半导体器件的绝缘基片、大规模和超大规模集成电路的散热基片和封装基片。工业上可用氮气和铝在高温下直接化合法来制备氮化铝粉体(AlN粉体在潮湿的空气中易发生水解反应)。已知:实验室可用饱和亚硝酸钠(NaNO2)溶液和氯化铵溶液共热制取氮气。现提供以下装置来模拟工业制取AlN粉体。
(1)写出实验室制取氮气的化学方程式:___________________________。
(2)请从下图中选择合适的装置按顺序组装一套用氮气和铝粉制AlN的装置(装置可以根据需要重复使用):________________________________。
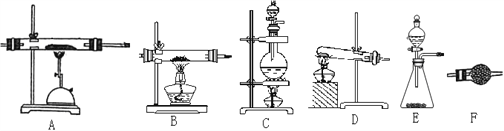
(3)实验开始后应先给_______处装置加热一段时间再给另一处装置加热,这样操作的原因是:_______________。
(4)已知:氮化铝(AlN)既能溶于强酸,又能溶于强碱,试写出AlN与HCl溶液反应的化学方程为________________。
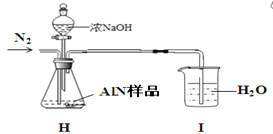
(5)AlN制备过程中存在一些副反应致生成的AlN不纯。 研究小组的同学取2.0500 g AlN样品与浓NaOH溶液充分反应,通过测定产生氨气的量来测定AlN的纯度(假设杂质与碱反应不生成NH3,忽略NH3在强碱性溶液中的溶解)。实验装置如下:请帮该同学纠正装置中一处明显错误:___________________。当H中反应完全后持续缓慢通入氮气将生成的氨全部吹入I中被水吸收。然后将I中氨水_________________________________________________________________________(请补充完这步操作,需根据后面数据计算作答),用_______取25.00mL氨水于锥形瓶中并加入几滴_______作指示剂,用0.1000mol/L的盐酸滴定至终点,消耗盐酸体积为22.50mL,经计算得AlN的纯度为90.00 %。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能把乙醇、甲酸、乙酸、葡萄糖溶液用一种下列试剂区分开的是( )
A. 新制氢氧化铜浊液 B. 碳酸钠溶液 C. 酸性高锰酸钾溶液 D. 紫色石蕊试液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】特斯拉全电动汽车使用的是钴酸锂(LiCoO2)电池,其工作原理如右图,A极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料。隔膜只允许特定的离子通过,电池反应式LixC6+Li1-xCoO2![]() C6+LiCoO2,下列说法不正确的是
C6+LiCoO2,下列说法不正确的是
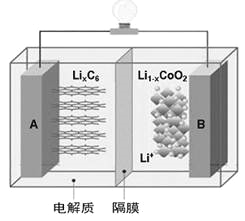
A. 据题意分析可知该隔膜只允许Li+通过,放电时Li+从左边移向右边
B. 放电时,正极锂的化合价未发生改变
C. 废旧钴酸锂电池进行“放电处理”让Li+进入石墨中而有利于回收
D. 充电时阳极的电极反应式为:LiCoO2-xe-=Li1-xCoO2+xLi+
【答案】C
【解析】电解质是能传导Li+的高分子材料,所以隔膜只允许Li+通过,根据图示,A是负极,放电时Li+从左边移向右边,故A正确;放电时,正极Co元素化合价降低、锂的化合价未发生改变,故B正确;“放电处理”,Li+进入Li1-xCoO2中,故C错误;充电时阳极失电子发生氧化反应,电极反应式为:LiCoO2-xe-=Li1-xCoO2+xLi+,故D正确。
点睛:原电池中负极失电子发生氧化反应,正极得电子发生还原反应;电解质溶液中阳离子移向正极、阴离子移向负极。
【题型】单选题
【结束】
7
【题目】下列溶液中各微粒的浓度关系正确的是
A. 0.2 mol·L-1的Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3)
B. pH相等的NaF与CH3COOK溶液:[c(Na+)-c(F-)]>[c(K+)-c(CH3COO-)]
C. pH相等的①NH4Cl ②(NH4)2SO4 ③NH4HSO4溶液,NH4+大小顺序为①=②>③
D. 0.2 mol·L-1HCl与0.1 mol·L-1NaAlO2溶液等体积混合:c(Cl-)>c(Na+)>c(H+)>c(Al3+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t℃时,将 2molSO2 和 1molO2 通入体积为 2L 的恒温恒容密闭容器中,发生如下反应:2SO2(g)+O2(g)![]() 2SO3(g) ,△H=-196.6kJ/mol. 2min 时反应达到化学平衡,此时测得反应物O2 还剩余 0.8mol,请填写下列空白:
2SO3(g) ,△H=-196.6kJ/mol. 2min 时反应达到化学平衡,此时测得反应物O2 还剩余 0.8mol,请填写下列空白:
(1)从反应开始到达化学平衡,生成 SO3 的平均反应速率为__________ ;平衡时,SO2 转化率为_____________
(2)下列叙述能证明该反应已达到化学平衡状态的是 __________
A.容器内压强不再发生变化 B.SO2 的体积分数不再发生变化
C.容器内气体原子总数不再发生变化 D.相同时间内消耗 2nmolSO2 的同时消耗 nmolO2
E.相同时间内消耗 2nmolSO2 的同时生成 nmolO2 F.混合气体密度不再变化
(3)以下操作会引起化学反应速率变快的是__________
A.向容器中通入O2 B.扩大容器的体积 C.使用正催化剂
D.升高温度 E.向容器中通入氦气。
(4)t2℃时,若将物质的量之比 n(SO2) :n(O2)=1:1 的混合气体通入一个恒温恒压的密闭容器中,反应达到平衡时,混合气体体积减少了 20%。则SO2 的转化率为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】材料的应用推动了城市发展,很多方面涉及到了化学反应,认真回答下列问题:
(1)我国早在春秋战国就开始生产和使用铁器,写出用赤铁矿为原料炼铁的化学方程式:___________________。
(2)氢氧化钾是我国古代纺织业常用的漂洗洗涤剂,古人将贝壳(主要成分是碳酸钙)灼烧后的固体与草木灰(主要成分是碳酸钾)在水中相互作用,便可得到氢氧化钾。请按要求用化学方程式表示上述反应:分解反应:___________,化合反应:_____________,复分解反应:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1mol某烃在氧气中充分燃烧,需要消耗氧气179.2L(标准状况),它在光照条件下与氯气反应能生成3种不同的一氯代物。则该烃的结构简式是
A. 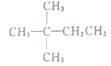 B. CH3CH2CH2CH2CH3
B. CH3CH2CH2CH2CH3
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,相同体积、相同pH的盐酸和醋酸溶液分别加水稀释,平衡pH随溶液体积变化的曲线如图所示。据图判断正确的是
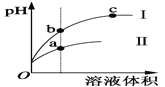
A. Ⅱ为盐酸稀释时pH变化曲线
B. b点溶液的导电性比c点溶液的导电性弱
C. a点KW的值比c点KW的值大
D. 与相同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积,a点比b点大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com