
����Ŀ������ͼ�а�������Ϣ����������������ȷ���� ( )
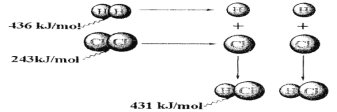
A��������������Ӧ����1 mol�Ȼ������壬��Ӧ����248 kJ������
B��436 kJ/mol��ָ�Ͽ�1 mol H2�е�H��H����Ҫ�ų�436 kJ������
C��������������Ӧ����2 mol�Ȼ������壬��Ӧ�ų�183 kJ������
D��431kJ/mol��ָ����2 mol HCl�е�H��Cl����Ҫ�ų�431 kJ������
���𰸡�C
��������
���������A����Ӧ����2mol�Ȼ�������ų���������431��2-436 -248 =183kJ/mol��A�����B��436kJ/mol��ָ�Ͽ�1molH2�е�H-H����Ҫ����436kJ��������B�����C����Ӧ����2mol�Ȼ�������ų���������431kJ/mol��2mol-436kJ/mol-248kJ/mol=183kJ/mol��C����ȷ��D��31kJ/mol��ָ����1molHCl�е�H-Cl����Ҫ�ų�431kJ��������D�����ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£�������ijһ��Ӧ��M��N�����ʵ����淴Ӧʱ��仯��������ͼ�����б�������ȷ���ǣ� �� 
A.��Ӧ�Ļ�ѧ����ʽΪ��2MN
B.t2ʱ�����淴Ӧ������ȣ��ﵽƽ��
C.t3ʱ������Ӧ���ʴ����淴Ӧ����
D.t1ʱ��N��Ũ����MŨ�ȵ�2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25���1.01��105Paʱ����Ӧ2N2O5��g���T4NO2��g��+O2��g����H=+56.76kJ/mol���Է����е�ԭ���ǣ�������
A.�����ȷ�Ӧ
B.�Ƿ��ȷ�Ӧ
C.���ؼ��ٵķ�Ӧ
D.������ЧӦ��������ЧӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������´��ڷ�Ӧ��CO(g)��H2O(g) ![]() CO2(g)��H2(g)����H����Q kJ/mol(Q>0)������������ͬ��2 L���ݾ���(�����û����������)�ܱ����������������������г���1 mol CO��1 mol H2O�������г���1 mol CO2��1 mol H2�������г���2 mol CO��2 mol H2O��700 �������¿�ʼ��Ӧ���ﵽƽ��ʱ�������������̶�Ӧ�������仯ֵ�ֱ�ΪQ1��Q2��Q3������˵����ȷ����
CO2(g)��H2(g)����H����Q kJ/mol(Q>0)������������ͬ��2 L���ݾ���(�����û����������)�ܱ����������������������г���1 mol CO��1 mol H2O�������г���1 mol CO2��1 mol H2�������г���2 mol CO��2 mol H2O��700 �������¿�ʼ��Ӧ���ﵽƽ��ʱ�������������̶�Ӧ�������仯ֵ�ֱ�ΪQ1��Q2��Q3������˵����ȷ����
A. 2Q1��2Q2��Q3
B. ��������CO�İٷֺ�������������CO�İٷֺ�����
C. �������з�Ӧ��ƽ�ⳣ�����������з�Ӧ��ƽ�ⳣ��С
D. ��������CO��ת��������������CO2��ת����֮�͵���1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪: 25�桢101 kPa�£��� 2 Na(s) + 1/2 O2(g) = Na2O(s) ��H1 = - 414 kJ / mol
�� 2 Na(s) + O2(g) = Na2O2(s) ��H2 = - 511 kJ / mol
����˵����ȷ����
A. ������������������Ӹ����Ȳ����
B. ���������ɵ����ʵ����IJ��ת�Ƶ�������ͬ
C. ������Na������O2��Ӧ����Na2O�����¶���������Na2O�������ӿ�
D. 25�桢101 kPa�£�Na2O2(s) + 2 Na(s) = 2 Na2O(s) ��H = -317 kJ / mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ͻ�������������й㷺Ӧ�á�
��1�������о�����������������������������Һ������Na[Al(OH)4]��������������ˮ�з�����ʽ����ĵ��뷽��ʽΪ________________________________��
��2��Ŀǰ�����ڶ����̼�Ȼ�ԭ-�Ȼ���ұ�������о��϶࣬���ø÷���ұ�����������Ƚ����ֻ�����
��֪����Al2O3(s)+AlCl3(g)+3C(s)=====3AlCl(g)+3CO(g) ��H1
��3AlCl(g)====2Al(l)+AlCl3(g) ��H2
��Al(l)====Al(s) ��H3
��Al2O3(s)+3C(s)====2Al(s)+3CO(g) ��H4=___________(�ú���H1����H2����H3�Ĵ���ʽ��ʾ)��
��3����֪��Al4C3�����̼�Ȼ�ԭ-�Ȼ���ұ�������м�������ˮ��Ӧ��������Y��Y�Ǻ���������������2L�����ܱ������г���2mol Y��2molˮ������һ�������·�����Ӧa Y(g)+bH2O(g) ![]() c CO(g)+dH2(g) ��H�����Y��ƽ��ת���ʦ�(Y)���¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
c CO(g)+dH2(g) ��H�����Y��ƽ��ת���ʦ�(Y)���¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
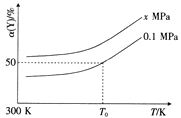
��������Ӧ�ġ�H_______0(�>����<����=��)��
��ͼ���У�x_________0.1(�>����<����=��)��
����T0K��0.1MPaʱ��������Ӧ��ƽ�ⳣ��K=____________��
�����������Ӧ�ķ�Ӧ���ʵĴ�ʩ��_______________________________ (�������)��
�ݴ�������Ӧ��ϵ�з����H2(����������CO)��Ϊ�ϳɰ���ԭ������Ϊ����COʹ�����ж���ԭ������ͨ��ϳ���֮ǰ��������NH3��ϣ�����[Cu(NH3)2]Ac��Һ����CO����Ӧԭ��Ϊ[Cu(NH3)2]Ac(aq)+CO(g)+NH3(g) ![]() [Cu(NH3)3]Ac��CO(aq) ��H<0�������¶ȡ�ѹǿ�����濼�ǣ���[Cu(NH3)2]Ac��Һ����CO������������________________________��
[Cu(NH3)3]Ac��CO(aq) ��H<0�������¶ȡ�ѹǿ�����濼�ǣ���[Cu(NH3)2]Ac��Һ����CO������������________________________��
��4���ҹ��״��ĺ�ˮ���������Ϊ�������ԽӴ������������Ͻ���Ϊ�������������Եĺ�ˮΪ�������Һ������ܷ�ӦΪ4Al+3O2+6H2O===4Al(OH)3����д����ˮ��ص�������Ӧʽ��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������刺���������ƽ�����ʵ���ҿ���NaClO3��ԭ����ȡ(���������ܽ�ȼ���ͼ)����ʵ���������£�
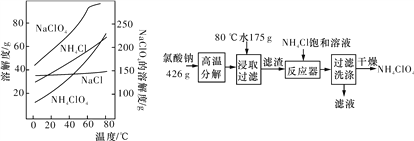
��1�������Ƹ��·ֽ����ɸ������ƺ��Ȼ��ƵĻ�ѧ����ʽΪ____��
��2��80 ��ʱ��ȡҺ��ȴ��0 ����������������Ҫ�ɷ�Ϊ___(д��ѧʽ)��
��3����Ӧ���м����Ȼ�隣�����Һ������Ӧ�����ӷ���ʽΪ___��
��4����֪��2NH4ClO4![]() N2����2O2����Cl2����4H2O���ֿ��ṩ�����Լ���
N2����2O2����Cl2����4H2O���ֿ��ṩ�����Լ���
a������ʳ��ˮ����b��ŨH2SO4����c��NaOH��Һ d��Mg e��Cu f��Fe
������ͼװ�öԸ���������ȷֽ��������������ֱ�������ջ��ռ���
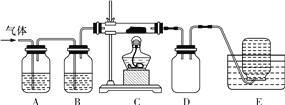
��E���ռ��������������____(�ѧʽ)��
��A��B��C��ʢ�ŵ�ҩƷ���ο�����___(��������������)��
��.a��b��c������.c��b��e������.b��c��f
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(H)�dz����ڵ��ƾ��в�ݮ�����ѡ�ӣ�ҡ�����������ζ��ʳ���㾫�����ķ���ʽΪC10H10O2���ҷ�����ֻ����1��������������ֻ��һ��ȡ���������ú�������ǿɳ�������л��������е�ijЩ���ţ��ֲ��H���ӵĺ����������ͼ��ʾ��

��֪JΪ����������һ��ͬ���칹�壬����ӽṹģ������ͼ��ʾ(ͼ��������֮������߱�ʾ������˫���Ȼ�ѧ��)��

�Իش��������⣺
��1����������(H)�Ľṹ��ʽΪ_______��
��2���ֲ��A�ĺ˴Ź�������ͼ��6���壬�����֮��Ϊ1��2��2��2��1��2���÷�����AΪԭ�Ϻϳ�H��·������(���ַ�Ӧ��ͷ�Ӧ��������ȥ)��

�ٻ�����F�еĹ�������__________(������)��
��F��G�ķ�Ӧ������__________��
����д���л�ѧ����ʽ��
F��I��____________________��
G��H��_________________________��
������F��ͬ���칹�����࣬������һ�����ͨʽ![]() ��ʾ(����X��Y����Ϊ��ԭ��)����д����������ͨʽ���ܷ���������Ӧ���������ʵĽṹ��ʽ��_____________________��
��ʾ(����X��Y����Ϊ��ԭ��)����д����������ͨʽ���ܷ���������Ӧ���������ʵĽṹ��ʽ��_____________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com