
【题目】用MnO2和浓盐酸制取纯净干燥的氯气,并让氯气与铜粉反应制取纯净的无水CuCl2 , 装置如图1所示.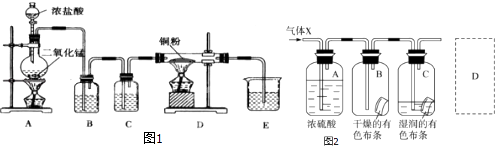
请回答下列问题:
(1)B中选用的试剂是饱和食盐水,其作用是;C中选用的试剂是 , 其作用是 .
(2)D中反应的化学方程式是 , 将此生成物溶于少量水,得到色溶液.
(3)某学生应用如图2所示的方法研究物质的性质,其中气体X的主要成分是氯气,杂质是空气和水蒸气.回答下列问题:①该项研究(实验)的主要目的是 .
②与研究目的直接相关的实验现象是 .
③从物质性质的方面来看,这样的实验设计还存在事故隐患,事故表现是 .
④请在图中的D处以图的形式表明克服事故隐患的措施 .
【答案】
(1)除去Cl2中的HCl;浓硫酸;除去Cl2中的水蒸气
(2)Cu+Cl2 ![]() CuCl2;蓝
CuCl2;蓝
(3)比较Cl2与HClO谁有漂白性;B中的布条不退色,C中的布条退色;氯气外逸,污染环境;
【解析】解:(1)从A中制得的氯气含有杂质氯化氢、水蒸气,依次通过盛有饱和食盐水、和浓硫酸的洗气瓶除去;所以答案是:除去Cl2中的HCl;浓硫酸;除去Cl2中的水蒸气;(2)氯气和铜在高温条件下化合生成氯化铜方程式为:Cu+Cl2 ![]() CuCl2 , 将此生成物溶于少量水得到氯化铜溶液为蓝色溶液,所以答案是:Cu+Cl2
CuCl2 , 将此生成物溶于少量水得到氯化铜溶液为蓝色溶液,所以答案是:Cu+Cl2 ![]() CuCl2 , 蓝;(3)①由B、C可知起对比作用,则该实验的目的为比较Cl2和HClO谁有漂白性,所以答案是:探究氯气具有漂白性的条件;②浓硫酸具有吸水性,其作用为吸收气体中的水蒸汽干燥氯气,干燥的氯气不具有漂白性,则与研究目的直接相关的实验现象是B中的布条不褪色,C中的布条褪色,所以答案是:B中有色布条不退色,C中有色布条退色;③从物质性质的方面来看,这样的实验设计还存在事故隐患,事故表现是氯气有毒,排放到空气中,污染环境,所以答案是:氯气外逸,污染环境.④图中的D处以图的形式表明克服事故隐患的措施是应进行尾气处理,不能随意排放到空气中,应加尾气处理装置,
CuCl2 , 蓝;(3)①由B、C可知起对比作用,则该实验的目的为比较Cl2和HClO谁有漂白性,所以答案是:探究氯气具有漂白性的条件;②浓硫酸具有吸水性,其作用为吸收气体中的水蒸汽干燥氯气,干燥的氯气不具有漂白性,则与研究目的直接相关的实验现象是B中的布条不褪色,C中的布条褪色,所以答案是:B中有色布条不退色,C中有色布条退色;③从物质性质的方面来看,这样的实验设计还存在事故隐患,事故表现是氯气有毒,排放到空气中,污染环境,所以答案是:氯气外逸,污染环境.④图中的D处以图的形式表明克服事故隐患的措施是应进行尾气处理,不能随意排放到空气中,应加尾气处理装置,  所以答案是:
所以答案是:  .
.
【考点精析】本题主要考查了氯气的实验室制法的相关知识点,需要掌握实验室制法:MnO2+4HCl(浓)=MnCl2+Cl2↑+2H2O才能正确解答此题.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】有转化关系(其他产物及反应所需条件均已略去).
A ![]() B
B ![]() C
C ![]() D
D ![]() E
E ![]() F,以下推断错误的是( )
F,以下推断错误的是( )
A.当X是盐酸时,则F是稀硝酸
B.当X是氢氧化钠时,则F是稀硝酸
C.当X是氢氧化钠时,B跟Cl2反应可能有白烟现象
D.当X是氢氧化钠时,B能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表述正确的是( )
A.氢氧根离子的电子式是 ![]()
B.二氧化碳分子的比例模型是 ![]()
C.芳香烃的组成通式是CnH2n﹣6(n≥6)
D.12C和14C的原子结构示意图均可表示为 ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有m g某气体,它由双原子分子构成,它的摩尔质量为Mg/mol.若阿伏加德罗常数用NA表示,则:
(1)该气体所含原子总数为 .
(2)该气体在标准状况下的体积为
(3)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为 .
(4)该气体溶于水后形成V L溶液,其溶液中溶质的物质的量浓度为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图用铜锌原电池(电解质溶液为稀硫酸)在铁棒上电镀铜,下列叙述正确的是( )

A. 铜在原电池中作负极,在电镀池中作阳极
B. 原电池溶液增加的质量比电镀池阴极增加的质量大
C. 锌棒每减少0.65 g,导线上转移的电子就为0.02 mol
D. 电镀池中的电解质溶液可用ZnSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列在溶液中能大量共存的离子组是
A. K+、H+、SO42-、CO32- B. Na+、Ca2+、SO42-、NO3-
C. Cu2+、Mg2+、Cl-、S2- D. Na+、Cu2+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组比较不正确的是 ( )
A. 锂与水反应不如钠与水反应剧烈
B. 碱金属Li、Na、K单质都能在O2中燃烧生成过氧化物
C. 熔、沸点:Li>Na>K
D. 碱性:LiOH<NaOH<KOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳和氮的化合物与人类生产、生活密切相关.
(1)C、CO、CO2在实际生产中有如下应用:a.2C+SiO2 ![]() Si+2CO b.3CO+Fe2O3
Si+2CO b.3CO+Fe2O3 ![]() 2Fe+3CO2
2Fe+3CO2
c.C+H2O ![]() CO+H2 d.CO2+CH4
CO+H2 d.CO2+CH4 ![]() CH3COOH
CH3COOH
上述反应中,理论原子利用率最高的是 .
(2)有机物加氢反应中镍是常用的催化剂.但H2中一般含有微量CO会使催化剂镍中毒,在反应过程中消除CO的理想做法是投入少量SO2 , 为搞清该方法对催化剂的影响,查得资料:
则:①不用通入O2氧化的方法除去CO的原因是 .
②SO2(g)+2CO(g)=S(s)+2CO2(g)△H= .
(3)汽车尾气中含大量CO和氮氧化物(NO2)等有毒气体.①活性炭处理NO的反应:C(s)+2NO(g)N2(g)+CO2 (g)△H=﹣akJmol﹣1(a>0)
若使NO更加有效的转化为无毒尾气排放,以下措施理论上可行的是: . 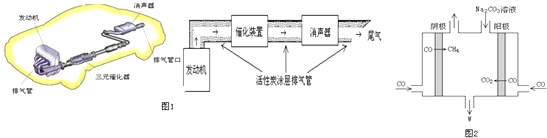
a.增加排气管长度 b.增大尾气排放口
c.添加合适的催化剂 d.升高排气管温度
②在排气管上添加三元催化转化装置,CO能与氮氧化物(NO2)反应生成无毒尾气,其化学方程式是 .
(4)利用CO2与H2反应可合成乙醚.以KOH为电解质溶液,组成乙醚﹣﹣﹣﹣空气燃料电池,该电池工作时其负极反应式是 .
(5)电解CO制备CH4和W,工作原理如图2所示,生成物W是 , 其原理用电解总离子方程式解释是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式中不正确的是( )
A.H2SO4═2H++SO ![]()
B.Ba(OH)2═Ba2++2OH﹣
C.NaNO3═Na++NO ![]()
D.KClO3═K++Cl﹣+3O2﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com