
【题目】如图用铜锌原电池(电解质溶液为稀硫酸)在铁棒上电镀铜,下列叙述正确的是( )

A. 铜在原电池中作负极,在电镀池中作阳极
B. 原电池溶液增加的质量比电镀池阴极增加的质量大
C. 锌棒每减少0.65 g,导线上转移的电子就为0.02 mol
D. 电镀池中的电解质溶液可用ZnSO4溶液
【答案】C
【解析】电镀的要求是:镀层金属为阳极,待镀的部件为阴极,含有镀层金属阳离子的溶液为电镀液。所以,在铁棒上电镀铜时,铜为阳极,铁为阴极,溶液中一定要有铜离子。在锌铜原电池中,锌为负极,铜为正极,所以选项A错误。电镀池阴极的反应为Cu2++2e-=Cu,原电池的总反应为Zn+H2SO4=ZnSO4+H2↑,所有电极上的得失电子数一定相等。假设转移2mol电子,此时原电池溶液增加的质量为65-2=63g,电镀池阴极析出1molCu,质量为64g,所以选项B错误。Zn转化为Zn2+,所以锌棒每减少0.65 g(0.01mol),导线上转移的电子就为0.02 mol,选项C正确。电镀池的电解液应该是硫酸铜溶液,选项D错误。


科目:高中化学 来源: 题型:
【题目】NA为阿伏伽德罗常数的值.下列说法正确的是( )
A.过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.4NA
B.23g Na 与足量H2O反应完全后可生成NA个H2分子
C.标准状况下,22.4LN2和H2混合气中含NA个原子
D.3mol单质Fe完全转变为Fe3O4 , 失去8 NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过.下列有关叙述不正确的是( ) 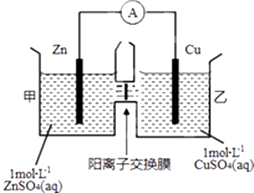
A.Zn电极上发生氧化反应
B.电子的流向为Zn→电流表→Cu
C.SO42﹣由乙池通过离子交换膜向甲池移动
D.电池工作一段时间后,乙池溶液的总质量明显增加
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羟基扁桃酸是药物合成的重要中间体,它可由苯酚和乙醛酸反应制得: 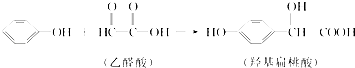
下列有关说法正确的是( )
A.苯酚和羟基扁桃酸互为同系物
B.羟基扁桃酸分子中至少有12个原子共平面
C.乙醛酸在核磁共振氢谱中只有1个吸收峰
D.常温下,1 mol羟基扁桃酸只能与1 mol Br2反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃时,CaSO4在水中的沉淀溶解平衡曲线,如图所示,向100mL该条件下的CaSO4饱和溶液中,加入400mL 0.01mol/L的Na2SO4溶液,针对此过程的下列叙述正确的是( ) 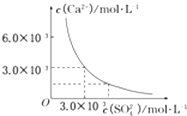
A.溶液中析出CaSO4沉淀,最终溶液中c(SO ![]() )较原来大
)较原来大
B.溶液中无沉淀析出,溶液中c(Ca2+)、c(SO ![]() )都变小
)都变小
C.溶液中析出CaSO4沉淀,溶液中c(Ca2+)、c(SO ![]() )都变小
)都变小
D.溶液中无沉淀析出,但最终溶液中c(SO ![]() )较原来大
)较原来大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用MnO2和浓盐酸制取纯净干燥的氯气,并让氯气与铜粉反应制取纯净的无水CuCl2 , 装置如图1所示.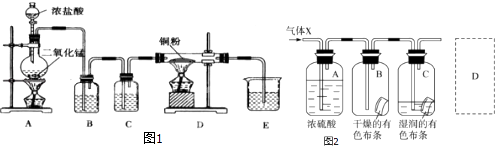
请回答下列问题:
(1)B中选用的试剂是饱和食盐水,其作用是;C中选用的试剂是 , 其作用是 .
(2)D中反应的化学方程式是 , 将此生成物溶于少量水,得到色溶液.
(3)某学生应用如图2所示的方法研究物质的性质,其中气体X的主要成分是氯气,杂质是空气和水蒸气.回答下列问题:①该项研究(实验)的主要目的是 .
②与研究目的直接相关的实验现象是 .
③从物质性质的方面来看,这样的实验设计还存在事故隐患,事故表现是 .
④请在图中的D处以图的形式表明克服事故隐患的措施 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于各图象的解释或结论正确的是( )
A.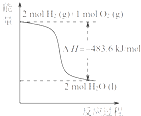 热化学方程式是H2(g)+
热化学方程式是H2(g)+ ![]() O2(g)=H2O(g)△H=﹣241.8 kJ/mol
O2(g)=H2O(g)△H=﹣241.8 kJ/mol
B.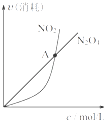 对于恒温恒容条件下的反应2NO2(g)?N2O4(g),A点为平衡状态
对于恒温恒容条件下的反应2NO2(g)?N2O4(g),A点为平衡状态
C.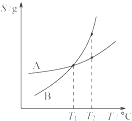 将A,B饱和溶液分别由T1℃升温至T2℃时,溶质的质量分数B>A
将A,B饱和溶液分别由T1℃升温至T2℃时,溶质的质量分数B>A
D.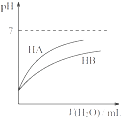 同温度、同浓度的NaA溶液与NaB溶液相比,其pH前者小于后者
同温度、同浓度的NaA溶液与NaB溶液相比,其pH前者小于后者
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】HA和HB两种酸的溶液分别加水稀释时,pH变化的简图如图所示,下列叙述中不正确的是( )

A. HA是一种强酸
B. x点,c(A-)=c(B-)
C. HB是一种弱酸
D. 原溶液中HA的物质的量浓度为HB的10倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对氯苯甲酸是合成非甾族消炎镇痛药的中间体,还能用于燃料和浓药的合成,实验室中制备对氯苯甲酸的反应、装置图如图2: 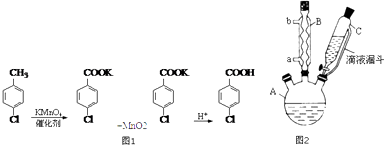
常温条件下的有关数据如表所示:
相对分子质量 | 熔点/℃ | 沸点/℃ | 密度/gcm﹣3 | 颜色 | 水溶性 | |
对氯甲苯 | 126.5 | 7.5 | 162 | 1.07 | 无色 | 难溶 |
对氯苯甲酸 | 156.5 | 243 | 275 | 1.54 | 白色 | 微溶 |
对氯苯甲酸钾 | 194.5 | 具有盐的通性,属于可溶性盐 | ||||
实验步骤:在规格为250mL的装置A中加入一定量的催化剂、适量KMnO4、100mL水;安装好装置,在滴液漏斗中加入6.00mL对氯甲苯,在温度为93℃左右时,逐滴滴入对氯甲苯;控制温度在93℃左右,反应2h,过滤,将滤渣用热水洗涤,使洗涤液与滤液合并,加入稀硫酸酸化,加热浓缩;然后过滤,将滤渣用冷水进行洗涤,干燥后称量其质量为7.19g.
请回答下列问题:
(1)装置B的名称是 .
(2)量取6.00mL对氯甲苯应选用的仪器是 . (填选仪器序号).
A.10mL量筒
B.50mL容量瓶
C.50mL酸式滴定管
D.50mL碱式滴定管
(3)控制温度为93℃左右的方法是 . 对氯甲苯的加入方法是逐滴加入而不是一次性加入,原因是 .
(4)第一次过滤的目的是 , 滤液中加入稀硫酸酸化,可观察到的实验现象是 .
(5)第二次过滤所得滤渣要用冷水进行洗涤,其原因是 .
(6)本实验的产率是(填标号).
A.60%
B.70%
C.80%
D.90%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com