
����Ŀ��(1)��״����VL�����ܽ���1Lˮ��(ˮ���ܶȽ���Ϊ1g/mL),������Һ���ܶ�Ϊ��g/mL,�����Һ�����ʵ����ʵ���Ũ��Ϊ______��
(2)��11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4��,ÿ1molCuSO4�������������ʵ�����______��
(3)����ͬ�ݻ����ܷ�����A��B,������,A�г���agA����,B�г���agCH4����,A��B�ڵ�ѹǿ֮����4:11,��A��Ħ������Ϊ______��
(4)20mLCaCl2��Һ��ˮϡ����100mL,ϡ�ͺ����Һ��Cl-���ӵ����ʵ���Ũ��Ϊ1mol/L,��ϡ��ǰCaCl2�����ʵ���Ũ��Ϊ______��
(5)��һ���¶Ⱥ�ѹǿ��,3L����A2��9L���������B2��ȫ��������6L���ij����C,�������C�Ļ�ѧʽΪ(��A��B��ʾ)______��
���𰸡�![]() 1/5 44g/mol 2.5mol/L AB3��B3A
1/5 44g/mol 2.5mol/L AB3��B3A
��������
��1����״����VL���������ʵ���Ϊ![]() mol������Ϊ
mol������Ϊ![]() mol��17g/mol=
mol��17g/mol=![]() g���ܽ���1Lˮ�У�������Һ������Ϊ
g���ܽ���1Lˮ�У�������Һ������Ϊ![]() g+1000g�����Ϊ��V=
g+1000g�������V=![]() =
=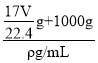 =
=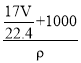 mL����
mL����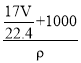 ��103L������Һ�����ʵ����ʵ���Ũ��Ϊ��c=
��103L������Һ�����ʵ����ʵ���Ũ��Ϊ��c=![]() =
= =
=![]() mol/L��
mol/L��
��2����11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4�У�P��Cu3P�У�PԪ�ػ��ϼ۴�0�۽���Ϊ-3�ۣ�P��H3PO4��PԪ�ػ��ϼ۴�0������Ϊ+5�ۣ�CuԪ�ش�+2�۽���Ϊ+1�ۣ��ɷ���ʽ��֪��CuSO4���ϼ۽�������Ϊ15��15mol CuSO4������3molP����1molCuSO4�������������ʵ�����![]() mol=
mol=![]() mol��
mol��
��3��������ͬ�¶Ⱥ�����£������ѹǿ֮�ȵ������ʵ���֮�ȣ���A��Ħ������ΪM�����У�![]() =4��11����֮��M=44g/mol��
=4��11����֮��M=44g/mol��
��4����ϡ��ǰCaCl2�����ʵ���Ũ��Ϊx��ϡ��ǰ�����ӵ����ʵ������䣬��0.02L��x��2=0.1L��1mol/L�����x=2.5mol/L��
��5��ͬһ�����£��μӷ�Ӧ����������֮�ȵ����������֮�ȣ���A2��B2��C�ļ�����֮��=3L��9L��6L=1��3��2���÷���ʽΪA2+3B2=2C������ԭ���غ�֪��C�Ļ�ѧʽΪAB3��B3A��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���3�������Ϊ1.0 L�ĺ����ܱ������з�Ӧ2H2(g)+CO(g)![]() CH3OH(g) �ﵽƽ�⡣����˵����ȷ����
CH3OH(g) �ﵽƽ�⡣����˵����ȷ����
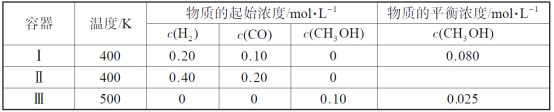
A.�÷�Ӧ������Ӧ����
B.�ﵽƽ��ʱ���������з�Ӧ��ת���ʱ��������еĴ�
C.�ﵽƽ��ʱ����������c(H2)������������c(H2)������
D.�ﵽƽ��ʱ���������е�����Ӧ���ʱ��������еĴ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1�������������ʢ�����״̬��NaCl ��NH3��H2O ��Na2O���� ��ͭ ��BaSO4���� �ƾ� ��Һ̬HCl ��KNO3��Һ���������ڵ���ʵ��ǣ�___________����״̬���ܵ������_____________�����ڷǵ���ʵ���_________________���������������
��2������A��D�ĸ��漰H2O2�ķ�Ӧ������գ�
A. Na2O2�� 2HCl��H2O2��2NaCl B. Ag2O��H2O2��2Ag��O2����H2O
C. 2H2O2��2H2O��O2�� D. ��H2O2����KMnO4����H2SO4����MnSO4����K2SO4����H2O����O2��
����ƽD����ʽ��ϵ�����ڷ�����____���÷�Ӧ�Ļ�ԭ����_________________��
��H2O2�����������ԣ������ֻ�ԭ�Եķ�Ӧ��________��H2O2�Ȳ����������ֲ�����ԭ���ķ�Ӧ��__________��(���ô�������)
������˫���ŷ���ʾB��Ӧ�е���ת�Ƶķ������Ŀ��___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ������Fe��Fe2O3��CuO�Ļ����������Ϊ100 mL���ʵ���Ũ��Ϊ2.2 mol/L��H2SO4��Һ�У���ַ�Ӧ����������896mL����״�������õ����ܹ���1.28 g�����˺���Һ�еĽ�������ֻ��Fe2+��������Һ�����Ϊ100mL��������Һ�м���2 mol/L NaOH��Һ��40mLʱ��ʼ���ֳ�������δ�μ�NaOH��Һǰ��Һ��FeSO4�����ʵ���Ũ��Ϊ
A. 1.8 mol/LB. 2 mol/LC. 2.2 mol/LD. ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʵ�����Ʊ���������֤�������ʵ�װ��(���мг�װ����ʡ��)��
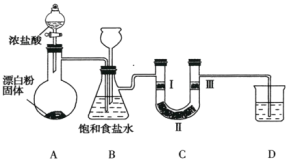
��֪��װ��A�������ķ���װ�ã���Ӧ�Ļ�ѧ����ʽΪ![]() ��
��
�ݴ˻ش��������⣺
(1)װ��B�б���ʳ��ˮ��������_________��
(2)װ��BҲ�ǰ�ȫƿ��Ŀ���Ǽ��ʵ�����ʱװ��C���Ƿ�����������д��װ��C�з�������ʱװ��B�е�ʵ������__________________��
(3)װ��C����������֤�����Ƿ����Ư���ԣ���װ��C��I��������Ӧ�����������___________(����ĸ)��
��� | I | �� | �� |
a | �������ɫ���� | ��ʯ�� | ʪ�����ɫ���� |
b | �������ɫ���� | ��ˮ����ͭ | ʪ�����ɫ���� |
c | ʪ�����ɫ���� | Ũ���� | �������ɫ���� |
d | ʪ�����ɫ���� | ��ˮ�Ȼ��� | �������ɫ���� |
(4)װ��D��������_____________________________��
(5)�����20mL��10mol��L-1��Ũ����������������Ƴ�ַ�Ӧ��ʵ�����ռ����������ڱ�״���µ������__________��
A.��2.24 L B.��2.24 L C.��2.24 L D.��2.24 L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���̲������������ڻ��������ʵ��,��ش������й�����
ʵ��һ:ͨ������ķ�����ȥ����ˮ�к��е������ӵ�������ȡ����ˮ,��ͼ��ʾ

��1�����������������:��___________ ��_____________
��2������������װ�÷���ƾ������Ȼ�̼������Һ�Ļ����,��ȱ�ٵ�������______________,������������������е�ʵ�������������______________;���Ľ�ˮ����__________ (����f������g��)
��3���������г��������Ƭ,��������Ŀ����___________________
ʵ���:��CCl4�ӵ�ˮ����ȡI2����Һ©������������Һ.
��ʵ�����������������:
����©���Ͽڲ�������ʹ���ϵİ��ۻ�С��©����С��.
�����÷ֲ��,��������,���ձ������²�Һ��
��4���²���������_____________��Һ,�ϲ�Һ���_________________ �õ�(�����Ͽ��������¿���)
��5����ȡ��ˮ�е�I2����ʱҪ�õ���ȡ��,���й���������ȡ����˵����ȷ������______��
A.����ⷴӦ
B.�������е��ܽ�ȴ�����ˮ�е��ܽ��
C.����ȡ����ˮ���������ܶȲ�ͬ
D.����ѡ��CCl4�� �ƾ�������ȡ��.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪԪ�����������ڵĺ����ֲ���������б�������ȷ����
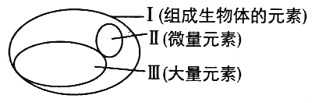
A.���ڷ�������ж����ҵ�����������������������ͳһ��
B.�������٣���ȴ���������������������ȱ�ٵ�
C.��͢��Ϊ����Ԫ�أ�һ��ȱ���Ϳ��ܻᵼ����Ӧ�IJ�֢
D.P��S��K��Ca��Zn���ڴ���Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[��ѧ--ѡ��5���л���ѧ����]
�����ϩ�����ڼ����������ܿ��پۺ�Ϊ ���Ӷ����н���ԣ�ij�������ϩ������G���ĺϳ�·�����£�
���Ӷ����н���ԣ�ij�������ϩ������G���ĺϳ�·�����£�
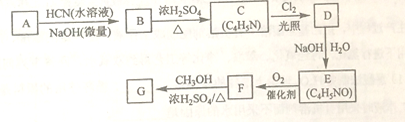
��֪��
��A����Է�����Ϊ58����Ԫ����������Ϊ0.276���˴Ź���������ʾΪ����
��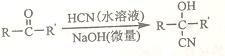
�ش��������⣺
��1��A�Ļ�ѧ����Ϊ_______��
��2��B�Ľṹ��ʽΪ______����˴Ź���������ʾΪ______��壬�������Ϊ______��
��3����C����D�ķ�Ӧ����Ϊ________��
��4����D����E�Ļ�ѧ����ʽΪ___________��
��5��G�еĹ�������___�� ____ ��_____��������������ƣ�
��6��G��ͬ���칹���У���G������ͬ���������ܷ���������Ӧ�Ĺ���_____�֡������������칹��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵�����ʾ������ȷ���ǣ� ��
A. ��ϡ��Һ�У�H2SO4��Ba(OH)2���к���Ҫ����57.3kJ/mol
B. 2C��s��+O2��g���T2CO��g����H ��O����S��O
C. ��֪��2SO2(g) +O2(g)![]() 2SO3 (g) ����H=��98.3kJ/mol����1molSO2��0.5molO2����һ�ܱ������з�Ӧ���ų�49.15kJ������
2SO3 (g) ����H=��98.3kJ/mol����1molSO2��0.5molO2����һ�ܱ������з�Ӧ���ų�49.15kJ������
D. ��10lkPa��25��ʱ��1gH2��ȫȼ��������̬ˮ���ų�120.9kJ����������������ȼ����Ϊ241.8 kJ/mol
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com