
【题目】下列反应在任意温度下一定能自发进行的是 ( )
A.2NaCl + 2H2O = 2NaOH + Cl2↑ +H2↑ △H > 0
B.NH3(g) + HCl(g) = NH4Cl(s) △H < 0
C.CaCO3(s) = CaO(s) + CO2(g) △H > 0
D.X2Y2(g) = X2(g) +Y2(g) △H < 0
【答案】D
【解析】
反应自发进行的判断依据是:△H-T△S<0,当△H<0,△S>0,△H-T△S<0在任意温度下都成立,反应都能自发进行。
A.2NaCl+2H2O ![]() 2NaOH+Cl2↑+H2↑,该反应是吸热反应△H>0,△S>0,低温下不能自发进行,故A错误;
2NaOH+Cl2↑+H2↑,该反应是吸热反应△H>0,△S>0,低温下不能自发进行,故A错误;
B.NH3(g)+HCl(g)=NH4Cl(s)△H<0,该反应是放热反应△H<0,△S<0,高温下不能自发进行,故B错误;
C.CaCO3(s)=CaO(s)+CO2(g)△H>0,该反应是吸热反应△H>0,△S>0,低温下不能自发进行,故C错误;
D.X2Y2(g)=X2(g)+Y2(g)△H<0,该反应是放热反应△H<0,△S>0,在任意温度下△H-T△S<0都成立,所以任意条件下能自发进行,故D正确;
故选:D。


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:
【题目】2019年3月,我国科学家研发出一种新型的锌碘单液流电池,其原理如图所示。下列说法不正确的是

A. 放电时B电极反应式为:I2+2e-=2I-
B. 放电时电解质储罐中离子总浓度增大
C. M为阳离子交换膜,N为阴离子交换膜
D. 充电时,A极增重65g时,C区增加离子数为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的恒容密闭容器中发生反应:2SO2(g)+O2(g)![]() 2SO3(g),下列证据不能说明反应一定达到化学平衡状态的是( )
2SO3(g),下列证据不能说明反应一定达到化学平衡状态的是( )
A.容器内的压强不再改变B.c(SO2):c(O2):c(SO3)=2:1:2
C.SO2的转化率不再改变D.SO3的生成速率与SO3的消耗速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E均为中学化学常见的纯净物,B为自然界中含量最多的液体,它们之间有如下的反应关系:
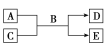
(1)常温下,若A为气态单质,C为非金属氧化物,A、C均能使品红溶液褪色,相对分子质量E>D,则该反应的化学方程式为:________________________________________________________,
检验D中阴离子所用试剂为:________________________________________________________。
(2)若A为短周期的金属单质,D为气态单质,C溶液呈酸性或强碱性时,该反应都能进行。写出C溶液呈强碱性时反应的离子方程式:______________________________________________。
(3)若A、C均为化合物,E为白色沉淀,C为引起温室效应的主要气体,写出E可能的物质的化学式(写两种):______________________,________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验探究小组研究320K时![]() 的分解反应:
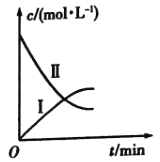
的分解反应:![]() 。如图是该小组根据所给表格中的实验数据绘制的。下列有关说法正确的是( )
。如图是该小组根据所给表格中的实验数据绘制的。下列有关说法正确的是( )
t/min | 0 | 1 | 2 | 3 | 4 |
| 0.160 | 0.114 | 0.080 | 0.056 | 0.040 |
| 0 | 0.023 | 0.040 | 0.052 | 0.060 |
A.曲线Ⅰ是![]() 的浓度变化曲线
的浓度变化曲线
B.曲线Ⅱ是![]() 的浓度变化曲线
的浓度变化曲线
C.![]() 的浓度越大,反应速率越快
的浓度越大,反应速率越快
D.![]() 的浓度越大,反应速率越快
的浓度越大,反应速率越快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2020年2月17日下午,在国务院联防联控机制发布会上,科技部生物中心副主任孙燕荣告诉记者:磷酸氯喹对“COVID-19”的治疗有明确的疗效,该药是上市多年的老药,用于广泛人群治疗的安全性是可控的。其合成路线如图所示:

已知:醛基在一定条件下可以还原成甲基。回答下列问题:
(1)有机物A为糠醛,它广泛存在于各种农副产品中。A中含氧官能团的名称为______,A与新制氢氧化铜悬浊液反应的化学方程式为_______。
(2)C的结构简式为________,D与E之间的关系为_______。
(3)反应⑦的反应类型为_______;反应⑤若温度过高会发生副反应,其有机副产物的结构简式为____。
(4)有机物E有多种同分异构体,其中属于羧酸和酯的有______种,在这些同分异构体中,有一种是羧酸,且含有手性碳原子,其名称为_________。
(5)以2—丙醇和必要的试剂合成2—丙胺[CH3CH(NH2)CH3]:_________(用箭头表示转化关系,箭头上注明试剂)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,氧化铁可以与一氧化碳发生下列反应:Fe2O3(s)+3CO(g)![]() 2Fe(s)+3CO2(g)
2Fe(s)+3CO2(g)
(1)该反应的平衡常数表达式为K=________。
(2)该温度下,在2 L盛有Fe2O3粉末的密闭容器中通入CO气体,10 min后,生成了单质铁11.2 g。则10 min内CO的平均反应速率为________。
(3)该反应达到平衡后,加入Fe粉,平衡________移动;保持恒温恒容通入CO,平衡向________移动。(填“向左”、“向右”或“不”)
(4)表明该反应已达平衡状态的是______________
A.单位时间内生成nmolCO同时生成nmolCO2 B.恒容时混合气体的压强不变
C.混合气体的总质量不变 D.CO2的体积分数不变 E.Fe的浓度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把1mol X气体和0.5mol Y气体混合于2L的密闭容器中,发生如下反应:
![]() ,2min末生成0.2mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol·L-1·min-1,试计算
,2min末生成0.2mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol·L-1·min-1,试计算
(1)前2min内,用X表示的平均反应速率____________。
(2)前2min内Y的转化率____________。
(3)化学方程式中Z的化学计量数n____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组查阅资料得知,漂白粉与硫酸溶液反应可制取氯气,化学方程式为![]() ,他们设计如下实验用于制取氯气并验证其性质。
,他们设计如下实验用于制取氯气并验证其性质。
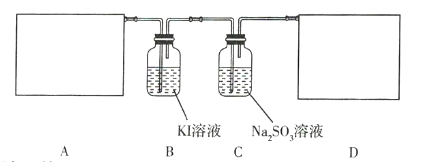
请回答下列问题。
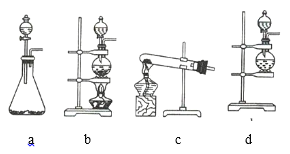
(1)该实验中A部分的装置是 _________________________________ (填序号)。
(2)B中的实验现象为 _____________________________。
(3)用离子方程式表示C中亚硫酸钠被氧化的主要原因: _____________________________。请你帮助他们设计一个实验,证明C中的亚硫酸钠已被氧化: _____________________________(简述实验步骤)。
(4)请根据题意画出D处的实验装置图,并注明装置中盛放的物质__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com