
【题目】光刻胶是大规模集成电路、印刷电路版和激光制版技术中的关键材料,某一光刻胶M的合成路线如下: (部分试剂、反应条件和产物已略去)
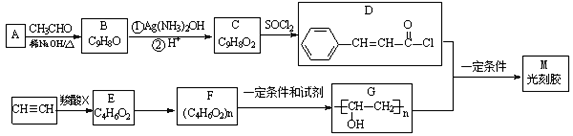
已知:
Ⅰ.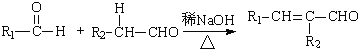 (R1,R2为烃基或氢)
(R1,R2为烃基或氢)
Ⅱ.![]() (R1,R2为烃基)
(R1,R2为烃基)
(1)写出A的结构简式______,B分子中的含氧官能团的名称为_______________。
(2)写出B与银氨溶液发生反应的化学方程式____________________________________。
(3)下列有关光刻胶M的说法正确的是______________________(填字母序号)。
a.可稳定存在于碱性溶液中
b.化学式为C11H10O2
c.可发生氧化反应、还原反应、取代反应
d. 1mol该物质与足量H2发生加成反应时可消耗4mol H2
(4)乙炔和羧酸X发生加成反应生成E,E的核磁共振氢谱有三组峰,且峰面积比为3:2:1, E能使溴水褪色且能发生水解反应,则F的结构简式为________________________。
(5)与C具有相同官能团且含有苯环的同分异构体还有______种(不考虑立体异构);C的另一种同分异构体满足下列条件:①能发生银镜反应和水解反应,其水解产物之一能与FeCl3溶液发生显色反应②苯环上的一氯取代产物只有两种,写出该同分异构体的结构简式:_________。
(6)根据已有知识并结合相关信息,写出以CH3CHO为原料制备CH3CH2CH2COOH的合成路线流程图_______________________(无机试剂任意选用),合成路线流程图示例如下: CH3CH2Br![]() CH3CH2OH
CH3CH2OH![]() CH3COOCH2CH3
CH3COOCH2CH3
【答案】![]() 醛基
醛基  c
c ![]() 4 ,
4 , 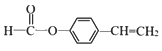 CH3CHO
CH3CHO![]() CH3CH=CHCHO CH3CH=CHCOOH
CH3CH=CHCHO CH3CH=CHCOOH![]() CH3CH2CH2COOH。
CH3CH2CH2COOH。
【解析】
试题根据D,可以反推出A为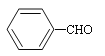 ,B为
,B为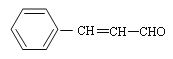 ,C为
,C为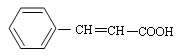 ,羧酸X为CH3COOH,E为
,羧酸X为CH3COOH,E为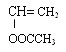 ,F为
,F为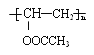 ,根据此分析进行解答。
,根据此分析进行解答。
(1)A是苯甲醛,A的结构简式![]() ,B为
,B为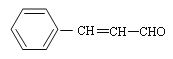 ,含氧官能团为醛基。
,含氧官能团为醛基。
故答案为 ![]() 醛基
醛基
(2)已知B为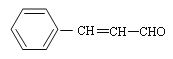 ,和银氨溶液发生化学反应为:
,和银氨溶液发生化学反应为:
故答案为
(3)D与G生成光刻胶,结合信息Ⅱ,光刻胶的结构简式为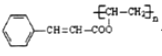 ,
,
A.酯基会与碱溶液发生反应,故A选项错误。
B.光刻胶为聚合物,其单体的化学式是C11H10O2,故B选项错误。
C.由该化合物的结构简式可知,化合物含有C=C和酯基,可以发生氧化反应、还原反应、取代反应,故C选项正确。
D.C=C及苯环均与氢气发生加成反应,则1mol该物质可消耗4nmolH2,故D选项错误。
故答案选C
(4)根据分析可得E的核磁共振氢谱有三组峰,且峰面积比为3:2:1, E能使溴水褪色且能发生水解反应,故E中含有碳碳双键与酯基,E为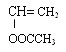 ,F为
,F为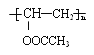 。
。
故答案为![]()
(5)C为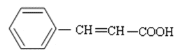 含有相同官能团且含有苯环结构,有乙烯基与羧基在苯环邻位、间位、对位三种和羧基位于乙烯基另外一个碳原子上,共四种同分异构体。能发生银镜反应,其水解产物之一能与FeCl3溶液发生显色反应,说明HCOO-直接与苯环相连;②苯环上的一氯取代产物只有两种,说明苯环有2个对位上的取代基。符合条件的C的同分异构体的结构简式是
含有相同官能团且含有苯环结构,有乙烯基与羧基在苯环邻位、间位、对位三种和羧基位于乙烯基另外一个碳原子上,共四种同分异构体。能发生银镜反应,其水解产物之一能与FeCl3溶液发生显色反应,说明HCOO-直接与苯环相连;②苯环上的一氯取代产物只有两种,说明苯环有2个对位上的取代基。符合条件的C的同分异构体的结构简式是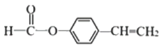 。
。
故答案为 4 
(6)2分子CH3CHO合成CH3CH=CHCHO,CH3CH=CHCHO氧化为CH3CH=CHCOOH,CH3CH=CHCOOH与氢气发生加成反应生成CH3CH2CH2COOH,合成路线是![]()
故答案为![]()


 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:
【题目】1799年,英国化学家汉弗莱·戴维发现了N2O气体。在食品行业中,N2O可用作发泡 剂和密封剂。
(l) N2是硝酸生产中氨催化氧化的副产物,NH3与O2在加热和催化剂的作用下生成N2O的化学方程式为________。
(2)N2O在金粉表面发生热分解反应:2N2O(g)=2N2(g)+O2(g)△H。
已知:2NH3(g)+3N2O(g)=4N2(g)+3H2O(l) △H1=-1010KJ/mol
4NH3(g)+3O2(g) =2N2(g)+6H2O(l) △H2=-1531KJ/mol
△H=__________。
(3)N2O和CO是环境污染性气体,研究表明,CO与N2O在Fe+作用下发生反应:N2O(g)+CO(g)![]() CO2(g)十N2(g)的能量变化及反应历程如下图所示,两步反应分别为:反应①Fe++N2O
CO2(g)十N2(g)的能量变化及反应历程如下图所示,两步反应分别为:反应①Fe++N2O![]() FeO+N2;反应②______________
FeO+N2;反应②______________
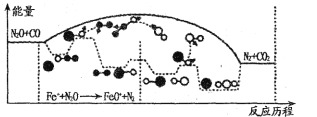
由图可知两步反应均为____(填“放热”或“吸热”)反应,由______(填“反应①或反应②”)决定反应达到平衡所用时间。
(4)在固定体积的密闭容器中,发生反应:N2O(g)+CO(g)![]() CO2(g)+N2(g),改变原料气配比进行多组实验(各次实验的温度可能相同,也可能不同),测定N2O的平衡转化率。部分实验结果如图所示:
CO2(g)+N2(g),改变原料气配比进行多组实验(各次实验的温度可能相同,也可能不同),测定N2O的平衡转化率。部分实验结果如图所示:
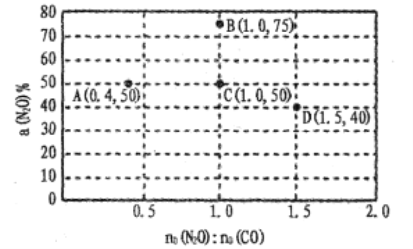
①如果要将图中C点的平衡状态改变为B点的平衡状态,应采取的措施是:____ ;
②图中C、D两点对应的实验温度分别为TC和TD,,通过计算判断TC____TD(填“>”“=”或“<”)。
(5)在某温度下,向1L密闭容器中充入CO与N2O,发生反应:N2O(g)+CO(g)![]() CO2(g)十N2(g),随着反应的进行,容器内CO的物质的量分数变化如下表所示:
CO2(g)十N2(g),随着反应的进行,容器内CO的物质的量分数变化如下表所示:
时间/min | 0 | 2 | 4 | 6 | 8 | 10 |
物质的量分数 | 50.0% | 40.25% | 32.0% | 26.2% | 24.0% | 24.0% |
则该温度下反应的平衡常数K=____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以钛铁矿[主要成分为钛酸亚铁(FeTiO3),含有MgO、SiO2 等杂质]为原料,制备金属钛和铁红的工艺流程如下:已知:①酸溶时,FeTiO3转化为Fe2+和TiO2+;②本实验温度下,Ksp[Mg(OH)2]= 1.0×10-11;请回答下列问题:
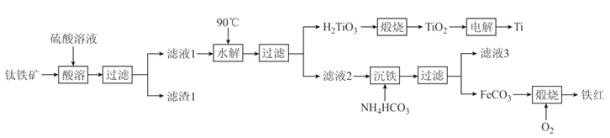
(1)FeTiO3中Ti元素的化合价为_______价。铁红的用途为________________(任写一种)。
(2)“水解”中,发生反应的离子方程式为____________________________________________。
(3)“沉铁”中,气态产物的电子式为_________;该过程需控制反应温度低于35℃,原因为_____________。
(4)FeCO3转化为铁红时,发生反应的化学方程式为________________________________________。
(5)滤液3可用于制备Mg(OH)2。若滤液3 中c(Mg2+)=1.2×10-4 mol·L-1,向其中加入等浓度等体积的NaOH溶液时,通过计算说明有无沉淀生成______________________________(溶液体积近似叠加)。
(6)电解生产钛时用TiO2和石墨做电极,电解质为熔融的CaO,则阴极反应式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香天竺葵醇具有温和、香甜的玫瑰花气息,其结构式如图所示。下列有关香天竺葵醇的说法错误的是
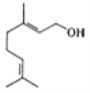
A.分子中含有两种官能团
B.该物质中的碳原子一定全部共面
C.使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色的原理不同
D.香天竺葵醇能发生加聚反应和氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2是目前大气中含量最高的一种温室气体,中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。CO2的综合利用是解决温室问题的有效途径。
(1)研究表明CO2和H2在催化剂存在下可发生反应生成CH3OH。己知部分反应的热化学方程式如下:
CH3OH(g)+ ![]() O2(g) =CO2(g)+2H2O(1) △H1=akJmol-1
O2(g) =CO2(g)+2H2O(1) △H1=akJmol-1
H2(g)+![]() O2(g) =H2O(1) △H2=bkJmol-1
O2(g) =H2O(1) △H2=bkJmol-1
H2O(g) = H2O(l) △H3=ckJmol-1
则 CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H=__________kJmol-1
CH3OH(g)+H2O(g) △H=__________kJmol-1
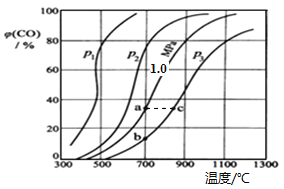
(2)为研究CO2与CO之间的转化,让一定量的CO2与足量碳在体积可变的密闭容器中反应:C(s)+CO2(g)![]() 2CO(g)
2CO(g) ![]() H,反应达平衡后,测得压强、温度对CO的体积分数(φ(CO)%)的影响如图所示。
H,反应达平衡后,测得压强、温度对CO的体积分数(φ(CO)%)的影响如图所示。
回答下列问题:
①压强p1、p2、p3的大小关系是________;Ka 、 Kb 、 Kc 为a、b、c三点对应的平衡常数,则其大小关系是_________。
②900℃、1.0 MPa时,足量碳与a molCO2反应达平衡后,CO2的转化率为___________ (保留三位有效数字),该反应的平衡常数Kp=_________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
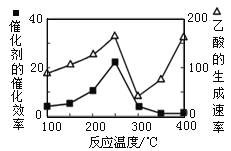
(3)① 以二氧化钛表面覆盖Cu2Al2O4 为催化剂,可以将CO2 和CH4 直接转化成乙酸,CO2(g)+CH4(g)![]() CH3COOH(g)。在不同温度下催化剂的催化效率与乙酸的生成速率如右图所示。250~300 ℃时,乙酸的生成速率降低的主要原因是_____________; 300~400℃时,乙酸的生成速率升高的主要原因是___________。
CH3COOH(g)。在不同温度下催化剂的催化效率与乙酸的生成速率如右图所示。250~300 ℃时,乙酸的生成速率降低的主要原因是_____________; 300~400℃时,乙酸的生成速率升高的主要原因是___________。
② 为了提高该反应中CO2的转化率,可以采取的措施是_____(写一条即可)。
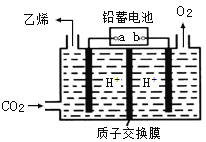
(4)以铅蓄电池为电源可将CO2转化为乙烯,其原理如图所示,电解所用电极材料均为惰性电极。阴极上的电极反应式为___________;每生成0.5mol乙烯,理论上需消耗铅蓄电池中_____mol硫酸。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 、
、![]() 、
、![]() 三种元素的原子具有相同的电子层数,
三种元素的原子具有相同的电子层数,![]() 原子的核电荷数比
原子的核电荷数比![]() 原子的核电荷数大2,
原子的核电荷数大2,![]() 原子的电子总数比
原子的电子总数比![]() 原子的电子总数大4;
原子的电子总数大4;![]() 单质
单质![]() 与足量
与足量![]() 溶液反应可生成
溶液反应可生成![]() (标准状况下)氢气,此时
(标准状况下)氢气,此时![]() 转化为与氖原子具有相同电子层结构的离子。
转化为与氖原子具有相同电子层结构的离子。
(1)写出各元素的名称:![]() ______,
______,![]() ______,
______,![]() ______。
______。
(2)写出![]() 的最高价氧化物对应的水化物与
的最高价氧化物对应的水化物与![]() 的简单氢化物的水溶液反应的离子方程式:____________。
的简单氢化物的水溶液反应的离子方程式:____________。
(3)![]() 形成的简单离子的氧化性比
形成的简单离子的氧化性比![]() 形成的简单离子的氧化性______ (填“强”或“弱”),其原因是______。
形成的简单离子的氧化性______ (填“强”或“弱”),其原因是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO和H2在一定条件下可以合成乙醇(CH3CH2OH):2CO(g)+4H2(g) ![]() CH3CH2OH(g)+H2O(g),下列叙述中能说明上述反应在一定条件下已达到最大限度的是( )
CH3CH2OH(g)+H2O(g),下列叙述中能说明上述反应在一定条件下已达到最大限度的是( )
A. CO全部转化为乙醇
B. 正反应和逆反应的化学反应速率均为零
C. 反应体系中乙醇的物质的量浓度不再变化
D. CO和H2以1:2的物质的量之比反应生成乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是 ( )
A. 甲苯既可使溴的CCl4溶液褪色,也可使KMnO4酸性溶液褪色
B. 有机物![]() 的消去产物有2种
的消去产物有2种
C. 有机物A(C4H6O2)能发生加聚反应,可推知A的结构一定是CH2===CH—COOCH3
D. 可用溴水鉴别直馏汽油、四氯化碳和乙酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如图:
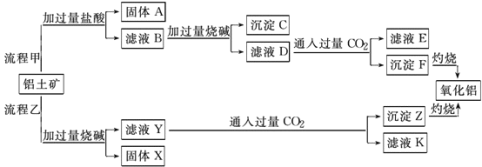
请回答下列问题:
(1)图中涉及分离溶液和沉淀所采取的操作名称是___,该实验操作用到的玻璃仪器___。
(2)检验滤液B含Fe3+,可取少量滤液并加入__(填试剂名称)。
(3)流程甲通入过量CO2后生成沉淀F的离子反应方程式为__。
(4)流程乙加入烧碱溶解SiO2的化学反应方程式___。
(5)能否将向溶液D中通入过量CO2换成加入过量盐酸?___(填 能 或 不能),其理由是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com