
【题目】硫酸铜的制备实验是化学实验教学中一个必做实验,某学习小组设计了如下两个实验方案:
实验一:
因铜不能与稀硫酸反应,实验中用铜和浓硫酸加热使之完全反应,将溶液通过蒸发、结晶等操作得到硫酸铜晶体。
(1)根据上述实验和反应,比较浓硫酸与稀硫酸的性质,浓硫酸具有 。
(2)该反应的化学方程式为 。
实验二:
以空气为氧化剂的一步氧化法,将空气或氧气直接通入到铜粉与稀硫酸的混合物中,其反应原理为2Cu + O2 + 2H2SO4 = 2CuSO4 + 2H2O ,但反应速率太慢,当升高温度到80~90℃,反应仍然缓慢。如在铜粉和稀硫酸的混合物中加入少量Fe2(SO4)3溶液,则速率明显加快。
(3)Fe2(SO4)3的作用是 。
(4)得到的混合液可以用下列四种物质中的 调节溶液的pH =2~4,使Fe3+ 形成Fe(OH)3沉淀而除去:
A.NaOH B. CuO C. CuCO3 D.Fe
(5)请根据以上内容,对这两个实验方案进行评价,填下表:
实 验 (一) | 实 验 (二) | |
主要优点 | 操作简便 | (1)原料充分转化为产品 (2)没有有害气体排放 |
主要缺点 |
【答案】(1)强氧化性;
(2)Cu+2H2SO4 (浓))== CuSO4+SO2↑+ 2H2O;
(3)催化剂;(4)BC;
(5)
实验(一) | 实验(二) | |
主 要 缺 点 | (1)有有毒气体排放 (2)硫酸没有全部转化为产品硫酸铜,不符合绿色化学原理 | (1)操作步骤较多 (2)硫酸铜晶体可能不太纯净 |
【解析】
试题分析:(1)铜不与稀硫酸反应,但和浓硫酸反应,发生Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O,体现浓硫酸的酸性和强氧化性;(2)Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O,体现浓硫酸的酸性和强氧化性;(2)Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O;(3)根据实验现象,加入硫酸铁后,速率明显加快,则硫酸铁作催化剂;(4)调节pH,不能引入新杂质,根据实验目的,加入物质的状态是不溶于水的固体,即选项BC正确;(5)实验一产生SO2,SO2有毒,对环境有影响,铜只与浓硫酸反应,随着反应的进行,浓硫酸的浓度降低,反应将会停止,消耗酸的量增多;实验二步骤繁琐,硫酸铜晶体中混有Fe2+或Fe3+,不纯净。
CuSO4+SO2↑+2H2O;(3)根据实验现象,加入硫酸铁后,速率明显加快,则硫酸铁作催化剂;(4)调节pH,不能引入新杂质,根据实验目的,加入物质的状态是不溶于水的固体,即选项BC正确;(5)实验一产生SO2,SO2有毒,对环境有影响,铜只与浓硫酸反应,随着反应的进行,浓硫酸的浓度降低,反应将会停止,消耗酸的量增多;实验二步骤繁琐,硫酸铜晶体中混有Fe2+或Fe3+,不纯净。


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:
【题目】下列溶液一定是碱性的是( )
A. pH=6的某电解质的溶液 B. c(OH-)>1×10-7mol/L
C. 溶液中含有OH- D. 溶液中c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)250C、101kPa时,____________纯物质完全燃烧生成__________时所放出的热量,叫做该物质的燃烧热。
(2)已知:①P4(s,白磷)+5O2(g)=P4O10(s)△H=—2983.2kJmol-1
②P(s,红磷)+5/4O2(g)=1/4P4O10(s)△H=—738.5kJmol-1
写出白磷转化为红磷的热化学方程式: __。
(3)已知:①Fe2O3(s)+3CO(g)==2Fe(s)+3CO2(g)△H1=-26.7kJ/mol
②3Fe2O3(s)+CO(g)==2Fe3O4(s)+CO2(g)△H2=-50.75kJ/mol
③Fe3O4(s)+CO(g)==3FeO(s)+CO2(g)△H3=-36.5kJ/mol
计算反应:2FeO(s)+2CO(g)==2Fe(s)+2CO2(g)的△H =_ __
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中不正确的是( )
A. 钠在反应TiCl4+4Na===Ti+4NaCl中作还原剂
B. NaOH应密封保存,以防分解变质
C. 盛放KOH溶液的试剂瓶不能用玻璃塞
D. 当足量的CO2通入饱和NaOH溶液中,会有固体析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定温度和压强下的理想气体,影响其所占体积大小的主要因素是
A.分子直径的大小 B.分子间距离的大小
C.分子间引力的大小 D.分子数目的多少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于同分异构体数目的叙述不正确的是( )
A.甲苯苯环上的1个氢原子被含3个碳原子的烷基取代,所得产物有6种
B.已知丙烷的二氯代物有4种同分异构体,则其六氯代物的同分异构体数目也为4种
C.含有5个碳原子的某饱和链烃,其一氯代物有3种
D.菲的结构为 ,它与硝酸反应,可生成5种一硝基取代物
,它与硝酸反应,可生成5种一硝基取代物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】联氨(又称联肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)联氨分子的电子式为_____________,其中氮的化合价为______________。
(2)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为___________。
(3)①2O2(g)+N2(g)=N2O4(l)△H1
②N2(g)+2H2(g)=N2H4(l)△H2
③O2(g)+2H2(g)=2H2O(g)△H3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)△H4=-1048.9kJ/mol
上述反应热效应之间的关系式为△H4=____________,联氨和N2O4可作为火箭推进剂的主要原因为________________。
(4)联氨为二元弱碱,在水中的电离方程式与氨相似。联氨与硫酸形成的酸式盐的化学式为 。
(5)联氨是一种常用的还原剂,可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg的联氨可除去水中溶解的O2 kg;与使用Na2SO3处理水中溶解的O2相比,联氨的优点是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去下列物质中的杂质,所用试剂和方法不正确的是( )
物质 | 杂质 | 除杂质所用试剂和方法 | |
A | KCl溶液 | I2 | CCl4 , 萃取分液 |
B | CO2 | HCl | 饱和NaHCO3溶液,洗气 |
C | Mg粉 | Al粉 | NaOH溶液,过滤 |
D | CaCO3 | CaO | 盐酸,过滤 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个密闭绝热容器(W)中,进行如下两个可逆反应:①A(g)+2B(g)![]() 3C(g)+D(s)△H1>0,②xM(g)+N(g)
3C(g)+D(s)△H1>0,②xM(g)+N(g)![]() 3Q(g)△H2.反应①中各物质与反应②中各物质均不发生反应. M的转化率与温度、压强的关系如图所示.
3Q(g)△H2.反应①中各物质与反应②中各物质均不发生反应. M的转化率与温度、压强的关系如图所示.
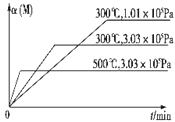
下列对W容器中进行的反应推断合理的是( )
A.x=2
B.平衡时, v 正 (B):v 逆 (C)=2:3
C.若保持容器容积不变,充入N,则C的物质的量减小
D. 若保持容器容积不变,充入Q,反应①的平衡常数不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com